Кондуктометрический метод анализа
Кондуктометрический метод анализа
Введение
Кондуктометрия (от англ.
conductivity - электропроводность и метрия) - совокупность электрохимических
методов анализа, основанных на измерении электропроводности растворов.
Кондуктометрия применяется для
определения концентрации растворов солей, кислот, оснований, для контроля
состава некоторых промышленных растворов.
Достоинства кондуктометрия: высокая
чувствительность (ниж. граница определяемых концентраций ~10-4-10-5 М),
достаточно высокая точность (относит, погрешность определения 0,1-2%), простота
методик, доступность аппаратуры, возможность исследования окрашенных и мутных
растворов, а также автоматизации анализа.
Кондуктометрический анализ основан
на изменении концентрации вещества или химического состава среды в
межэлектродном пространстве; он не связан с потенциалом электрода, который
обычно близок к равновесному значению. Кондуктометрия включает прямые методы
анализа (используемые, например, в солемерах) и косвенные (например, в газовом
анализе) с применением постоянного или переменного тока (низкой и высокой
частоты), а также хронокондуктометрию, низкочастотное и высокочастотное
титрование.
Объект контрольной работы -
электрохимические методы исследования.
Предметом работы является кондуктометрия.
Цель работы - раскрыть сущность
кондуктометрии.
Для выполнения поставленной цели
необходимо решить ряд задач:
раскрыть понятие кондуктометрии;
охарактеризовать методы
кондуктометрии;
рассмотреть кондуктометрическое
титрование.
1. Теоретические основы
кондуктометрического метода анализа
Кондуктометрические методы анализа
основаны на измерении электропроводности исследуемых растворов. Существует
несколько методов кондуктометрического анализа:
прямая кондуктометрия - метод,
позволяющий непосредственно определять концентрацию электролита путем измерения
электропроводности раствора с известным качественным составом;
кондуктометрическое титрование -
метод анализа, основанный на определении содержания вещества по излому кривой
титрования. Кривую строят по измерениям удельной электропроводности
анализируемого раствора, меняющейся в результате химических реакций в процессе
титрования;
хронокондуктометрическое титрование
- основано на определении содержания вещества по затраченному на титрование
времени, автоматически фиксируемого на диаграммной ленте регистратора кривой
титрования.
Кондуктометрия
Кондуктометрия относится к наиболее
распространенным методам исследования растворов и жидких систем вообще.
проводящими принято условно с χ ~10-7 Ом-1·см-1 и выше;
умеренно проводящими с χ: 10-7 - 10-11 Ом-1 ·м-1;
непроводящими - χ ниже 10-11 Ом-1 ·м-1.
Данная классификация условна.
В ФХА принято пользоваться
диаграммами «удельная электропроводность χ - состав». Поскольку электропроводность относится к заведомо не аддитивным
свойствам, способ выражения концентрации при этом может быть произвольным,
однако для наглядности чаще всего выбирают мольные доли. Диаграммы
«молекулярная электропроводность λ - состав» используется реже.
2. Электрическое
сопротивление
Основной константой, характеризующей
электрические свойства вещества, является удельное электрическое сопротивление,
зависящее от природы вещества и от температуры.
Согласно закону Ома удельное
электрическое сопротивление (ρ) [Ом·м]:
 ,
,
где R - электрическое сопротивление,
ом; S - площадь поперечного сечения, м²; l - длина, м.
Температурная зависимость
электрического сопротивления металлов подчиняется закону:
ρt = ρ0 (1+αt),
где α
- температурный коэффициент.
Электрическая проводимость
обусловлена движением заряженных частиц и зависит от количества носителей
заряда и их подвижности.
Для разбавленных твердых растворов,
их удельное электрическое сопротивление по правилу Маттиссена представлено из
двух слагаемых:
ρ = ρ(t) + ρ(x),
где ρ(t)
- электрическое сопротивление чистого металла, зависящее от
температуры метала; ρ(x) остаточное электрическое сопротивление, не зависящее от
температуры и определяется типом примеси и ее концентрацией.
Эта формула применима при содержании
примеси до 1 ат.% Согласно правилу Линде, добавочное электрическое
сопротивление, вызываемое содержанием примеси 1 ат.%, пропорционально квадрату
разности валентностей чистого металла и примеси (∆z):
∆ρ(x) = a + b(∆z) 2,
где a, b - величины, определяющие
свойства металла - растворителя.
Правило Маттиссена достаточно хорошо
выполняется для большинства разбавленных металлических расплавов, правилу Линде
многие расплавы не подчиняются.
Механизм электрической проводимости
в металлических расплавах и твердых металлах принципиально не различается.
Переход металла из твердого в жидкое
состояние сопровождается некоторым изменением электрических свойств: при
плавлении удельное электросопротивление большинства металлов увеличивается в
1,5÷2 раза. Для некоторых
металлов (Bi, Sb, As) характерно аномальное поведение: при плавлении их
удельное электросопротивление уменьшается.
Электрическая проводимость оксидных
расплавов близка к электропроводимости типичных электролитов (галлогениды
щелочных металлов) и зависит от состава шлака и температуры. Это является одним
из доказательств ионной теории строения шлаковых расплавов.
Их ионная структура определяет
преимущественно ионную проводимость в расплавленном состоянии.
Электропроводимость определяется, в первую очередь, размерами катионов и
анионов и силами взаимодействия между ними.
Повышение температуры увеличивает
электропроводимость оксидных расплавов. При переходе из твердого состояния в
жидкое электропроводимость резко возрастает.
Уравнение Я.И. Френкеля
характеризует температурную зависимость электропроводимости ионных кристаллов:
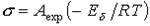
Уравнение применимо и для оксидных
расплавов, в которых перенос тока осуществляется только катионами (которые
много меньше по размеру, чем анионы), т.е. если радиусы анионов велики по
сравнению с катионами, и анионы остаются почти неподвижными в электрическом
поле.
При соблюдении уравнения Я.И.
Френкеля экспертные данные укладываются в прямолинейную зависимость. 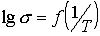 Отклонения свидетельствуют о структурных изменениях, которые
могут быть связаны с разложением комплексных анионов на простые.
Отклонения свидетельствуют о структурных изменениях, которые
могут быть связаны с разложением комплексных анионов на простые.
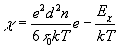
Контактные методы измерения
электрической проводимости расплавов
В основе лежит закон Ома: на
фиксированном участке проводника из жидкого металла, имеющего длину l и площадь
поперечного сечения S, определяется электросопротивление Rχ.
Из соотношения  устанавливают значения удельной электропроводимости металла.
устанавливают значения удельной электропроводимости металла.
Для определения электросопротивления
проводника применяют следующие электрические измерительные схемы: схема
вольтметра-амперметра, в которой при помощи вольтметра измеряют падение
напряжения на концах проводника Vx, а амперметром - силу тока I. В этом случае
значение Rx определяют по закону Ома:  . Точность метода невысока (≤ 1%) и определяется классом
точности приборов.
. Точность метода невысока (≤ 1%) и определяется классом
точности приборов.
Компенсационный метод: в цепь
включают эталонное сопротивление Rэ и с помощью потенциометра измеряют падение
напряжения на проводнике Vx и эталоне Vэ. Расчет по формуле:  более точный метод.
более точный метод.
С использованием моста Уитстона или
двойного моста Томсона. Точность 0,2-0,3%, но необходимо учитывать контактные
сопротивления и сопротивление проводов.
Определение электропроводимости
расплавов связано с техническими трудностями: контакт расплава с электродами,
подбор материалов.
Конструкции измерительных ячеек с
различным расположением калиброванного канала, в котором проводник из жидкого
металла, электроды токовые и потенциальные.
Для расчета удельного электрического
сопротивления (или электрической проводимости) по измеренному (методом моста
или методом вольтметра-амперметра) значению электрического сопротивления
расплава необходимо знать константу ячейки. Градуировку ячейки обычно
производят водным раствором (при комнатной температуре) или расплавом NaCl или
KCl (при 700-900°С).
Значение константы ячейки определяют
по формуле:

где r - сопротивление проводящих
проводов и электродов при соответствующих температурах опыта; Rx измеряемое
сопротивление.
Одним из способов определения r
является предварительное определение.
Чаще используют другой метод,
заключающийся в измерении электросопротивления при двух последовательных
погружениях электродов на различную глубину. Этот способ позволяет исключить
поправку на сопротивление проводов (r), т. к. расчет удельного электрического
сопротивления ведут по разности измеренных сопротивлений:
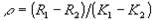
где К1 и К2 константы ячейки при
двух последовательных погружениях электродов.
Конструкция установки разработанной
Б.М. Лепинских и О.А. Есиным (УПИ) с мостовой схемой измерения и ячейкой типа
электрод-электрод.
Регулирование глубины погружения
электродов производится вращением стержня (#), при этом происходит подъем или
опускание тигля при неподвижных электродах.
Среднее значение константы ячейки
устанавливают градуированием по 0,1 н раствору KCl. Этот метод используется для
определения электрической проводимости двойных шлаковых систем. Схема моста
позволяет измерять сопротивление расплавов с точностью до 0,01 ом.
Относительная ошибка определения удельной электрической проводимости двойных
шлаковых систем. Схема моста позволяет измерять сопротивление расплавов с
точностью до 0,01 ом. Относительная ошибка определения удельной электрической
проводимости достигает 11,8%.
Несомненно, большими аналитическими
возможностями обладает кондуктометрическое титрование. Титрование позволяет
восполнить недостаток селективности определения применением селективного к
анализируемому иону титранта. Известны примеры кислотно-основного,
осадительного, комплексонометрического титрований. Точность
кондуктометрического титрования составляет 1%, но если принять меры по
термостатированию анализируемого раствора, то точность определения можно в
несколько раз увеличить.
Типичный вид кривой
кондуктометрического титрования представлен на рисунке 1.
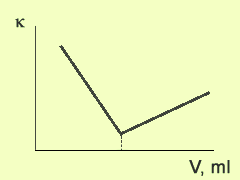
Рис. 1
Точка эквивалентности на графике
находится пересечением двух прямых. Одна прямая (до точки эквивалентности)
отражает изменение концентрации анализируемого иона и ионов титранта, а другая
(после точки эквивалентности) является следствием увеличения концентрации ионов
титранта.
Однако не всегда кривая титрования
имеет такой вид. На рис. 2 приведены в качестве примера кривые титрования,
полученные в результате различных аналитических определений.
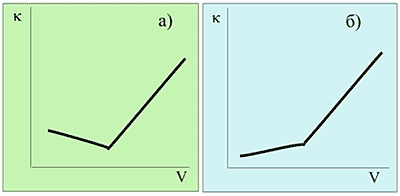
Рис. 2
Вид кривых очевидно различен. В
связи с этим возникает закономерный вопрос о причинах различий и возможности
прогнозирования вида кривой на основании данных о свойствах анализируемого иона
и вещества титранта. В большинстве случаев прогноз возможен, поскольку вид
кривой титрования определяется разностью эквивалентных электропроводностей
анализируемого иона и ионов, составляющих вещество титранта.
Рассмотрим несложный расчет,
позволяющий прогнозировать вид кривой титрования. Прежде всего, нужно ясно
представить себе перечень ионов, принимающих участие в процессе титрования.
Пусть нам предстоит определить хлорид с помощью осадительной реакции с нитратом
серебра (рис. 2а):
Cl- + Ag+ + NO3- = AgCl
+ NO3 -.
Не вызывает сомнения, что в процессе
титрования до точки эквивалентности происходит уменьшение ионов Cl- и NO3-
Увеличение концентрации ионов Ag+ практически не происходит, так как серебро
осаждается ионом Cl- В связи с этим можно утверждать, что динамика
электропроводности происходит со скоростью, пропорциональной сумме
l 0Cl + l 0NO3 =-0,00655 + 0,00617 =
-0,00038 Ом-1 м² г-экв-1.
Знак '-' перед электропроводностью l
0Cl говорит о том, что концентрация Cl в результате титрования уменьшается.
Знак '+' перед l 0NO3 свидетельствует об увеличении концентраци NO3.
Полученное в итоге отрицательное
число -0,00038 Ом-1 м² г-экв-1 указывает на то, что при титрованиии до точки
эквивалентности электропроводность раствора уменьшается.
После точки эквивалентности
электропроводность будет повышатьcя, так как эту ветвь титрования полностью
определяет титрант, т.е. ионы Ag и NO3:
0Ag + l 0NO3 = 0,005436 + 0,00617 =
0,011606 Ом-1 м² г-экв-1.
Прошу обратить внимание на то, что
полученное число положительно, что говорит об увеличении электропроводности
раствора с каждой порцией титранта.
Кривой титрования (рис. 2б) на
рисунке может соответствовать титрование ацетата натрия соляной кислотой.
Почему? Потому, что до точки эквивалентности электропроводность раствора будет
возрастать, а не убывать как в предыдущем случае:
l 0 ацетат + l 0Cl = -0,0034 +
0,00655 = 0,00315 Ом-1 м² г-экв-1.
В заключении хочу предупредить о
том, что любое отклонение кривой титрования от описанных выше видов, должно
настораживать, так как при этом увеличивается вероятность появления больших
систематических ошибок.
4. Методы кондуктометрии
Контактные методы. Измерения
проводят с помощью контактных ячеек (рис. 1, а). При этом используют электроды
из Pt, Ti, нержавеющей стали и др. Для измерения растворов с высокой
концентрацией электролита (10-2-10-3 М) применяют платинированные электроды с
развитой поверхностью.

Рис. 1. Кондуктометрические ячейки и
их эквивалентные электрические схемы: a-контактная ячейка; б-емкостная ячейка;
в-индуктивная ячейка; R-сопротивление электролита; С1-емкость двойного
электрического слоя на межфазной границе электрод - электролит; С2-емкость
раствора; С3-емкость конденсатора, образованного раствором, стенкой ячейки и
внешним электродом; Zф-фарадеевский импеданс, связанный с протекающей на
границе электрод-электролит электрохимической реакцией; L1 и L2-индуктивности
соотв. электролита и катушки
В прямой кондуктометри непосредственно
определяют концентрацию электролита по х его раствора (если между этими
величинами имеется линейная зависимость). Метод применяется главным образом для
анализа разбавленных растворов. В случае концентрирированных растворов
необходимо строить градуировочные графики. Определение веществ в присутствии
других электролитов возможно, если концентрации последних постоянны. На методе
прямой кондуктометрия основаны конструкции солемеров и др. кондуктометрических
устройств, позволяющих определять олеум. а также различных соли в минеральной,
речной и морской водах, физиологических жидкостях и др. Прямую кондуктометрию
применяют при контроле регенерации ионитов, очистки воды, промывки осадков, при
оценке качества вин, соков и других напитков, чистоты органических
растворителей, газов, твердых солей, текстильных материалов, бумаги, зерна,
почвы и т.д. Часто анализируемые образцы предварительно сжигают, а выделяющиеся
газы поглощают подходящими растворами. По электропроводности поглотителей
определяют количества газов (в частности, СО2, NO2, SO2), следовательно -
содержание соответствующих элементов, например С, N, S, в металлах, сплавах и
органических соединениях.
В косвенной кондуктометрия,
позволяющей исследовать смеси электролитов, наряду с электропроводностью
растворов измеряют рефракцию, вязкость, рН, плотность или др. величины.
Например, при анализе промышленных нитрующих смесей, содержащих H2SO4, HNO3 и
Н2О, дополнительно измеряют плотность. По совокупности всех экспериментальных
данных определяют количеств, состав смеси.
Бесконтактные методы. Применяются
для относительных измерений электропроводности, главным образом для
высокочастотного титрования. Измерения проводят с применением емкостных (С-)
или индуктивных (L-) ячеек, представляющих собой сосуды из диэлектрика, которые
соответственно имеют с внеш. стороны не менее двух металлических электродов
(рис. 1, б) или помещены в магнитном поле катушки индуктивности (рис. 1, в).
Электроды С-ячейки или катушка индуктивности соединяются с высокочастотным
генератором. Электропроводность электролита при токе высокой частоты
обусловлена не только реальным перемещением зарядов, но в большей мере потерями
электрической энергии в емкостной и индуктивных ячейках. Это отражается на
реактивной составляющей X полного сопротивления (импеданса) цепи Z2 = R2 + X2,
где R-активное сопротивление, X=XL-ХC, XL и ХC - соответствующее индуктивное и
емкостное сопротивление цепи. Индуктивные ячейки используют обычно для
измерения сравнительно высокой электропроводности, а емкостные - для измерения
низкой электропроводности. Чувствительность измерения повышается в С-ячейках
при использовании диэлектриков с высокой диэлектрической проницаемостью,
уменьшении толщины стенок сосуда и увеличении площади электродов, а в L-ячейках
- с увеличением объема пробы. Применяются также комбинированные LC-ячейки, RC-
и RL-ячейки с повышенной чувствительностью, а также многозвенные ячейки с
различным числом электродов, включенных в фазовращающие контуры
автоколебательных генераторов. При высокочастотном титровании необходимо
предварительно выбирать условия с учетом характеристической кривой ячейки, т.е.
зависимости 1/XL или 1/ХC от х (рис. 3). Чем больше интервал между значениями
(:0 и (:, в котором эта зависимость линейна, тем удобнее ячейка для измерений.
Кроме того, чувствительность измерений различна на различных участках
характеристической кривой; например, в случае кривой 1 чувствительность
наименьшая в максимуме и наибольшая в точках перегиба.
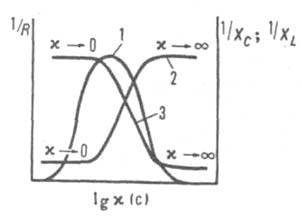
Рис. 3. Характеристические кривые
бесконтактных высокочастотных ячеек: 1,2,3 - зависимости обратных величин
соотв. активной, емкостной и индуктивной составляющих Z от lg
Кривые высокочастотного титрования
имеют минимум (как кривая 1 на рис. 2) или максимум, а также могут представлять
собой М-образные кривые. Бесконтактные методы уступают контактным по точности,
но превосходят их по чувствительности. Кроме того, из-за отсутствия
взаимодействия материала электрода с исследуемой средой эти методы позволяют
проводить измерения при высоких и низких температурах, в агрессивных средах, в
замкнутых объемах. Они применяются для кислотно-основных титрований на фоне
дифференцирующих растворителей (СН3СООН, ацетон, диоксан и др.), детектирования
веществ в хроматографии, экспресс-анализа органических соединений, воздуха и
промышленных газов, анализа хим. реактивов, контроля качества лекарственных
средств в запаянных ампулах, для изучения комплексообразования, гидролиза,
сольватации, фазовых переходов.
Заключение
Кондуктометрия - совокупность
электрохимических методов анализа, основанных на измерении электропроводности х
жидких электролитов, которая пропорциональна их концентрации. Аналитическое
использование кондуктометрии обладает характерными чертами, связанными с низкой
селективностью кондуктометрического детектирования. В самом деле, близкие
значения эквивалентных электропроводностей ионов не позволяют говорить о том,
что какой-либо ион может целиком определять электропроводность всего раствора.
Таким образом, измерения электропроводности может приносить реальную
аналитическую пользу только в том случае, если соотношение ионов в
анализируемой смеси неизменно от пробы к пробе. Это, так называемая, задача
определения разбавления исходного раствора. Примерами могут служить анализ
промывных вод в ваннах отмывки гальванического производства, контроль за
приготовлением технологических растворов в производственных условиях и т.п.
Кондуктометрические методы
характеризуются высокой экспрессностью, простотой и доступностью измерительных
приборов, удобством работы и достаточной точностью. Ценной особенностью
кондуктометрических методов является возможность проведения автоматического и
дистанционного анализа. Прямые кондуктометрические измерения имеют погрешность
1-2%, при соблюдении специальных условий она снижается до 0,2%.
Список литературы
электропроводность сопротивление
проводник кондуктометрический
1. Харитонов Ю.Я. Аналитическая химия. Кн. 2. - М.: Высшая школа.
2003. - 345 с.
. Брайнина Х.З., Нейман Е.Я., Слепушкин В.В. Инверсионные электроаналитические
методы. - М.: Химия, 1988. - 239 с.
. Электрохимические методы в контроле окружающей среды. - М.:
Химия, 1990. - 238 с.
. Сурова Н.А. Использование вольтамперометрической
компьютеризированной системы для анализа экологических объектов // Ученые
записки Симферопольского государственного университета. Математика, физика,
химия. - 1997. - №4 (43). - С. 112-119.
. Гейровский Я., Кута Я. Основы полярографии. - М.: Мир, 1965. -
295 с.
. Ройзенблат Е.М., Веретина Г.И. О чувствительности определения ртути
методом инверсионной вольтампереметрии на графитовом электроде // Журн. аналит.
химии. - 1974. - Т. 29, №12. - С. 2376-2380.
. Будников Г.К. Определение следовых количеств веществ как
проблема современной аналитической химии // Соросовский Образовательный Журнал.
2000. Т. 6, №3. С. 45-51.
. Эйхлер В. Яды в нашей пище. М.: Мир, 1993. - 189 с.
. Золотов Ю.А., Кимстач В.А., Кузьмин Н.М. и др. // Рос. хим.
журн. 1993. Т. 37, №4. С. 20-27.
. Майстренко В.Н., Хамитов Р.З., Будников Г.К.
Эколого-аналитический мониторинг супертоксикантов. М.: Химия, 1996. - 319 с.
. Будников Г.К. Диоксины и родственные соединения как
экотоксиканты // Соросовский Образовательный Журнал. 1997. №8. С. 38-44.