Пігментосинтезувальна активність бактеріальних та дріжджових клітин за дії важких металів
Здатність до утворення
пігментів у мікроорганізмів детермінована генетично і тому може
використовуватися як ідентифікаційна ознака.
Продигіозин - один із
кількох вторинних бактеріальних метаболітів, що мають незвичайну структуру, у
якій метоксибіпірольний фрагмент включений у дипірометиленову структуру.
Результати багатьох експериментів показують, що продигіозин діє як
аутоокиснений акцептор, тим самим підтверджується його можлива участь у диханні
мікроорганізмів. В утворенні продигіозину беруть участь амінокислоти.
Припускають, що накопичення амінокислот у середовищі в період стаціонарної фази
призводить до більш швидкої появи літичних процесів. Це припущення підтверджує
спостереження, що пігментований штам має більш пізній автолітичний процес, ніж
безпігментний. Утворення пігменту в цьому випадку можна розглядати як
адаптивний процес, викликаний зміною фізіологічного стану клітини. Інша точка
зору відносно біологічного значення пірилдіпірилметенових пігментів заснована
на їх здатності пригнічувати в лабораторних умовах ріст мікроорганізмів.
Великий інтерес становить спостереження, що екзогенний продигіозин є потужним
сенсибілізатором для деяких мікроорганізмів.
Піоцианін, який входить
до класу феназинових пігментів, являє собою антибіотик бактерій виду
Pseudomonas aeruginosa; активний проти всіх грампозитивних бактерій. Механізм
утворення феназинового кільця піоцианіну все ще не з’ясований, хоча це питання
вивчали кілька груп учених. Ранні досліди Blackwood і Naish на зростаючих
культурах Pseudomonas aeruginosa показали, що гліцерин або діоксиацетон є
кращими попередниками, ніж глюкоза, ацетат або фенілаланін. Ці дані дозволяють
припустити, що піоцианін синтезується з проміжної сполуки, яка містить три
вуглецеві атоми. Феназини, що синтезуються одним видом, можуть впливати на інші
види та їхні тканини, причому цей вплив здійснюється різними шляхами. Вони одні
з найперших бактеріальних продуктів, для яких була показана антибіотична
активність проти інших мікроорганізмів. Бактеріостатичні властивості іодиніну
та піоцианіну сьогодні вивчені детально. Є дані, що феназини володіють
канцеростатичною активністю.
Іншою групою пігментів
мікроорганізмів є каротиноїди, які належать до групи природних пігментів,
забарвлених у жовтий, помаранчевий та червоний кольори. Специфічною ознакою
каротиноїдів є наявність хромофора, що складається із низки кон’югованих
подвійних зв’язків, кількість яких визначає характер забарвлення пігменту. Вони
синтезуються рослинами, найпростішими, грибами та бактеріями.
Каротиноїдам притаманна
антиоксидантна, протипухлинна та імуностимулювальна активності, а ß-каротин є
провітаміном жиророзчинного вітаміну групи А. З огляду на це, каротиноїди
зазвичай використовуються у виробництві кормів для тваринництва, харчовій та
фармацевтичній промисловості, косметології як природні барвники або харчові
добавки.
Відомо, що каротиноїди,
які входять до складу вегетативних клітин Bacillus, мають жовте забарвлення, а
пігменти спор - помаранчеве. Така здатність бактерій роду Bacillus може бути
використана для створення біосенсорів. Проте слід зазначити, що прокаріоти та
одноклітинні еукаріоти є найменш вивченими з точки зору
організмів-сигналізаторів забруднень. На сьогодні новим напрямком досліджень у
біоіндикації є використання пігментосинтезувальних бактерій як біоіндикаторів.
Мікроорганізми найбільш чутливо реагують на зміни складу середовища та здатні
швидко оновлювати біомасу, цим пояснюються переваги їх застосування в
біоіндикаційних дослідженнях. Однак клітина прокаріот відрізняється від
еукаріотичної клітини не тільки відсутністю ядра і багатьох органоїдів, але й
спрощенням розмноження та особливостями дихання і харчування.
Тому метою нашої роботи
було здійснити порівняльний аналіз олігодинамічної дії важких металів (ВМ), як
одних із найпріорітетніших ксенобіотиків довкілля, на синтез пігменту
прокаріотичних і одноклітинних еукаріотичних організмів.
Дріжджі роду Rhodotorula
культивували на твердому поживному середовищі Сабуро (бактерії - на МПА). У
розплавлені середовища попередньо вносили солі ВМ (у перерахунку на катіон).
Засівали мікроорганізми суцільним газоном методом Дригальського. Щільність
суспензії становила 107 кл/см3. Культивування проводили в термостаті. Дріжджі
та бактерії Serratia marcescens культивували за температури 28-29 0С,
Pseudomonas aeruginosa - за 37С.
Облік результатів
засівання бактерій на МПА з металами проводили візуально на 2 добу
культивування (Ag+ - на 5 добу), дріжджів (та бактерій на середовищі МПА з
сульфатом і хлоридом міді) - на 3 добу культивування, порівнюючи дослідні зразки
з контролем. Для розрахунку різниці в інтенсивності кольору пігменту (dE) між
дослідними чашками та контролем дріжджові колонії фотографували, розміщали
фотографії в комп’ютерну програму Adobe Photoshop. Потім визначали показники
каналів кольорової моделі (Lab) і в програмі CIEDE 2000 розраховували різницю в
інтенсивності кольору пігменту. Статистичну обробку проводили за допомогою
комп’ютерних програм «Microsoft Office Excel 2007» і «Statistica 10».
Серед пігментів можуть
зустрічатися представники різних класів речовин: каротиноїди, феназинові
барвники, піроли, азахінони, антоціани тощо, які здатні виконувати певні
функції в клітині (табл. 1).
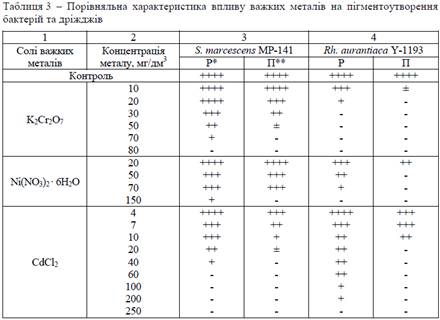
Дослідження показали, що
концентраційні інтервали (КІ) між втратою пігменту та блокуванням росту
простежувалися в дріжджових клітин і були в межах від 25 до 90% . Для бактерій
S. marcescens КІ були лише для хлориду та сульфату цинку - 16,7 та 20% ,
відповідно (табл. 2). Дріжджові клітини виявилися дещо чутливішими за
бактеріальні щодо дії на них більшої частини важких металів (табл. 3).
Концентрації, з яких починалося блокування синтезу пігменту в Rh. aurantiaca
Y-1193, були набагато меншими, ніж у бактерій S. marcescens MP-141 (для
біхромату калію, нітрату нікелю, хлориду кадмію, хлориду міді, хлориду та
сульфату цинку в 3,5, 3, 2, 1,3, 1,25, 4 рази меншими, відповідно). Проте для
сульфату міді та нітрату срібла, навпаки, концентрації, з яких блокувався
синтез пігментів, були нижчими у А marcescens MP-141, ніж у дріжджів (у 2 та 3
рази, відповідно).
грампозитивний пігмент піоцианін
Таблиця 1 -
Характеристика деяких груп пігментів мікроорганізмів
|
Ознака
|
Піролові похідні (продигіозин)
|
Феназинові пігменти (піоцианін,
іодинін)
|
Каротиноїди
|
|
Попередники синтезу
|
Амінокислота пролін
|
Феназин-1,6-дикарбонова кислота
|
Фітоїн, фітофлюїн, лікопін
|
|
Смуги поглинання, нм
|
530-535 (у кислих розчинах),
460470 (у лужних умовах)
|
400-600
|
280-550
|
|
Оптимальні Умови утворення
пігментів
|
T, °С
|
28-30
|
37
|
28-30
|
|
pH
|
6,0-6,5
|
7,2
|
2-6
|
|
Речовини, необхідні для синтезу
пігментів
|
Вітаміни (тіамін), аніони SO4
", мікроелементи (Mg, Zn, Mn, Rb, Ca, Fe), амінокислоти (гліцин, аланін
тощо)
|
Глюкоза, азот, фосфор; поживне
середовище на основі бурякового відвару
|
Для дріжджів роду Rhodotorula:
глюкоза; вуглець та азот (у співвідношенні 40:1)
|
|
Розчинність у воді
|
Не розчинні
|
Розчинні
|
Нерозчинні
|
|
Представники
продуцентів-мікроорганізмів
|
Serratia marcescens, Actinomyces
coelicolor, Act. longisporum, Act. Longispororu-ber
|
Види Pseudomonas, Streptomyces,
Brevibacte-rium, Nocardia
|
Гриби (Mucoraceae), дріжджі
(Sporobolomycetacea), актиноміцети (Actinoplanaceae), найпростіші, бактерії
(Micrococcaceae)
|
|
Біологічне значення
|
Беруть участь у диханні
|
Створюють окислювально-відновну
пару, здатну до передачі електронів
|
Беруть участь у фотосинтезі,
фототропізмі, фото- рецепції; володіють антиоксидантною активністю
|
Таблиця 2 - Значення
концентраційного інтервалу між втратою пігменту та інгібуванням росту в
мікроорганізмів під впливом важких металів
|
Солі важких металів
|
Культу
|
ри пігментосинтезувальних
мікроорганізмів
|
|
Serratia marcescens MP- 141
|
Rhodotorula aurantiaca У-1193
|
Pseudomonas fluorescens var.
pseudo-iodinum МР-11
|
Rhodotorula glutinis У-1335
|
|
Концентраційні інтервали між
втратою пігменту та блокуванням росту,%
|
|
K2Cr207
|
- *
|
-
|
-
|
75
|
|
№(N03)260
|
-
|
50
|
-
|
-
|
|
Cda2
|
90
|
-
|
62,5
|
|
AgN0з
|
-
|
25
|
-
|
-
|
|
СиСЬо
|
-
|
50
|
Не досліджували
|
58,3
|
|
CuS04
|
-
|
50
|
-
|
-
|
|
Zna2
|
16,7
|
20
|
-
|
-
|
|
ZnS04
|
20
|
33,3
|
-
|
37,5
|
Примітка: -* - не
спостерігалося концентраційного інтервалу.
Розрахунок різниці в
інтенсивності кольору пігменту показав, що з підвищенням концентрації металів в
середовищі значення dE збільшувалося (табл. 4). Так, наприклад, за концентрації
хрому 10 мг/дм3 спостерігався суцільний ріст рожево забарвлених колоній А
marcescens MP-141, dE дорівнювала 4,0 ум. од. Повністю синтез пігменту
блокувався за концентрації Сг6+ 70 мг/дм3, тому dE складала 18,6 ум. од.
Дріжджі Як. ажапкаса Y-П93 виявилися в 3,5 разу чутливішими відносно дії хрому
на синтез пігменту, ніж А татсе8сет MP-14, і втрачали здатність його
синтезувати за концентрації металу 20 мг/дм3, dE була 19,1 ум. од.
Таблиця 4 - Вплив
концентраційного ряду іонів металів на інтенсивність кольору пігменту в
мікроорганізмів
|
Солі важких металів
|
Концентрація металу, мг/дм3
|
S. marcescens MP-141
|
Rh. aurantiaca Y-1193
|
|
|
L
|
a
|
b
|
dE
|
L
|
a
|
b
|
dE
|
|
Контроль
|
44
|
24
|
23
|
-
|
38
|
22
|
34
|
-
|
|
10
|
40
|
21
|
23
|
4,0±0,02
|
21
|
12
|
22
|
14,6±0,05
|
|
20
|
35
|
18
|
20
|
8,5±0,06
|
14
|
12
|
20
|
|
К2СГ2О7
|
30
|
33
|
14
|
21
|
11,3±0,9
|
-
|
-
|
-
|
-
|
|
50
|
28
|
13
|
22
|
15, ±0,2
|
-
|
-
|
-
|
-
|
|
70
|
24
|
10
|
19
|
18,6±1,1
|
-
|
-
|
-
|
-
|
|
20
|
39
|
20
|
22
|
5,0±0,001
|
25
|
13
|
20
|
12,3±0,6
|
|
50
|
33
|
19
|
19
|
|
18
|
11
|
17
|
17,4±0,02
|
|
Nl(NÜ3)2
• 6H2O
|
70
|
33
|
20
|
20
|
9,7±0,8
|
16
|
10
|
18
|
18,5±0,7
|
|
100
|
31
|
17
|
18
|
18,8±0,3
|
14
|
10
|
16
|
20,0±0,04
|
|
150
|
21
|
14
|
18
|
19,2±1,0
|
-
|
-
|
-
|
|
4
|
35
|
15
|
20
|
9,5±0,05
|
35
|
15
|
16
|
9,0±0,03
|
|
7
|
30
|
13
|
20
|
13,6±1,2
|
33
|
14
|
14
|
10,7±0,7
|
|
10
|
28
|
11
|
18
|
15,6±0,07
|
31
|
12
|
11
|
13,1±0,001
|
|
CdCl2
|
20
|
26
|
10
|
16
|
17,2±0,2
|
22
|
11
|
11
|
17,1±0,2
|
|
40
|
23
|
9
|
14
|
19,5±0,05
|
20
|
10
|
12
|
17,8±0,9
|
|
60
|
-
|
-
|
-
|
-
|
19
|
10
|
10
|
19,1±0,04
|
|
100
|
-
|
-
|
-
|
-
|
19
|
9
|
8
|
20,0±0,3
|
|
200
|
-
|
-
|
-
|
17
|
6
|
9
|
21,1 ±0,7
|
|
1
|
33
|
23
|
21
|
9,5±0,06
|
35
|
20
|
30
|
3,0±0,006
|
|
5
|
28
|
14
|
20
|
14,6±0,05
|
33
|
18
|
25
|
5,7±0,001
|
|
7
|
25
|
12
|
17
|
17,1±1,0
|
32
|
18
|
23
|
7,0±0,005
|
|
AgNÜ3
|
10
|
22
|
9
|
16
|
20,1±0,4
|
30
|
16
|
23
|
8,2±0,007
|
|
15
|
-
|
-
|
-
|
-
|
26
|
13
|
19
|
11,9±0,9
|
|
25
|
-
|
-
|
-
|
-
|
18
|
9
|
17
|
17,8±0,3
|
|
30
|
-
|
-
|
-
|
-
|
16
|
8
|
16
|
19,3±0,005
|
|
40
|
-
|
-
|
-
|
15
|
8
|
14
|
20,3±0,02
|
Примітка:
. L, a, b -
показники каналів кольорової моделі CIE Lab.
2. dE - різниця в
інтенсивності кольору між контролем і дослідом, розрахована за допомогою
комп’ютерної програми CIEDE 2000.
Щодо дії ВМ на Ps.
fluorescens var. pseudo-iodinum МР-11 та Rh. glutinis Y-1335, найбільш
чутливими виявилися бактеріальні клітини (табл. 5).
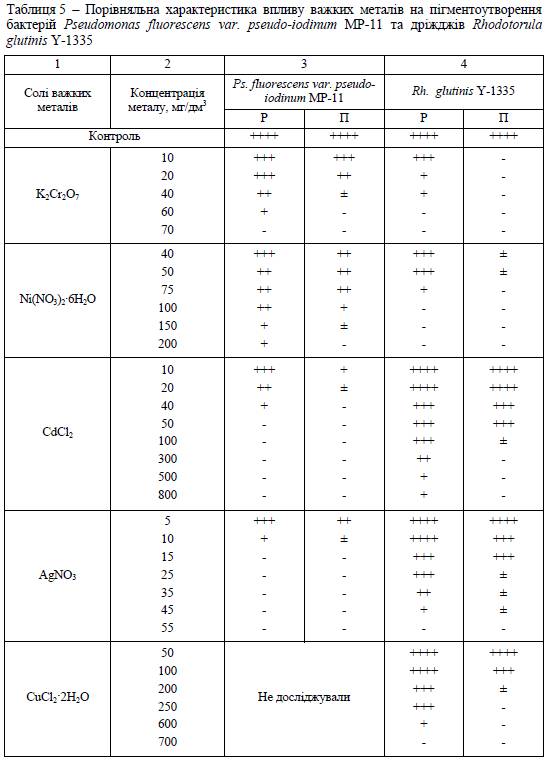
Концентрації ВМ, з яких
починалося інгібування синтезу пігментів, були нижчими у Ps. fluorescens var.
pseudo-iodinum МР-11 (у 7,5, 12 та 1,5 разу для хлориду кадмію, сульфату міді
та хлориду цинку, відповідно), ніж у Ек. glutinis У-1335. Остання культура
проявила найбільшу чутливість за дії іонів хрому, арґентуму та нікелю (за
концентрацій 10, 55 та 75 мг/дм3, відповідно, синтез каротиноїдів повністю
блокувався). Стійкими дріжджі Ек. glutinis У-1335 виявилися під впливом купруму
(сульфату), за концентрації іонів міді 1200 мг/дм3 на чашках спостерігався
слабкий ріст безбарвних колоній.
Ек. glutinis У-1335
реагували втратою каротиноїдів із менших концентрацій (порівняно з втратою
феназинових пігментів Ps. fluorescens var. pseudo-iodinum МР-11) біхромату
калію та нітрату нікелю (у 10 і 2,6 разу, відповідно). Щодо сульфату цинку, то
дріжджі виявилися також чутливішими за бактерії, але нітрат срібла спричинив
більш токсичну дію на Ps. fluorescens var. pseudo-iodinum МР-11. Олігодинамічна
дія купруму (хлориду) на дріжджі Ек. аигаЫшса У-1193 (А) та Ек. glutinis У-1335
(Б) представлена на рис. 1. Іони міді спричинили більш токсичний вплив на
дріжджі Ек. аигапкаса, можливо, це пов’язано з тим, що вони синтезують менший
спектр каротиноїдних пігментів, які виконують в клітині захисну функцію.

Із проведеного
порівняльного аналізу щодо впливу різних концентрацій металів на синтез
пігментів прокаріот та одноклітинних еукаріот можна зробити висновки, що
дріжджові клітини доцільніше використовувати в біоіндикаційних дослідженнях.
По-перше, це пов’язано з
тим, що дріжджі майже для кожного металу мали КІ між втратою пігменту та
блокуванням росту. По-друге, дріжджі здатні реагувати втратою пігменту з менших
концентрацій металів, ніж прокаріотичні клітини.
Проте індикацію нітрату
срібла та сульфату міді доцільніше проводити за допомогою бактерій обох видів,
а хлориду кадмію та цинку - з використанням Ps. fluorescens уаг. pseudo-iodinum
МР-11.
Отже, отримані результати
спонукають нас продовжити дослідження щодо вивчення впливу ксенобіотиків на
синтез пігменту мікроорганізмів із метою їх застосування в біоіндикаційних
дослідженнях.
Висновки.
1. Концентраційні
інтервали між втратою пігменту та блокуванням росту простежувалися в дріжджових
клітин і коливалися в межах від 25 до 90% . Для бактерій S. marcescens MP-141
концентраційні інтервали були лише для хлориду та сульфату цинку - 16,7 та 20%
, відповідно.
2. Розрахунок
різниці в інтенсивності кольору пігменту показав, що з підвищенням концентрації
металів в середовищі значення dE збільшувалося. Так, за концентрації хрому в
середовищі Сабуро 10 мг/дм3 спостерігався суцільний ріст рожево забарвлених
колоній S. marcescens MP-141, dE дорівнювала 4,0 ум. од. Повністю синтез
пігменту блокувався за концентрації Cr6+ 70 мг/дм3, тому dE складала 18,6 ум.
од.
. Дріжджові
клітини виявилися чутливішими за бактеріальні щодо дії на них більшої частини
важких металів і реагували втратою пігменту з менших концентрацій металів, ніж
прокаріотичні клітини, тому їх можна рекомендувати для біоіндикації важких
металів у довкіллі. Проте індикацію нітрату срібла та сульфату міді доцільніше
проводити за допомогою бактерій обох видів, а хлориду кадмію та цинку - з
використанням Ps. fluorescens var. pseudo-iodinum МР-11.