Исследование антиоксидантной активности производных гидрохинона на модели термического автоокисления свиного жира
Введение
Природные многоатомные фенолы представляют собой обширную группу
соединений, разнообразных по физическим и химическим свойствам и обладающих
весьма разносторонним действием на организм человека. Интерес современной науки
к этой группе соединений обусловлен, прежде всего, их высокой биологической
активностью. По мнению многих исследователей, возможный механизм, посредством
которого реализуются некоторые биологические эффекты воздействия фенольных
соединений, связан с проявлением их антиоксидантной активности.
Несколько лет назад в НИИ Химии Антиоксидантов был получен ряд
полифункциональных антиоксидантов, являющихся производными двухатомного фенола
гидрохинона и некоторых его производных. Проведенные исследования показали, что
соединения, синтезированные на основе собственно гидрохинона характеризуются
очень высокими показателями антиоксидантной активности в отношении липидных
субстратов. В то же время, два сульфида на основе 2,6-диметилгидрохинона по
способности ингибировать окисление лярда уступали не только своим
неметилированным аналогам, но и многим монофункциональным антиоксидантам
(дипломная работа Брылевой Е.А).
В связи с вышесказанным, для дальнейшего целенаправленного синтеза
высокоэффективных антиоксидантов, являющихся производными двухатомных фенолов,
необходимо проведение более глубокого исследования по выявлению взаимосвязи
между числом, типом и положением алкильных заместителей в ароматическом кольце
и брутто-ингибирующей активностью соединения.
Вероятно, что аномально низкая активность бензильных сульфидов на основе
2,6-диметилгидрохинона могла быть легко объяснена и даже заранее предсказана,
при сопоставлении данных об антиоксидантной активности гидрохинона и его
алкил-производных. Однако, при анализе литературных источников, такие сведения
нами не были обнаружены.
В связи с этим, целью настоящей дипломной работы является исследование
антиоксидантной активности серосодержащих фенольных антиоксидантов на основе
гидрохинона и его алкил-замещенных аналогов, а также фенольных прототипов этих
соединений на модельной реакции термического автоокисления свиного жира.
Для достижения поставленной цели предполагается решить следующие задачи:
ü исследовать антиокислительные свойства разнообразных
алкилированных производных гидрохинона, а также бензильных сульфидов на их
основе на модели термического автоокисления свиного жира;
ü установить взаимосвязь между числом, типом и положением
алкильных заместителей в ароматическом кольце и периодом индукции соединений;
ü провести сравнительный анализ закономерностей, справедливых в
отношении монофункциональных соединений и тиоалкилфенолов.
Глава 1. Литературный обзор
.1 Механизм неингибированного окисления
Торможение реакций окисления небольшими добавками некоторых веществ -
ингибиторов или антиокислителей хорошо известно и широко применяется на
практике. Вещества, способные задерживать «порчу» органических материалов, в
том числе и жирсодержащих продуктов, применялись ещё в глубокой древности.
Туземцы Южной Америки для сохранения пищевых качеств медвежьего жира добавляли
в него экстракт коры красного ильма. Фармацевты применяли экстракты почек
некоторых деревьев для стабилизации различных мазей на жировой основе. Позднее
было установлено, что в коре и почках деревьев содержатся эфиры галловой
кислоты - эффективные природные антиокислители [1].
Широкое исследование отрицательного катализа окислительных реакций
началось в 20х годах XX
века работами Муро и Дюфресса. В годы первой мировой войны эти исследователи
успешно решили задачу стабилизации акролеина, а затем показали в своих
многочисленных работах широкую распространенность торможения реакций окисления.
Они показали, что ингибиторы сами окисляются в ходе окислительных реакций, но
механизм их действия не был установлен.
В основе современных представлений о стабилизации органических материалов
и механизме действия стабилизаторов лежит теория цепных разветвлённых и
вырожденно-разветвлённых реакций Семёнова Н.Н., нашедшая дальнейшее развитие в
трудах Эмануэля Н.М. и Денисова Е.Т. [2,3].
Окисление алифатических и алкилароматических углеводородов молекулярным
кислородом в жидкой фазе представляет собой радикальный цепной процесс с
квадратичным обрывом цепи [1-9]. Это же относится и ко многим другим
органическим соединениям, в том числе и к большинству карбоцепных полимеров.
Первичным молекулярным продуктом окисления при не слишком высоких температурах
являются перекисные соединения, в основном гидроперекиси, но в некоторых
случаях полиперекиси или H2O2. Детали механизма меняются в зависимости от структуры
окисляемого субстрата, а также от условий окисления. Продукты более глубокого
окисления - карбонильные, карбоксильные и другие соединения образуются в
основном в результате дальнейших превращений перекисных соединений.
Характерная особенность радикально-цепных окислительных процессов -
возможность их резкого замедления путём введения небольших количеств
ингибиторов (стабилизаторов). Добавление стабилизаторов - наиболее эффективное
средство защиты органических материалов от старения. Стабилизаторы с высокой скоростью
реагируют с пероксидными радикалами, обрывая цепной процесс окисления.
Основным компонентом жиров являются глицериды - сложные эфиры спирта
глицерина и жирных кислот. Кислоты могут быть как насыщенными, так и
ненасыщенными. Из насыщенных жирных кислот наиболее распространена
пальмитиновая кислота, содержащаяся практически во всех глицеридах. В
глицеридах растительного происхождения преобладают лауриновая и миристиновая
кислоты, а в глицеридах животного происхождения - стеариновая кислота. Таким образом,
благодаря наличию в молекулах жиров насыщенных и ненасыщенных углеводородных
фрагментов, механизм окисления жирсодержащих продуктов аналогичен механизму
предложенному для окислительной деструкции полимеров, каучуков,
горюче-смазочных материалов, технических масел и топлив.
Механизм окисления углеводородов можно представить схемой [2,3,5-7,9-11]:



Первичные свободные радикалы при окислении чистого углеводорода
образуются в результате бимолекулярного взаимодействия окисляемого вещества с
кислородом (0) или в результате тримолекулярной реакции:
RH + O2 + HR → 2R• + H2O2
Чрезвычайно низкая скорость реакции зарождения цепи затрудняет измерение
ее скорости и изучение детального механизма.
В ряде случаев скорость зарождения цепи искусственно увеличивают,
добавляя в окисляющийся углеводород инициаторы, распадающиеся в условиях
реакции с высокими выходами активных свободных радикалов. Обычно это пероксиды
или азосоединения [7]:


Процессы первичной генерации радикалов весьма разнообразны. В
естественных условиях радикалы образуются при взаимодействии O2 с молекулами основного вещества или более легко
окисляемых примесей, при гомолитическом распаде примесных молекул, в результате
реакций с участием соединений металлов переменной валентности, присутствующих в
следовых концентрациях. Радикалы могут зарождаться также при действии
естественного света, ионизирующей радиации, в реакциях с участием озона и
синглетного кислорода [6].
Образующийся на стадии зарождения цепи радикал R• вызывает далее цепную реакцию окисления, которая протекает
как последовательность многократно повторяющихся актов (1-2) [7,8]
В результате разложения молекул ROOH образуются свободные радикалы, способные инициировать новые цепи
окисления (3). После накопления ROOH в
достаточно высокой концентрации в окисляющейся системе, реакция разложения
гидроперекисей становится главным источником инициирования.
Ионы переходных металлов, в частности железа, кобальта, меди, марганца
являются эффективными катализаторами разложения гидропероксидов [9]. При протекании реакций:
ROOH + Me+ → RO• + OH- + Me2++
Me2+ → RO2• + H+ + Me+
состав образующихся продуктов такой же, как и в отсутствии ионов
металлов. Влияние ионов металлов сводится к уменьшению энергии активации
распада гидроперекисей. В отсутствие примесей цепи обрываются, т. е. свободные
радикалы, участвующие в цепной реакции, гибнут, взаимодействуя между собой
(4-6)
Кроме рекомбинации гибель свободных радикалов происходит в реакциях
диспропорционирования:
R-CH2-CH2• + R-CH2-CH2•
→ R-CH=CH2 + R-CH2-CH3
В присутствие примесей, реагирующих со свободными радикалами, появляются
дополнительные пути обрыва цепи. Так ионы металлов переменной валентности
реагируют с радикалами по схеме:
R• + Me+ → R- + Me2+
Особое значение имеют реакции обрыва цепи ингибиторами - веществами,
реагирующими со свободными радикалами с образованием малоактивных радикалов.
Наиболее эффективные ингибиторы с высокой скоростью реагируют с пероксидными
радикалами, обрывая цепной процесс окисления.
Реакции, протекающие в присутствии ингибитора InH (ингибированное окисление), можно представить схемой
[2-3;5-7;9;10-11]:

Взаимодействуя
с ROO• по реакции (7), стабилизатор снижает концентрацию
пероксидных радикалов и замедляет окисление. Образующийся при этом радикал In•
может вступать в реакцию с другими свободными радикалами, давая молекулярные
продукты. Вместе с тем, этот радикал должен быть малоактивным и не должен
вступать в реакцию (10), чтобы не могли возникнуть новые цепи окисления. Для
эффективного стабилизатора отношение констант скоростей k10/k2 реакций
(10) и (2) должно быть очень малым, а отношение k7/k2 большим.
Эти реакции уменьшают скорость вырожденного разветвления цепей окисления и тем
самым тормозят процесс окисления [1].
1.2 Основные представления о механизме действия фенольных
антиоксидантов
Антиоксидантами (АО) или антиокислителями принято называть соединения
различной химической природы, способные тормозить или устранять свободно-радикальное
окисление органических веществ молекулярным кислородом. Интерес современной
науки к антиоксидантам обусловлен, прежде всего, их практическим значением. В
течение многих лет антиоксиданты широко используются для продления срока службы
и улучшения эксплуатационных качеств полимерных и горюче-смазочных материалов
[1,4,12,13], предотвращения окислительной порчи пищевых продуктов,
жирорастворимых витаминов, кормов и косметических средств [3,8]. Применение АО
в этих областях дает огромный экономический эффект и позволяет сберегать
значительные сырьевые ресурсы.
Среди синтетических антиоксидантов в настоящее время наиболее широкое
распространение получили алкилированные фенолы, что обусловлено как
сравнительной простотой их производства, так и комплексом ценных свойств:
высокой эффективностью, малой токсичностью (что позволяет применять их для
стабилизации пищевых продуктов и материалов бытового назначения),
универсальностью действия и возможностью изменять их свойства в широких
пределах варьированием заместителей [14-17]. Под фенольными антиоксидантами
(ФАО) понимают любые соединения вида Ar(OH)n, в которых одна или несколько гидроксильных групп
соединены с ароматическим ядром, причем молекула АО может содержать несколько
фрагментов Ar(OH)n.
В основе противоокислительного действия ФАО лежит их взаимодействие с
перекисными радикалами:
PhOH + RO2• ® PhO• + RООН (7)
Феноксильный
радикал, образующийся в реакции (7), сравнительно инертен, он не продолжает
цепь окисления, но может взаимодействовать с другими радикалами. Взаимодействие
с RO2 сопровождается образованием несимметричных хинолидных перекисей (QP):
сопровождается образованием несимметричных хинолидных перекисей (QP):
PhO + RO2
+ RO2
 QP (8)
QP (8)
В соответствии с распределением спиновой плотности образуется смесь орто-
и пара-изомеров хинолидных перекисей:

Аналогично
к PhO присоединяются и другие активные радикалы [17].
присоединяются и другие активные радикалы [17].
С
реакцией (8) конкурируют процессы бимолекулярной гибели феноксильных радикалов:
PhO +PhO
+PhO
 продукты (9)
продукты (9)
Их
направление зависит от структуры феноксила. Так, 2,4,6-тризамещенные феноксилы,
имеющие н- или втор-алкильные заместители, вступают в реакции
диспропорционирования с образованием метиленхинона и регенерацией молекулы
исходного фенола:
 9а
9а
Для феноксильных радикалов, у которых хотя бы одно из “активных” 2,4,6 -
положений не замещено, характерна рекомбинация с образованием димерных
фенольных соединений:
 9б
9б
ФАО
и продукты их окисления могут вступать также в реакции (10)-(14). Данные
реакции крайне нежелательны с точки зрения способности ФАО тормозить окислительные
процессы:
PhO + RH
+ RH  PhOH +R
PhOH +R (10)
(10)
QP 2RO2
2RO2 + продукты (11)
+ продукты (11)
PhO
 продукты +R
продукты +R
 RO2
RO2 (12)+ ROOH
(12)+ ROOH RO
RO + PhO
+ PhO + H2O (13)
+ H2O (13)
PhOH + O2 PhO
PhO + HO2
+ HO2 (14)
(14)
В ряде случаев реакции (10)-(14) могут существенно влиять на
противоокислительную активность ФАО, однако для эффективных АО интенсивность
протекания этих реакций невелика, они не вносят существенного вклада в общую
кинетику и их принято считать побочными. [2,5,10,18,19].
В целом, принципиальный механизм ингибированного окисления весьма сложен
и варьирует с изменением структуры АО, а также условий окисления - концентрации
АО, природы окисляемого субстрата, давления кислорода, температуры и пр.
[6,21,22].
1.3 Серосодержащие фенольные антиоксиданты
Среди разнообразных серосодержащих соединений, применяемых в качестве АО,
хорошо зарекомендовали себя, прежде всего органические производные
двухвалентной серы. Атом серы в таких соединениях играет роль восстановителя
гидропероксида, а фенольный гидроксил - гасителя пероксидных радикалов.
 -Гидроксиарилалкантиолы
-Гидроксиарилалкантиолы
 -Гидроксиарилалкантиолы
привлекают особое внимание исследователей не только как исходные продукты для
синтеза разнообразных серосодержащих производных фенолов, но и как эффективные
ингибиторы окислительных процессов.
-Гидроксиарилалкантиолы
привлекают особое внимание исследователей не только как исходные продукты для
синтеза разнообразных серосодержащих производных фенолов, но и как эффективные
ингибиторы окислительных процессов.
Среди
 -гидроксиарилалкантиолов наиболее известен и изучен
3,5-ди-трет-бутил-4-гидроксифенилметантиол (I):
-гидроксиарилалкантиолов наиболее известен и изучен
3,5-ди-трет-бутил-4-гидроксифенилметантиол (I):
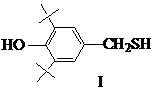
Особенностью тиола (I)
является то, что он способен химически связываться с непредельными субстратами
окисления. Химическое связывание тиола (I) с полимером предотвращает его потери при термообработке
полимера и его контакте с растворителями [26], это равносильно увеличению
эффективности антиоксиданта и продлевает сроки эксплуатации стабилизированных
им полимеров. Присоединение тиола (I) к полимерной цепи осуществляют различными методами, в том числе
механохимической обработкой [27], под действием пероксидного инициатора [28],
краткосрочным высокотемпературным нагреванием [26]. Процесс протекает с
участием тиильного радикала [27] по
схеме:

где
R = 3,5-ди-трет-бутил-4-гидроксибензил
Ингибиторы со сложноэфирными группами
Антиоксиданты на основе пространственно-затрудненных фенолов, содержащие
в своей структуре сложноэфирную группу, находят широкое применение для
стабилизации полимерных материалов, что обусловлено их высокой эффективностью и
простотой получения.
В промышленности выпускается серия антиоксидантов под общим названием
Ирганокс, среди которых можно выделить серосодержащие соединения - Ирганокс
1035 (II) и Ирганокс 416 (III):

II

III
Ирганокс 1035 (другое название Фенозан 30) рекомендуется и для
стабилизации полиолефинов; полиэтилена низкого и высокого давления;
бутен-1-этиленовых, этилен-гексеновых сополимеров; ударопрочного полистирола;
АБС-сополимеров; композиций на основе поливинилфторида, поливинилхлорида,
хлорированного полиэтилена; бутадиенового, стирол-бутадиенового,
изобутиленбутадиенового, полиэфирного каучуков; полиэфирных композиций;
волокон; пленок; поли-пара-ксилилена (парилена); полиакриламида; поликарбоната;
полиамидных волокон; реактивных топлив; полиуретанов; эпоксидных смол [29].
Данное соединение является малотоксичным, поэтому может быть рекомендовано в
качестве добавки к полимерам, контактирующим с пищевыми продуктами [30].
Ирганокс 416 используется в качестве стабилизатора пластмасс [31].
В соединениях (II, III) эфирный фрагмент и атом серы
разделены атомами углерода. Однако большой интерес представляют также
стабилизаторы, содержащие тиоэфирную группу в качестве активного фрагмента.
Тиоэфиры общей формулы (IV):
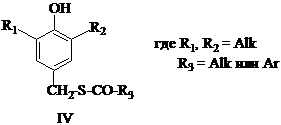
используются как стабилизаторы для жидких горючих веществ (керосин,
газолин), углеводородных масел, петролеумных и натуральных восков,
полиолефинов, эластомеров, включая натуральную резину и синтетический каучук,
полибутадиен (или изопрен) [23].
Соединения типа (V):
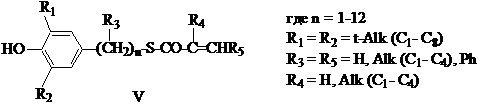
используются для стабилизации полимеров, либо будучи физически
внедренными в полимер, либо будучи сополимеризованными в композиции с другим
мономером. Типы сомономеров: бутадиен-1,3; 2-хлор-бутадиен-1,3; изопрен;
2-этилбутадиен-1,3; 2,3-диметилбута-диен-1,3; а также моноолефины, включающие
винильные или винилдиеновые системы типа стирола, a-метилстирола, дивинилбензола,
винилхлорида, акрилонитрила, 2-винилпиридина и др. [31].
w-(3,5-Ди-трет-бутил-4-гидроксифенил)алкилтиоэфиры карбоновых кислот (VI-IX), полученные на кафедре химии НГПУ, запатентованы как
стабилизаторы полимерных материалов: полиэтилена и композиций на основе
полиэтилена, полимерных композиций на основе сополимера стирола с
полибутадиеном или сополимера стирола с акрилонитрилом и полибутадиеном [32,
33].

VI

VII

VIII

IX
R-(CH2)3-S-CO-(CH2)2-R
R-(CH2)4-S-CO-(CH2)2-R
XI
где R = 3,5-ди-трет-бутил-4-гидроксифенил
Данные соединения превосходят по ингибирующей активности Ирганокс 1035.
Гидроксиарилалкилсульфиды
Среди гидроксиарилалкилсульфидов широко используются в качестве
термостабилизаторов для резин на основе натурального и синтетического каучуков,
полиолефинов и полиэфиров 4,4’-тиобисфенолы - Сантонокс (XII) и Antioxidant 736
(XIII) [24,34,35].


Как
эффективные стабилизаторы полимеров, каучуков и смазочных масел зарекомендовали
себя также 2,2’-тиобисфенолы (XIV, XV) [34]:


Большую известность получил
бис-(2,6-ди-трет-бутил-4-гидроксибензил)сульфид (XVI) или ТБ-3:

ТБ-3
широко используется как эффективный стабилизатор полиолефинов, АБС-сополимеров,
бутадиенового, изопренового каучуков, сополимеров пропилена с бутадиеном,
бутадиен-стирольных термопластичных эластомеров, резин,
олигодиенуретандиэпоксидов, композиций на основе полифениленоксида и
антиокислительная присадка к смазочным маслам [23,34,35,36].
Однако
ТБ-3 как термостабилизатор характеризуется двумя существенными недостатками.
Во-первых, - невысокой термостабильностью, что позволяет использовать его
только в тех случаях, когда переработка полимерной композиции осуществляется
при температуре не выше 200°С. Во-вторых, - ТБ-3 изменяет
естественную окраску полимерной композиции, что ограничивает его использование
в производстве полиэтилена, полипропилена и подобных им материалов.
Для стабилизации полимеров применяют соединения общей формулы (XVII), проявляющие прекрасные
антиоксидантные свойства и не влияющие на цвет полимера (наиболее
предпочтительная концентрация от 0.1 до 1 % по весу.

где R1=R2=Alk (C1-C5);
3= H или CH3; Х=Alk
(C3-C18);
Y= Alk (C1-C8);
n = 0, 1 или 2; q = 1-4
Данные соединения используются в качестве стабилизаторов для следующих
органических субстратов: полимеров, полученных из углеводородов (полиэтилена,
полибутадиена, сополимеров); винильных полимеров с галогеном типа
поливинилхлорида; полимеров из w-ненасыщенных кислот и их производных типа полиакрилатов,
полиакрилонитрила; полимеров из ненасыщенных спиртов и аминов типа поливинилового
спирта, поливинилацетата; гомополимеров и сополимеров, полученных из эпоксидов;
полиацеталей; полифениленоксидов; полиуретанов и полимочевины; поликарбонатов,
полисульфонов; полиамидов из диаминов и дикарбоновых кислот; полиэфиров;
кросс-полимеров из альдегидов с одной стороны, и фенолов, мочевин и меламинов;
амидных смол; ненасыщенных полиэфирных смол; натуральных полимеров типа
целлюлозы, резины, белков и их производных; высокомолекулярных мономерных
веществ типа минеральных масел, животных и растительных жиров, восков и т.д.
[38].
Как стабилизаторы органических материалов заявляются вещества общей
формулы (XVIII):

Данные
соединения используются как антиоксиданты для натуральной и синтетической
резин, полиэтилена, полипропилена, а также покрытий типа масел и смазок
[23,39].
Дисульфиды (XIX-XX) предлагаются в качестве присадок к
дизельным топливам и смазочным маслам [37,39]:


XX
Эффективное
антиокислительное и противокоррозионное действие оказывают также соединения (XXI-XXII)
[39]:

XXI

Большой
интерес в качестве полифункциональных АО представляют соединения типа (XXIII-XXV),
синтезированные ранее на кафедре химии НГПУ:

XXIII


XXV
Дисульфид (XXIII) и сульфиды
(XXIV) запатентованы как высокоэффективные
термостабилизаторы полимерных композиций на основе полиэтилена, полипропилена и
сополимеров стирола [40,41]. Кроме этого, все указанные соединения представляют
интерес в качестве ингибиторов, предотвращающих развитие окислительных
процессов в жирах[42,43,44].
.4 Синергизм в смесях антиоксидантов
Одним из направлений в создании эффективной защиты органических
соединений от окислительной деструкции является применение синергетических
смесей антиоксидантов (АО).
Впервые явление синергизма в смесях АО описали Олкотт и Маттилл, которые
обнаружили, что эффективность природного АО токоферола возрастала в присутствии
органических и некоторых неорганических кислот, которые в индивидуальном
состоянии не являются АО. Для смеси токоферола и аскорбиновой кислоты авторы
предложили и обосновали механизм, согласно которому аскорбиновая кислота
восстанавливает окисленную форму токоферола.
Синергизм - это физико-химическое явление, при котором смесь двух и более
АО при заданной суммарной концентрации тормозит окисление дольше или снижает
его скорость сильнее, чем каждый из компонентов смеси, взятый в отдельности в
концентрации, равной сумме концентраций смеси [7].
Количественно эффект синергизма характеризуется величиной:
Dtсин = t1,2 - (t1 + t2)
где t1,2 - период индукции в присутствии двух
ингибиторов, t1 и t2 - периоды индукции в присутствии
индивидуальных ингибиторов.
В настоящее время известно большое количество синергистов процессов
ингибированного окисления, принадлежащих к различным классам. Разнообразие
химической природы синергистов не позволяет установить какой-то единый механизм
их действия.
Торможение процесса окисления может быть достигнуто тремя способами -
путем ликвидации радикалов, ведущих цепь окисления; путем ликвидации
разветвляющего цепь агента, например, гидроперекисей; путем снижения скорости
инициирования. В соответствии с этим Эмануэлем Н.К. и Карпухиным Г.В.
предложено деление синергетических смесей на 5 групп [45]:
1. Оба ингибитора смеси взаимодействуют с пероксидными радикалами
(ароматические амины или фенолы);
2. Один ингибитор реагирует с пероксидными радикалами, а другой - с
алкильными радикалами (хиноны, нитроксильные радикалы);
3. Один ингибитор реагирует с радикалами, а другой разрушает
гидропероксиды (серо- и фосфорсодержащие соединения);
. Один компонент смеси взаимодействует с радикалами или
гидропероксидами, а другой снижает скорость инициирования (дезактиваторы
металлов, УФ-адсорбен-ты);
. Смесь ингибитора, реагирующего с радикалами или разрушающего
гидропероксиды, с веществом, которое само по себе не тормозит процесс окисления
(органические и неорганические кислоты).
Наиболее сильный эффект обычно проявляют смеси двух ингибиторов, один из
которых обрывает цепи окисления, а другой разрушает гидропероксиды [3,46].
Значительное усиление ингибирующего действия объясняется тем, что каждый из
введенных ингибиторов не только тормозит окисление основного вещества, но и
вместе с тем оба стабилизатора предохраняют друг друга от быстрого
расходования. Так, ингибитор, обрывающий цепи, тормозит образование
гидропероксидов и тем самым предохраняет от быстрого расходования разрушитель
гидропероксидов. Последний, в свою очередь, разрушая пероксиды, уменьшает
зарождение цепей и этим сохраняет первый ингибитор.
В качестве ингибиторов, обрывающих цепи окисления, используют фенолы или
ароматические амины, а в качестве разрушителей гидропероксидов - алифатические
сульфиды и фосфиты, которые взаимодействуют с гидропероксидами по реакциям
[2,46]:


Разрушители
гидропероксидов в процессе окисления могут вступать в побочную реакцию с
пероксидными радикалами без обрыва цепи окисления [46]:


что
снижает эффективность их действия.
Тормозящее
действие ингибиторов, разрушающих гидропероксиды, тем сильнее, чем выше
скорость взаимодействия этих веществ с гидропероксидами [3].
Распространенные
синергетические смеси АО обычно содержат не менее двух компонентов, что
приводит к определенным трудностям их применения [46]. Чтобы получить
гомогенную смесь всех компонентов необходимо растворить их в подходящем
растворителе, что бывает часто затруднительно и часто даже невозможно из-за
разной растворимости соединений в одном и том же растворителе.
На
практике различные ингибиторы добавляют на разных стадиях производства
полимеров, что усложняет введение их в массу. Не исключено также химическое
взаимодействие отдельных компонентов между собой, в результате чего могут
образоваться неактивные продукты. В этих случаях подбирают вещества, не
реагирующие друг с другом, что ограничивает выбор ингибиторов, пригодных для
приготовления синергетических смесей.
Еще
один недостаток синергетических смесей связан с непостоянством их действия во
времени. Каждый компонент смеси имеет только для него характерные
физико-химические свойства, поэтому изменение концентрации какого-либо одного
компонента будет оказывать влияние на эффективность действия всей смеси.
Для
получения наибольшего синергетического эффекта необходимо применять смеси с
оптимальными количествами ингредиентов, что требует сложных и трудоемких
предварительных исследований.
Данная
проблема решается путем использования полифункциональных антиоксидантов -
соединений, содержащих в структуре молекулы несколько реакционных групп,
способных ингибировать отдельные элементарные акты цепной реакции окисления
[46].
Среди
полифункциональных АО большой интерес представляют серосодержащие производные
пространственно-затрудненных фенолов, отличительной чертой которых является их
высокая антиоксидантная активность. Показано, что серосодержащие фенолы
превосходят по эффективности свои кислород- и азотсодержащие аналоги [47], а
также композиции на основе ионола и алкилсульфида [48,49]. К несомненным
достоинствам этих соединений следует отнести также их малую токсичность,
доступность исходного сырья, а также возможность получения на их основе
неокрашенных композиций [1,4,35].
окисление тиоалкилфенол гидрохинон
Глава 2. Материалы, объекты и методы исследования
.1 Объекты исследования
Объектами настоящего исследования были выбраны бензильные сульфиды на
основе алкилированных производных гидрохинона (1-16); группа монофункциональных
соединений (17-27), близких по структурам к соответствующим сульфидам. В
качестве реперных антиоксидантов использовались α-токоферол (ТФ) и
2-трет-бутил-4-метоксифенол (БОА) бензильные сульфиды на основе гидрохинона

(1)
(2) (3) (4)

(5)
(6) (7) (8)

(9)
(10) (11) (12)

(13)
(14) (15) (16)
гдеR=SC12H25 производные гидрохинона

(17)
(18) (19) (20) (21)

(22)
(23) (24)

(25)
(26) (27)
.2
Методика окисления свиного жира
В
качестве субстрата окисления использовали свиной подкожный жир, закупленный на
Центральном рынке г. Новосибирска и переработанный на кафедре химии НГПУ.
Вытопку жира проводили на водяной бане при контакте с воздухом и температуре не
выше 1000С. Вытопленный жир отфильтровывали для освобождения от
остатков тканей, тщательно перемешивали во избежание неоднородности субстрата и
замораживали в морозильной камере при -180С. В этих же условиях
осуществляли дальнейшее хранение сырья.
Окисление
свиного жира с использованием окислительной ячейки
В
пробе жира массой 50 г растворяли навеску антиоксиданта, массу которой
рассчитывали по формуле:
m = 
CPhOH - молярная
концентрация; М - молярная масса антиоксиданта

Рис.
1 термостатируемая окислительная ячейка: 1 - трубка для подачи кислорода; 2 -
стеклянный фильтр №2; 3 - термометр; 4 - обратный холодильник; 5 - проба жира; 6
- термостатирующая жидкость
и
взвешивали на аналитических весах. Смесь нагревали на водяной бане, хорошо
перемешивали и переносили в окислительную ячейку. Отсчет времени начинали через
5 минут после загрузки пробы жира в окислительную ячейку. Этого времени
достаточно, чтобы жир нагрелся до 1330С.
В
качестве окислителя использовали кислород, что имеет определенные преимущества
перед окислением в токе воздуха. В этом случае намного легче создать условия,
когда процесс окисления протекает в кинетической области.
Кислород
подавали по трубке через впаянный в нижнюю часть окислительной ячейки
стеклянный фильтр. При прохождении через такой фильтр струя подаваемого
кислорода разбивалась, благодаря чему он проходил равномерно через слой
расплавленного жира в виде мелких пузырьков. Скорость подачи кислорода
составляла 1 л в минуту.
Термостатирование
окислительной ячейки осуществляли за счет кипения термостатирующей жидкости, в
качестве которой использовали хлорбензол (tкип=133,50С). При таком способе
термостатирования изменять температуру можно простой заменой растворителя, что
делает возможным проводить окисление без использования термостата. Кроме того,
за счет постоянства температуры кипения растворителя, окисление можно проводить
в совершенно одинаковых условиях.
Ход
окисления контролировали по накоплению перекисных соединений в субстрате. Перед
началом окисления и через определенные промежутки времени в ходе окисления
отбирали пробы жира (~1,00 г) и определяли в них перекисные числа
йодометрическим методом. Процесс завершался при полном прогоркании жира. Об
этом свидетельствовали высокие значения перекисных чисел и органолептические
показатели - неприятный запах и вспенивание жира.
На
основании полученных данных строили кинетические кривые зависимости перекисного
числа от времени и определяли период индукции (рис.2). За период индукции
принимали время, в течение которого жир окислялся до перекисного числа 0,1
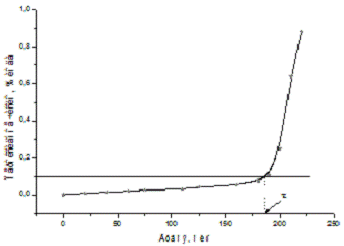
Рис.
2 Определение периода индукции как времени достижения перекисного числа 0.1 при
окислении лярда
2.3
Методика определения перекисного числа в жирах
Точную
навеску жира (1г) растворяли в 10 мл смеси ледяной уксусной кислоты и
хлороформа в соотношении 1:1 (по объему). Затем прибавляли 2 мл 20%-ного
водного раствора йодида калия. Далее по секундомеру выдерживали 1 минуту в
темноте. Перед титрованием в каждую колбу добавляли 10 мл дистиллированной
воды, 5 капель раствора крахмала и выделившийся йод при тщательном
перемешивании титровали 0,01 н раствором тиосульфата натрия до исчезновения
синей окраски.
Аналогичным
образом ставили «слепую» пробу на реактивы.
Вычисление
перекисного числа проводили по формуле:
П.ч.
= CN·(V1-V2)·0,1269·100%
CN -
нормальная концентрация раствора тиосульфата натрия;
V1 - объем раствора тиосульфата натрия в миллилитрах,
который идет на титрование йода, выделившегося из навески жира;
V2 - объем раствора тиосульфата натрия в миллилитрах,
который идет на титрование йода, выделившегося в «холостом» опыте;
П.ч.
- перекисное число, выраженное в процентах йода.
Например,
на титрование йода, выделившегося в пробе, пошло 1,15 мл, а в «слепой» пробе 0
мл 0,01 н раствора тиосульфата натрия. Следовательно, перекисное число будет
равно:
Данная
запись означает, что масса выделившегося йода составляет 0,15% по отношению к
массе жира.
m(йода) =  г
г
г
- 100%
,46·10-3
- х%
х
= 
.4
Приготовление титрованных растворов
Приготовление
раствора бихромата калия
В
качестве стандартного раствора использовали 0,01 н раствор бихромата калия. Для
приготовления данного раствора, на аналитических весах брали точную навеску K2Cr2O7, которую рассчитывали следующим образом:
Э(K2Cr2O7) = М/6 = 49,01 г/экв.
,01
экв. содержится в 1000 мл
х
экв. содержится в 250 мл.
х =  (K2Cr2O7)
= n экв. · Э = 0,0025
экв. · 49,03 г/экв. = 0,1225 г.
(K2Cr2O7)
= n экв. · Э = 0,0025
экв. · 49,03 г/экв. = 0,1225 г.
Навеску
K2Cr2O7,
количественно переносили в мерную колбу емкостью 250 мл, растворяли в воде,
разбавляли раствор до метки и тщательно перемешивали.
Приготовление
раствора тиосульфата натрия
В
качестве рабочего раствора использовался 0,01 н раствор Na2S2O3.
Для
приготовления раствора на технических весах брали навеску Na2S2O3, которую рассчитывали следующим образом:
М(Na2S2O3 · 5 Н2О) = Э = 248,19 г/экв.
,01
экв. содержится в 1000 мл
х
экв. содержится в 500 мл.
х = 
m(Na2S2O3 · 5 Н2О) =
n экв. · Э = 0,005
экв. · 248,19 г/экв. = 1,24095 г.
Навеску
тиосульфата натрия около 1,24-1,25 г переносили в мерную колбу вместимостью 500
мл и растворяли в дистиллированной воде. Раствор выдерживали несколько дней в
темной склянке.
Стандартизация
раствора тиосульфата натрия
Раствором
тиосульфата натрия наполняли бюретку на 5 мл и устанавливали уровень жидкости в
ней на нуле. В коническую колбу переносили 1 мл 20%-ного раствора KI и
2 мл 2 н раствора H2SO4. К
полученной смеси прибавляли 2 мл раствора K2Cr2O7. Смесь ставили в темноту на 5 минут. Затем в колбу
прибавляли 10 мл воды и титровали без добавления крахмала до обесцвечивания
раствора.
Пользуясь
формулой, вычисляли искомую нормальность раствора тиосульфата натрия:
V(K2Cr2O7) · Сн(K2Cr2O7) = V(Na2S2O3)
· Cн(Na2S2O3);
Cн(Na2S2O3) =  .
.
Глава
3 Исследование антиоксидантной активности производных гидрохинона на модели
термического автоокисления свиного жира
В
наши дни антиоксиданты и антиоксидантные композиции являются одним из наиболее
востребованных типов добавок в отраслях промышленности, тем или иным образом
связанных с получением, хранением и обработкой жиров, масел и жирсодержащих
материалов. Объектом особого внимания в последние годы являются синтетические и
природные антиоксиданты, перспективные с точки зрения их возможного
использования в медицине и косметике. К такого рода антиоксидантам и
антиоксидантным композициям предъявляется ряд особых требований, наиболее
значимыми из которых являются: растворимость в липидных субстратах; малая токсичность;
высокая ингибирующая эффективность в отношении торможения процессов перекисного
окисления липидов.
Несколько
лет назад в Новосибирском институте химии антиоксидантов был получен ряд
высокоэффективных полифункциональных антиоксидантов на основе гидрохинона и его
монометилового эфира, которые полностью удовлетворяют этим требованиям. Эти
вещества хорошо растворимы в растительных и животных жирах и по ингибирующей
способности превосходят подавляющее большинство известных к настоящему времени
серосодержащих фенольных антиоксидантов. Для наиболее эффективных
антиоксидантов данного типа была установлена низкая токсичность. При этом,
среди исследованных ранее сульфидов особо выделяется группа производных
2,6-диметилгидрохинона, которые по значениям периодов индукции уступают не
только своим неметилированным аналогам, но и реперным антиоксидантам - ионолу и
витамину Е. Для дальнейшего целенаправленного синтеза высокоэффективных
антиоксидантов на основе двухатомных фенолов мы считаем необходимым проведение
углубленного исследования по выявлению взаимосвязи между типом и положением
алкильных заместителей в ароматическом кольце и брутто-ингибирующей активностью
серосодержащих производных гидрохинона. Полученные данные могут быть интересны
не только в прикладном аспекте, но и с точки зрения расширения существующих
представлений о механизме действия фенольных антиоксидантов.
В
настоящей дипломной работе проведено исследование антиоксидантной активности
ряда структурно взаимосвязанных тиоалкилфенолов, а также их предшественников,
не содержащих серы, на модельной реакции термического автоокисления свиного
жира.
Окисление
проводили с использованием термостатируемой окислительной ячейки при 133°С в
условиях барботажа кислородом. Концентрация исследуемых соединений составляла
1.5 мкмоль/г. Об ингибирующей эффективности антиоксидантов судили по величине
периода индукции τ,
который определяли как время достижения
субстратом перекисного числа 0.1.
Результаты
представлены в таблицах 1-3 и диаграммах на рис. 3-4.
Полученные
экспериментальные данные свидетельствуют о том, что все исследованные нами
серосодержащие производные гидрохинона обладают выраженной противоокислительной
активностью. Однако, наблюдаются существенные различия в значениях периодов
индукции соединений, имеющих и не имеющих алкильные заместители в ароматическом
кольце. Анализ данных таблицы 1 показывает, что по ингибирующей эффективности
производные алкил- и диалкил-гидрохинона значительно уступают своим
неалкилированным аналогам. Исключение составляет сульфид (6) на основе
3,5-диметил-4-метоксифенола, который по величине τ не отличается от своего гомолога (5). Найденная
закономерность не согласуется с результатами, полученными ранее при
исследовании АОА сульфидов, являющихся производными фенолов с разной степенью
пространственного экранирования фенольной OH-группы.
Согласно многочисленным литературным данным, а также результатам исследований,
Таблица
1. Периоды индукции окисления свиного жира, ингибированного тиоалкилфенолами, [Ar(OH)2]
= 1.5 мкмоль/г*
|
антиоксидант
|
шифр
|
период индукции, мин
|
антиоксидант
|
шифр
|
период индукции, мин
|
|

|
1
|
788±28
|

|
10
|
142±3
|
|
 2797±23 2797±23 11310±15 11310±15
|
|
|
|
|
|
|
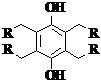
|
3
|
585±5
|

|
12
|
76±6
|
|
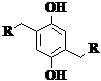
|
4
|
820±30
|

|
13
|
105±5
|
|
 5668±8 5668±8 1487±7 1487±7
|
|
|
|
|
|
|
 6685±5 6685±5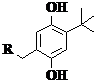 15304±15 15304±15
|
|
|
|
|
|
|

|
7
|
84±8
|

|
16
|
252±13
|
|

|
8
|
α-токоферол
|
ТФ
|
122±3
|
|

|
9
|
170±5
|
контроль
|
|
15
|
|
2-трет-бутил-4-метоксифенол
|
БОА
|
170±5
|
•*ПЧисх. = 0,0068 % I2
|
проводимых в течение последних лет в НИИ Химии Антиоксидантов, брутто-
ингибирующая эффективность серосодержащих фенольных антиоксидантов повышается
при введении алкильных заместителей в орто- и пара- положения по отношению к
гидроксильной группе. При этом, максимальная эффективность достигается в этом
случае, когда строение заместителей таково, что они, они с одной стороны,
способны надежно стабилизировать феноксильный радикал, предотвращая его участие
в реакции (10) и, с другой, не создают значительных трудностей для участия PhOH в реакции (7)

Согласно
данным диаграммы на рис. 3 оптимальным типом орто-замещения в ряду сульфидов на
основе фенола является метил-циклогексильный, метил-изопропильный и
диизопропильный. Также известно, что введение любой алкильной группы в
орто-положение приводит к повышению значений периодов индукции по сравнению с
неэкранированным -гидроксибензилдодецилсульфидом.
Как
было сказано ранее, в ряду серосодержащих производных гидрохинона проявляется
противоположная тенденция. Введение любого типа алкильных заместителей в
ароматическое кольцо не только не способствует повышению ингибирующей
эффективности, но и приводит к снижению показателей в 2-10 раз.
Сравнение
значений периодов индукции моно- и диалкилзамещенных производных гидрохинона
показывает, что последние значительно менее активны в качестве стабилизаторов
свиного жира. Особо выделяется группа соединений на основе
2,6-диалкилгидрохинона. Вне зависимости от типа орто-заместителей и количества
серосодержащих групп, сульфиды (7),(8),(12) и (14) характеризуются одинаковыми
значениями τ
порядка 80 мин.

Рис.
3. Периоды индукции окисления свиного жира в присутствии тиоалкилфенолов с
различным орто-замещением
Нами
было проведено исследование по выявлению взаимосвязи между расположением
алкильных заместителей в молекулах серосодержащих производных
диалкилгидрохинона и проявляемой ими АОА. Результаты иллюстрирует диаграмма на
рис.4. Согласно полученным данным, среди всех исследованных соединений наименее
эффективны были те антиоксиданты, в молекулах которых заместители находились в
положениях 2 и 6. Данная закономерность проявляется как в ряду производных 2, 6
- диметилгидрохинона, так и у соединений с метил- изопропильным типом
замещения. Наибольшим значением периода индукции в данной группе
характеризуется сульфид (9) на основе 2,5-диметилгидрохинона. Однако его
превосходство над изомером (10) невелико и может быть объяснено большей
симметричностью структуры, что, вероятно позволяет сульфиду (9) легче
«встраиваться» между молекулами субстрата.

Рис.
4. Периоды индукции окисления свиного жира, ингибированного бензильными
сульфидами на основе гидрохинона с различным расположением алкильных
заместителей в ароматическом кольце
Нами
была дана оценка ингибирующей эффективности фенольных прототипов соединений
(1)- (16) в тех же модельных условиях, при концентрации [Ar(OH)2]=1.5
мкмоль/г. Сведения об АОА алкил- диалкил-производных гидрохинона были
необходимы нам по двум причинам. Во-первых, анализ литературных источников
показал, что до настоящего времени системные исследования, посвященные этой
проблеме, не проводились. Во-вторых, если существует корреляция между
значениями периодов индукции производных моно- и диалкилгидрохинона и сульфидов
на их основе, то эту взаимосвязь можно использовать для предсказания
эффективности других соединений этого ряда.
Полученные
результаты приведены в таблице 2.
К
сожалению, нам не удалось установить точное значение периода индукции для
гидрохинона (17). В условиях эксперимента (температура 133ºС) он возгонялся, поэтому его концентрация в субстрате
постоянно уменьшалась. Указанная величина (250 минут) является ориентировочной,
в то время как истинное значение τ, вероятно, должно быть несколько выше. Тем не менее, анализ полученных
данных позволяет сделать однозначный вывод о том, что по сравнению с другими
исследованными соединениями (17) - (27) гидрохинон характеризуется очень
высокими показателями АОА и уступает только БОА; это хорошо согласуется с
результатами, полученными ранее для сульфидов.
Данные
таблицы 2 свидетельствуют о том, что введение одной алкильной группы в молекулу
гидрохинона приводит к меньшему, чем в случае двух заместителей, снижению
антиоксидантной активности.
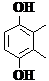
Таблица
2. Периоды индукции окисления свиного жира в присутствии алкилированных
производными гидрохинона, [Ar(OH)2] = 1.5 мкмоль/г *
|
антиоксидант
|
шифр
|
период индукции, мин
|
антиоксидант
|
шифр
|
период индукции, мин
|
|

|
17
|
250±30**
|

|
23
|
52±2
|
|

|
18
|
118±9
|

|
24
|
35±3
|
|

|
19
|
52±1
|

|
25
|
128±3
|
|

|
20
|
38±2
|

|
26
|
52±3
|
|
|
21
|
35±1
|

|
27
|
35±3
|
|

|
22
|
54±6
|

|
БОА
|
275±10
|
* ПЧ исх. = 0,00518% I2 ** возгоняется в условиях
эксперимента
Таким образом, для всех исследованных алкилированных производных
гидрохинона, а также бензильных сульфидов на их основе характерны следующие
общие закономерности:
ü Введение любого рода алкильных заместителей в молекулу
гидрохинона или его бензильного сульфида приводит к резкому снижению АОА;
ü Диалкилзамещенные соединения по значениям периодов индукции
окисления свиного жира существенно уступают моноалкилированным;
ü Среди исследованных бензильных сульфидов наименее
эффективными в качестве ингибиторов окисления свиного жира являются производные
2,6- диалкилгидрохинона. У монофункциональных антиоксидантов самые низкие
значения периодов индукции были зафиксированы в группе 2,5 и 2,3- замещенных
гидрохинонов.
Среди исследованных нами антиоксидантов присутствовали также некоторые
соединения на основе метилового эфира гидрохинона: 2-трет-бутил-4-метоксифенол,
а также сульфиды (5) и (6). Анализ полученных значений периодов индукции
(таблица 3) позволяет нам сделать вывод о том, что описанные ранее
закономерности влияния числа и положения алкильных заместителей на
антиоксидантную активность производных гидрохинона, по всей видимости, не
распространяются на его метиловые эфиры. Так, БОА, имеющий в составе молекулы
трет-бутильный заместитель, не уступает по ингибирующей эффективности
гидрохинону, а присутствие двух метильных групп совершенно не влияет на
активность сульфида (6). Возможно, причина столь существенных различий
заключается в том, что у производных 4-метоксифенола, в отличие от гидрохинона,
механизм, посредством которого проявляется их антиоксидантная активность,
принципиально иной.
Таблица 3. Периоды индукции окисления свиного жира в присутствии
производных гидрохинона и его метилового эфира, [Ar(OH)2] =
1.5 мкмоль/г
|
антиоксидант
|
шифр
|
период индукции, мин
|
|
 2797±23* 2797±23*
|
|
|
|
 5668±8* 5668±8*
|
|
|
|
 6685±5* 6685±5*
|
|
|
|

|
17
|
250±30**
|
|

|
25
|
128±3**
|
|

|
БОА
|
275±10**
|
* ПЧисх. = 0,0068 % I2
*** ПЧ исх. = 0,00518% I2
Выводы
На модели термического автоокисления свиного жира была исследована
антиоксидантная активность ряда тиоаклилфенолов и алкилпроизводных гидрохинона.
Показано, что наиболее эффективными ингибиторами окисления являются бензильные
сульфиды на основе гидрохинона: додецилтиометилгидрохинон ,
2,5-бис(додецилтиометил)гидрохинон и его изомер. Среди монофунцкциональных
антиоксидантов-производных гидрохинона наибольшие значения периодов индукции
были получены для гидрохинона и 2-трет-бутил-4-метоксифенола (БОА).
Введение алкильных заместителей любого типа в молекулу гидрохинона или
его бензильного сульфида приводит к резкому снижению АОА. При этом
диалкилзамещенные соединения по значениям периодов индукции окисления свиного
жира существенно уступают моноалкилированным.
Среди исследованных бензильных сульфидов наименее эффективными в качестве
ингибиторов окисления свиного жира являются производные 2,6-
диалкилгидрохинона. У монофункциональных антиоксидантов самые низкие значения
периодов индукции были зафиксированы в группе 2,5 и 2,3- замещенных производных
гидрохинона.
Показано, что найденные закономерности влияния количества и положения
алкильных заместителей на антиоксидантную активность производных гидрохинона не
распространяются на его метиловые эфиры.
Литература
. Горбунов Б.Н., Гурвич Я.А., Маслова И.П. Химия и технология
стабилизаторов полимерных материалов. - М.: Химия, 1981.
. Эмануэль Н.М., Денисов Е.Т., Майзус З.К. Цепные реакции
окисления углеводородов в жидкой фазе. - М.: Наука, 1965.
. Эммануэль Н.М., Лясковская Ю.Н. Торможение процессов
окисления жиров. - М.: Пищепромиздат, 1961.
. Фойгт И. Стабильность синтетических полимеров против
действия тепла и света. - М.: Химия,1972.
. Ершов В.В., Никифоров Г.А., Володькин А.А.
Пространственно-затрудненные фенолы. - М.: Химия,1971.
. Рогинский В.А. Фенольные антиоксиданты. Реакционная
способность и эффективность. - М.: Наука,1988.
. Шляпников Ю.А., Кирюшкин С.Г., Марьин А.П.,
Антиокислительная стабилизация полимеров. - М.: Химия,1986.
. Денисов Е.Т., Ковалев Г.И., Окисление и стабилизация
реактивных топлив. - М.: химия,1983.
. Грасси Н., Скот Дж. Деструкция и стабилизация полимеров. -
М.: Мир,1988.
. Уолтерс У. Механизм окисления органических соединений. -
М.: Наука, 1966.
. Нонхибел Д., Уолтон Дж. Химия свободных радикалов. - М.:
Мир, 1977.
. Журавлев А.И. Антиокислители.- В кн.: БМЭ. 3-изд,1975.
Т.2.- С.33-35.
. Эммануэль Н.М., Бучаченко А.Л. Химическая физика старения и
стабилизация полимеров.- М.: Наука, 1982.
. Роль фенольных антиоксидантов в повышении устойчивости
органических систем к свободно-радикальному окислению: Аналитический обзор /
И.В.Сорокина, А.П.Крысин, Т.Б.Хлебникова, В.С.Кобрин, Л.Н.Попова; СО РАН;
ГПНТБ, НИОХ.- Новосибирск, 1997. (Сер. «Экология». Вып. 46).
. Евстигнеева Р.П., Волков И.М., Чудинова В.В. //
Биологические мембраны.-1998. Т.15. № 2. С.119-135.
. Биохимия окислительного стресса. Оксиданты и антиоксиданты
/ Е.Б.Меньщикова, Н.К. Зенков, С.М.Шергин. - Новосибирск, 1994.
. Свободно-радикальные процессы в биологических системах. -
М.: Наука,1966.
18. Scott G. Atmospherik oxidation and antioxidants. -
Amsterdam: Elsevier, 1965.
. Pospisil I. Antioxidants. - Pradus, 1968.
. Бурлакова Е.Б., Алесенко А.В., Молочкина Е.М. и др. Биоантиоксиданты в лучевом поражении
и злокачественном росте. - М.: Наука, 1975.
21. Патент Великобритании. 2031422. Preparation of
2,2¢-bis(4-substitutedphenol)sulfides
/ Yamaquchi A., Kobayashi T., Yamaqushi K. // C.A. 1981. V.94. №1. 1Ю83765Ю.
. Клиев А.М., Мамедов Ф.Н. Производные фенолов и тиолов. -
Баку: ЭЛМ,1981.
. 3,5-Диалкил-4-гидроксибензилтиопроизводные. // Патент №
911,958 Англия. 1961.
24. Фенольные стабилизаторы. Обзорная информация. - М.:
ЦНИИТЭНЕФТЕХИМ. 1990. № 5.
25. Рачинский Ф.Ю., Большаков
Г.Ф., Брук Ю.А. Влияние некоторых производных ионола на термоокислительную
стабильность сернистых реактивных топлив / Химия сероорганических соединений,
содержащихся в нефти и нефтепродуктах. -- М.: Химия, 1968. Т. 8. - C. 654-659.
26. Kolawole E.G., Scott G. Stabilization of ABS with
bound synergistic stabilizers added as masterbatches. // J. Appl. Polym.
Science. - 1981. - V. 26. - P. 2581-2592.
. Scott G., Tavakoli S. M. Mechanisms of antioxidant
action: Formation of antioxidant adducts with rubbers through sulphur by a
mechanochemical procedure. // Polym. Degrad. and Stab. - 1982. - N 4. - P.
343-351.
. Fernando W. S.E., Scott G. Mechanisms of antioxidant
action: autosynergistic polymer-bound antioxidants as heat and light
stabilizers for ABS / Eur. Polim. J. - 1980. - V. 16. - P. 971-978.
. Просенко А.Е. w-(4-Гидроксиарил)галогеналканы и серосодержащие антиоксиданты
на их основе.- Автореф. … канд. хим. наук. - Новосибирск,2000.
. Михайлец И.Б., Максимова Н.С., Слюсарева И.П., Евсюков В.И.
Гигиенические свойства стабилизатора Фенозан 30. // Химическая промышленность.
- Сер. Токсикология, санитарная химия пластмасс. - 1979. - № 4. - С. 36-38.
. Химикаты для полимерных материалов. / Под ред. Б.Н.
Горбунова. - М.: Химия, 1984
. Антиоксиданты. // Патент № 4,165,333 США. 1979.
. Лугова Л.И., Макарова Г.П., Сотникова Л.К. и др.
3,5-Ди-трет-бутил-4-оксифенил-алкилтиоэфир карбоновой кислоты в качестве
термостабилизатора полиэтилена и композиция на основе полиэтилена. // Авторское
свидетельство № 1131869 СССР. 1984.
. Кириллова Э.И., Лугова Л.И., Коптюг В.А. и др. Полимерная
композиция. // Авторское свидетельство № 1118654 СССР. 1984.
. Гурвич Я.А., Золотаревская Л.К., Кумок С.Т. Фенольные
стабилизаторы. - М.: ЦНИИТЭНЕФТЕХИМ, 1978.
. Химические добавки к полимерам (справочник) / Под ред. И.Г.
Масловой. - М.: Химия, 1981.
. 2,6-Ди-трет-бутилфенол в органическом синтезе
стабилизаторов для полимеров. Хим. промышленность. Сер. Химикаты для полимерных
материалов. Обзорная информация. - М.: НИИТЭХИМ. №1. 1987.
. Хинькис С. С., Матвеева Е.Н. и др. Слабо-окрашивающие
стабилизаторы полиолефинов // Пластмассы. - 1968. - № 11. - C. 7-8.
. Тиаалкильные замещенные фенолы и их производные в
стабилизации органических материалов. // Патент № 1396469 Англия. 1977.
. Кулиев А.М. Химия и технология присадок к маслам и
топливам. - М.: Химия, 1972.
. Кириллова Э.И., Лугова Л.И., Крысин А.П. и др. Полимерная
композиция. // Авторское свидетельство № 1464444 СССР. 1988.
. Демидова В.М., Лугова Л.И., Просенко А.Е. и др. Полимерная
композиция. // Авторское свидетельство № 979428 СССР. 1982.
44.
Просенко А.Е., Терах Е.И., Кандалинцева Н.В. и др. Синтез и исследование
антиокислительной свойств новых серосодержащих производных
пространственно-затрудненных фенолов. // Журнал прикл. химии. - 2001. - Т. 74.
- № 11. - С. 1839-1843.
.
Карпухин Г.В., Эмануэль Н.М. Классификация синергетических смесей
антиоксидантов и механизмов синергизма. // Докл. АН СССР. 1984. Т. 276. № 5. С.
1163-1167.
46. Ингибирование процессов окисления полимеров смесями
стабилизаторов. - М.: НИИТЭХИМ, 1970.
48. Farsaliev V.M., Fernando W.S., Scott G. Mechanisms
of antioxidant action: autosynergistic behaviour of sulphyr-containing phenols.
// Eur. Polym. J. - 1978. - V. 14. - № 10. - P. 785-788.
. Scott G., Tusoff M. Mechanisms of antioxidant
action: autosynergistic antioxidants containing chain- breakihg and
preroxydolytik funetions. // Eur. Polym. J. - 1980. - V. 16. - № 6. - P.
497-501.