Синтез оксалат уранила с пиридинкарбоновыми кислотами
МИНИСТЕРСТВО
ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
ГОСУДАРСТВЕННОЕ
ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ВЫСШЕГО
ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«САМАРСКИЙ
ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ»
Химический
факультет
Кафедра
неорганической химии
Специализация
неорганическая химия
Синтез
оксалат уранила с пиридинкарбоновыми кислотами
Курсовая
работа
Выполнил
студент
курса,
04301.10 группы
Сафин
М.Р.
Научный
руководитель
д.х.н.,
профессор
Сережкин
В.Н.
Зав.
кафедрой
д.х.н.,
профессор
Сережкин
В.Н.
Самара 2013
Содержание
1. Введение
. Обзор литературы
.1 Оксалат уранила - синтез,
строение и свойства
.2 Комплексные соединения уранила с
никотиновой кислотой
. Экспериментальная часть
.1 Методы исследования
.2 Характеристика исходных веществ
.3 Изучение комплексообразования в
системе оксалат уранила с никотиновой кислотой
. Выводы
. Списки используемых источников
. Введение
Ураниловые соединения - весьма распространенный
класс практически важных веществ. Многие из них могут быть успехом применены в
народном хозяйстве: как реагенты в процессах обогащения ядерного горючего
(урановых руд), полупроводники, пьезоэлектрики, полимерные материалы с
определенными электрическими, термическими и другими характеристиками [1, 2].
Известно большое количество оксалатсодержащих
соединений актинидов. Оксалаты актинидов используют для производства металлов,
для получения соединений, которые применяются в ядерной и химической
технологиях. Следовательно, можно считать актуальными знания о составе и
строении новых оксалатсодержащих соединений урана (VI)
с пиридинкарбоновыми кислотами [3].
Целью данной работы явились синтез и изучение
комплексных соединений полученных взаимодействием тригидрооксалат уранила с
пиридинкарбоновыми кислотами (никотиновая, изоникотиновая, пиколиновая) в связи
с чем были поставлены следующие задачи:
) синтез комплекса оксалат уранила с
пиридинкарбоновыми кислотами;
) определение структуры полученных
соединений;
) исследование термической устойчивости
комплексов методом дифференциального термического анализа;
) изучение спектров поглощения соединений
в ИК диапазоне;
. Обзор литературы
.1 Оксалат уранила - синтез, строение и свойства
Оксалат уранила UO2C2O4
·3H2O
существует в виде тригидрата и является устойчивым на воздухе. Для его синтеза
к нагретому до 80-90оС концентрированному раствору нитрата уранила
приливают горячий насыщенный раствор щавелевой кислоты и перемешивают до тех
пор, пока образовавшийся гель не закристаллизуется в тяжелый осадок.
Максимальный выход соединения достигается при избытке 2% по массе Н2С2О4
против стехиометрии, однако для получения крупнокристаллического осадка следует
брать несколько больший избыток Н2С2О4.
Раствор с осадком охлаждают, осадок отфильтровывают и промывают на фильтре
холодной водой, затем 2-4 раза спиртом и эфиром [4].
Тригидрат оксалата уранила - исходный продукт
для получения большинства оксалатокомплексов уранила; он образует моноклинные
кристаллы в виде прямоугольных или ромбических пластинок {010}, удлиненных в
направлении {001}, с углом при вершине, равным 51°. Оптически двуосный,
положительный, 2V=31° [6].
Авторы [7,8] провели рентгеноструктурное исследование U02C204-3H20.
Пространственная группа Р21/с. Параметры моноклинной элементарной
ячейки: а = 5.62А, b = 17.07А, с
= 9.45, β=
98.74°. Плотность,
вычисленная из рентгенографических данных, равна 3.07 г/см3 [7]. По
полученным данным [8] расстояния U=0
в уранильной группе равны 1.74(3) и 1.75(3)
Å.
В структуре UO2C2O4
·3H2O
в экваториальной плоскости ионов уранила расположены четыре атома кислорода
двух тетрадентатных оксалато-групп (тип координации К02) и атом
кислорода молекулы воды (М1). Основной структурной единицей
кристаллов являются бесконечные зигзагообразные цепи состава [U02(C2О4)(H2О)],
относящиеся кристаллохимической (КХ) группе АК02М1 (А = UО22+
) комплексов уранила, между ними размещаются внешнесферные молекулы воды,
которые вместе с координированными ураном молекулами воды участвуют в
образовании системы водородных связей.
В твердом состоянии оксалат уранила к
дегидратации на воздухе устойчив. При нагревании удаление воды происходит
ступенчато и осуществляется в три стадии, каждая из которых отвечает удалению
одной из «молекул воды [5]. Эндотермические эффекты при 95 - 100°С связаны с
потерей двух молекул воды, а при 180°С - с потерей третьей молекулы воды, которая
входит в координационную сферу U
(VI). Первые две молекулы воды отщепляются в вакууме уже при комнатной
температуре. В процессе дегидратации не происходит существенного изменения
параметров кристаллической решетки, практически не изменяются значения удельной
плотности продуктов. Выше 280°С UО2C2О4
разлагается. Конечный продукт этого процесса в среде инертного газа или в
вакууме UО2, как
правило, стехиометрического состава. Процесс разложения безводного оксалата
уранила протекает в две стадии в узком температурном интервале. Среди большого
числа соединений U (VI)
оксалат уранила - одно из немногих соединений, в результате термического
разложения которых в инертной атмосфере непосредственно образуется UО2.
При проведении процесса на воздухе в интервале 290 - 380°С твердый продукт
представляет собой UO3,
переходящий при более высокой температуре в U3O8.
Процесс термораспада UO2C2O4
можно представить следующей схемой:
UО2C2О4
→ UO2
→ UO3
→ 1/3U3O8
Растворимость оксалата уранила в
воде, 95% - ном этиловом и безводном метиловом спирте мала. С увеличением
температуры -растворимость в воде увеличивается, достигая максимальной величины
в 3,06 мас. % по безводной соли при 100°С (табл. 1) [5].
оксалата уранила в
воде, 95% - ном этиловом и безводном метиловом спирте мала. С увеличением
температуры -растворимость в воде увеличивается, достигая максимальной величины
в 3,06 мас. % по безводной соли при 100°С (табл. 1) [5].
Таблица 1. Растворимость оксалата
уранила в воде
|
Температура,
оС
|
Растворимость
UО2C2О4,
масс. %
|
|
11
|
0.45
|
|
15
|
0.47
|
|
20
|
0.50
|
|
50
|
1.00
|
|
75
|
1.63
|
|
100
|
3.06
|
оксалат уранил никотиновый кислота
Растворимость тригидрата оксалата уранила
повышается также в присутствии минеральных кислот, щавелевой кислоты и
оксалатов щелочных металлов.
В водном растворе UО2C2О4
обнаруживает весьма незначительную электропроводность, константа
диссоциации составляет (1.7±0.3) ·10-7.
.2 Комплексные соединения уранила с никотиновой
кислотой
В литературе описаны три комплекса урана (VI) с
никотиновой кислотой [UО2SO4(C6H5NO2)2(H2О)]·H2О
(I) [9], [UO2(NO3)2(C6H5NO2)2]
(II) [10], [UO2(C6H4NO2)2(H2O)2]
(III) [11].
Координационным полиэдром атома урана в структуре I является пентагональная
бипирамида UO2O5,
на главной оси которой находятся атомы кислорода иона уранила, а в
экваториальной плоскости располагаются два атома кислорода двух сульфат-ионов,
два - молекул никотиновой кислоты и один - внутрисферной молекулы воды.
Координационные полиэдры атомов серы - тетраэдры SO4.
Сульфат- ионы играют по отношению к атомам урана роль бидентатно-мостиковых
лигандов (тип координации В2 [12] и располагаются в цис-положении по
отношению друг к другу (рис. 1).

рис. 1 Фрагмент кристаллической структуры
комплекса сульфата уранила с никотиновой кислотой
Молекулы никотиновой кислоты, находящиеся в
транс-положении по отношению друг к другу, и молекула воды играют роль
монодентатных концевых лигандов (тип М1). Согласно полученным
данным, основной структурной единицей кристалла I являются димеры состава [UО2SО4(C6H5NО2)2H2О],
относящиеся к кристаллохимической группе AB2M13
комплексов уранила. Разветвленная система водородных связей объединяет
электронейтральные димеры в трехмерный каркас, в пустотах которого находятся
внешнесферные молекулы воды.
В структуре II координационным полиэдром атома
урана является центросимметричная гексагональная бипирамида UО2О6,
на главной оси, которой находятся атомы кислорода иона уранила, а в
экваториальной плоскости располагаются четыре атома кислорода двух нитратогрупп
и два - двух молекул никотиновой кислоты. Нитрат-ионы, расположенные в
транс-положении относительно друг друга, играют по отношению к ионам уранила
роль бидентатно-циклических лигандов (тип координации В01 [12]).
Молекулы никотиновой кислоты являются концевыми лигандами, тин координации М1,
и также расположены в транс-положении относительно друг друга. Согласно
полученным данным, основной структурной единицей кристалла II являются
одноядерные центросимметричные группировки состава [UО2(NО3)2(C6H5NО2)2]
(рис. 2), относящиеся к кристаллохимической группе АВ012М12
комплексов уранила. За счет образования водородных связей между гидроксильной
группой молекулы никотиновой кислоты одного комплекса и атомом азота пиридиновой
группировки кислоты другого комплексные группировки выстраиваются в цепочки
вдоль трансляции b.

Основными структурными единицами кристаллов III
являются одноядерные центросимметричные группировки, совпадающие с составом
соединения [UО2(C6H5NО2)2(H2О)2]
. Кристаллохимическая формула комплекса АВ012 М12.
Координационным полиэдром атома урана является
центросимметричная гексагональная бипирамида UО2О6,
на главной оси, которой находятся атомы кислорода иона уранила, а в
экваториальной плоскости располагаются четыре атома кислорода двух молекул
никотиновой кислоты и два - двух молекул внутрисферной воды. В координационное
окружение атома урана никотиновая кислота входит в виде однозарядного
никотинат-аниона (рис. 3) [11].

рис. 3 Фрагмент кристаллической структуры
никотината уранила
Никотинат - ионы являются
бидентатно-циклическими лигандами (тип координации B01)
и расположены в транс-положении относительно друг друга.
. Экспериментальная часть
.1 Методы исследования
Основными методами исследования, которые
применяли в данной работе, явились химический, дифференциальный термический
анализ (ДТА) и ИК спектроскопия.
Химический анализ
Для анализа на содержание урана использовали
весовой метод. Навеска исследуемого вещества прокаливалась в муфельной печи до
800 оС до постоянной массы. Весовой формой являлся U3O8.
Процентное содержание урана рассчитывали по формуле:
%U = (m(U3O8)/mx)·(3M(U)/M(U3O8))
где m(U3O8)
- масса остатка после прокаливания; mx
-
масса навески; M(U)
- молярная масса урана; M(U3O8)
- молярная масса U3O8
Инфракрасная спектроскопия
ИК спектры записывали на спектрофотометре Spectrum
100 (PerkinElmer)
в области 400 - 4000 см-1. Образец готовили в виде смеси с KBr:
навеску полученного вещества массой 1 мг тщательно перетирали в ступке с KBr.
Из полученной смеси под давлением прессовали «таблетку», которая помещалась в
спектрофотометр. Обнаружение отдельных функциональных групп проводили по их
характеристическим частотам по литературным данным [8].
Дифференциальный термический анализ
Съемку дериватограмм проводили на дериватографе
ОД-103 «МОМ». Прокаливание вещества (навеска составляла 0,0686 г) проводилили в
платиновых тиглях. В качестве эталона использовали оксид алюминия.
.2 Синтез и характеристика исходных веществ
В качестве исходных веществ были использованы
оксалат уранила UO2C2O4
·3H2O
и пиридинкарбоновые кислоты (никотиновая, изоникотиновая, пиколиновая). Кислоты
растворяли в воде при нагревании (табл. 2). Оксалат уранила в количестве 0,2 г
так же растворяли в воде. К полученным водным растворам приливали раствор
оксалат уранила. Были добавлены кристаллы щавелевой кислоты H2C2O4.
Медленная кристаллизация на воздухе при комнатной температуре полученных
растворов приводит через 2-3 дня к образованию осадка в виде желтых
мелкокристаллических веществ в растворе, которые после фильтрования
использовались для дальнейших исследований.
Таблица 2. Исходные реагенты
|
Вещество
|
m (г)
|
(мл)
V (H2O)
к кислоте
|
(г)
m (UO2C2O4
·3H2O
)
|
соотношение
кислота : соль
|
|
никотиновая
кислота  0.179 0.179
|
10.0
|
0.2
|
1
: 5
|
|
|
0.179
|
3.0
|
0.2
|
1
: 3
|
|
изоникотиновая
кислота  0.29812.00.21 : 5 0.29812.00.21 : 5
|
|
|
|
|
|
пиколиновая
кислота  0.2980.50.21 : 5 0.2980.50.21 : 5
|
|
|
|
|
Были сняты ИК - спектры исходных веществ (рис.
4, 5, 6, 7)
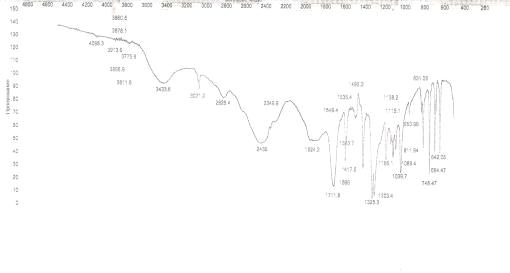
рис. 4 ИК спектр никотиновой кислоты

рис. 5 ИК спектр изоникотиновой кислоты

рис. 6 ИК спектр пиколиновой кислоты
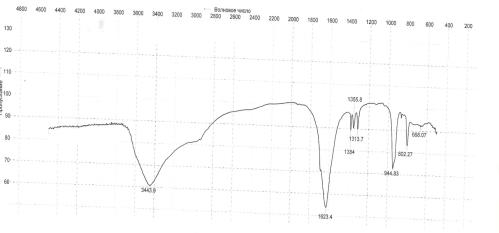
рис. 7 ИК спектр оксалата уранила
.3 Изучение комплексообразования в системе
оксалат уранила с никотиновой кислотой
В качестве исходных веществ использовали оксалат
уранила UO2C2O4
·3H2O
и пиридин-3-карбоновая кислота. В мольных соотношениях 1:3 и 1:5, так как ИК -
спектры, полученных веществ в соответствующих соотношениях, схожи, условно
приняли как за один синтез.
К навеске оксалата уранила UO2C2O4
·3H2O
массой 0.2 грамма приливали 15мл дистиллированной воды. К полученному раствору
добавляли рассчитанное количество никотиновой кислоты. Для ускорения
растворения реакционную смесь нагревали на кипящей водяной бане. После раствор
оставляли кристаллизоваться при комнатной температуре на воздухе в течение 2-3
дней. Выделившиеся желтое мелкокристаллическое вещество отфильтровали и
подвергли исследованиям.
По результатам химического анализа (табл. 3)
состав продукта взаимодействия отвечал UO2C2O4(C5H4NCOO)2(H2O)2
Таблица 3. Результаты химического анализа UO2C2O4(C5H4NCOO)2(H2O)2
|
Содержание
урана, масс. %
|
|
Вычисленное
|
Экспериментальное
|
|
38.26
37.52
|
37.93
|
|
ср.
37.89
|
Для полученного комплекса UO2C2O4(C5H4NCOO)2(H2O)2
нами была записана дериватограмма (рис. 8).

Рис. 8 Дериватограмма UO2C2O4(C5H4NCOO)2(H2O)2
(навеска 0.0686г).
В ИК спектре синтезированного комплекса UO2C2O4(C5H4NCOO)2(H2O)2
присутствуют полосы поглощения, отвечающие ионам уранила, оксалата, молекулам
воды и никотиновой кислоте (рис. 9)

рис. 9 ИК
спектр
UO2C2O4(C5H4NCOO)2(H2O)2
. Выводы
) Осуществлен синтез комплекса с
использованием в качестве исходных веществ оксалат уранила UO2C2O4
·3H2O
и пиридинкарбоновые кислоты (никотиновая кислота). С помощью химического
анализа установлен состав комплекса: UO2C2O4(C5H4NCOO)2(H2O)2
2) Проведено ИК спектроскопическое
исследование UO2C2O4(C5H4NCOO)2(H2O)2.
Установлено наличие в спектрах характеристических частот, отвечающих поглощению
окслат-ионов, ионов уранила, молекул никотиновой кислоты и воды, входящих в
состав соединения.
. Списки использованных источников
1. Химия
актиноидов: В 3-х т. Т.1.: Пер. с англ./Под ред. Каца Дж., Сиборга Г., Морса
Л.. - М.: Мир, 1991. С.525
. Вдовенко
М.В. Химия урана и трансурановых элементов. Изд-во АН СССР Москва-Ленинград.
1960. С. 700
. Третьяков
Ю.Д., Мартыненко Л.И., Григорьев А.Н., Цивадзе А.Ю. Неорганическая химия. Химия
элементов. М.: Академкнига, 2007. С. 538
. Комплексные
соединения урана/ Под ред. Черняева И.И. М.: Наука, 1964. С. 492
. Матюха
В.А., Матюха С.В. Оксалаты редкоземельных элементов и актиноидов. Москва, 2008.
С. 188
6. Poojary
M.D., Pattil K.C.//Proc.Indian Acad.Sci (Chem.Sci). 1987. V. 99. №5-6.
P. 311
. Накамото
К. ИК спектры и спектры КР неорганических и координационных соединений. М.:
Мир, 1991. С. 302
i. Сережкина
Л.Б., Михайлов Ю.Н., Горбунова Ю.Е., Митьковская Е.В., Гре- чишникова Б.В.,
Сережкин В.Н. // Журн. неорган, химии. 2005. Т. 50. № 8. С.1273.
9. Митьковская
Е.В., Михайлов Ю.Н., Горбунова Ю.Е., Сережкина Л.Б., Сережкин B.II.
// Журн. неорган, химии. 2004. Т. 49. № 9. С. 1538.
10. Alcock
N.W., Errington W., Kemp T.J. et al. // Acta Cryst. 1996. V. C52. № 3. P. 615.
11. Порай-Кошиц
M.A.,
Сережкин В.Н. // Журн. неорган, химии. 1994 Т. 39. № 7. С. 1109.