Валидационная оценка методов качественного и количественного анализа ингредиентов лекарственного средства
Пятигорский
филиал государственного бюджетного образовательного учреждения высшего
профессионального образования
Волгоградский
государственный медицинский университет
Министерства
здравоохранения Российской Федерации
Курсовая
работа
Валидационная
оценка методов качественного и количественного анализа ингредиентов
лекарственного средства Папаверина гидрохлорида 2% раствора для инъекций
Исполнитель: студент 5 курса 16
группы
Семенов Сергей Юрьевич
Руководитель: к. ф. н., старший
преподаватель
А.Г. Курегян
Пятигорск,
2012
Содержание
Введение
Глава 1. Анализ папаверина
гидрохлорида в субстанции и в лекарственных формах
.1 Способы анализа папаверина
гидрохлорида в субстанции
.1.1 Подлинность
.1.2 Посторонние примеси
.1.3 Количественное определение
.2 Методы анализа папаверина
гидрохлорида в лекарственных формах
.2.1 Папаверина гидрохлорид в
растворе для инъекций
.2.2 Папаверина гидрохлорид в
таблетках
.2.3 Папаверина гидрохлорид в
суппозиториях
Глава 2. Валидация методик анализа
папаверина гидрохлорида в растворе для инъекций 2%
.1 Приготовление модельной смеси
.2 Линейность (linearity)
.3 Правильность (accuracy)
.4 Прецизионность (precision)
Список литературы
Введение
Валидация аналитической методики
- это экспериментальное доказательство того, что методика пригодна для решения
предполагаемых задач.
Необходимость валидации всех аналитических
методик не вызывает сомнений - это один из элементов валидации всего процесса
производства лекарств. Кроме этого, с практической точки зрения, валидация аналитических
методик дает ряд существенных "вторичных" полезных эффектов.
Во-первых, при проведении валидации в процессе
разработки новых методик можно своевременно выявить их недостатки и на ранних
стадиях существенно улучшить методику. Во-вторых, при грамотно и качественно
выполненной работе появляется уверенность и в методике, и в качестве
анализируемого препарата. В третьих, в процессе валидации обязательно принимают
практическое участие различные аналитические лаборатории. Практика
валидационных экспериментов дает понимание сути методики и осознание
необходимости строгого соблюдения ее параметров. В результате, при последующей
эксплуатации валидированной методики значительно снижается вероятность ошибок.
Для валидации методик используются
следующие параметры:
 правильность
(accuracy) - близость получаемых результатов к истинному значению, оценивается
по погрешности определения;
правильность
(accuracy) - близость получаемых результатов к истинному значению, оценивается
по погрешности определения;
 специфичность (specificity) -
способность измерять точно и селективно аналит (определяемое вещество) в
присутствии компонентов, которые могут ожидаться в матрице образца (примеси,
родственные химические соединения, продукты разложения, ингредиенты плацебо),
также оценивается по погрешности определения;
специфичность (specificity) -
способность измерять точно и селективно аналит (определяемое вещество) в
присутствии компонентов, которые могут ожидаться в матрице образца (примеси,
родственные химические соединения, продукты разложения, ингредиенты плацебо),
также оценивается по погрешности определения;
 точность (precision) - мера
сходимости результатов при многократном повторении аналитической процедуры.
точность (precision) - мера
сходимости результатов при многократном повторении аналитической процедуры.
Точность методики определяется двумя
параметрами: сходимость и воспроизводимость.
 сходимость (repeatability) -
близость результатов индивидуальных тесто в, когда процедура анализа
повторяется на многочисленных пробах гомогенного образца одинаковых проб в
нормальных условиях проведения анализа (иногда переводится как повторяемость),
критерием является стандартное отклонение параллельных определений;
сходимость (repeatability) -
близость результатов индивидуальных тесто в, когда процедура анализа
повторяется на многочисленных пробах гомогенного образца одинаковых проб в
нормальных условиях проведения анализа (иногда переводится как повторяемость),
критерием является стандартное отклонение параллельных определений;
 воспроизводимость
(reproducibility) - степень сходимости результатов, полученных анализом одних и
тех же образцов при различных нормальных условиях теста - разные лаборатории,
химики-аналитики, инструменты, партии реактивов, температура окружающей среды,
различное время проведения анализов и т.п., также оценивается по стандартному
отклонению параллельных определений;
воспроизводимость
(reproducibility) - степень сходимости результатов, полученных анализом одних и
тех же образцов при различных нормальных условиях теста - разные лаборатории,
химики-аналитики, инструменты, партии реактивов, температура окружающей среды,
различное время проведения анализов и т.п., также оценивается по стандартному
отклонению параллельных определений;
 линейность (linearity) -
способность показать, что результаты теста сразу или после определенной
математической обработки пропорциональны концентрации аналита в образце в
пределах данного интервала, определяется математической обработкой результатов
теста образцов с различными концентрациями аналита в пределах интервала,
установленного для данного метода. Обычно производится расчет линии регрессии
методом наименьших квадратов для результатов с различными концентрациями
аналита. Наклон регрессионной линии и его вариация дает математическую степень
линейности. Для оценки степени линейности должны быть рассчитаны коэффициент
корреляции, перекрывание оси Y, наклон регрессионной линии и остаточная сумма
отклонений;
линейность (linearity) -
способность показать, что результаты теста сразу или после определенной
математической обработки пропорциональны концентрации аналита в образце в
пределах данного интервала, определяется математической обработкой результатов
теста образцов с различными концентрациями аналита в пределах интервала,
установленного для данного метода. Обычно производится расчет линии регрессии
методом наименьших квадратов для результатов с различными концентрациями
аналита. Наклон регрессионной линии и его вариация дает математическую степень
линейности. Для оценки степени линейности должны быть рассчитаны коэффициент
корреляции, перекрывание оси Y, наклон регрессионной линии и остаточная сумма
отклонений;
 интервал метода (range) оценивается
проверкой того, как данный аналитический метод обеспечивает точность,
правильность и линейность при определении образцов, содержащих аналит на
границах интервала и внутри его. Определяется в ходе проведения испытаний по
каждому из перечисленных параметров;
интервал метода (range) оценивается
проверкой того, как данный аналитический метод обеспечивает точность,
правильность и линейность при определении образцов, содержащих аналит на
границах интервала и внутри его. Определяется в ходе проведения испытаний по
каждому из перечисленных параметров;
 предел обнаружения (limit of
detection) - параметр предельных тестов - минимальная концентрация аналита в
образце, которая может быть обнаружена, но не определена количественно в
условиях анализа. Определение предела обнаружения варьируется в зависимости от
типа метода (инструментальный или неинструментальный). Для инструментальных
методов в основном определяют отношение сигнал/шум или измеряют величину
фонового сигнала, после чего рассчитывают минимальный уровень (обычно принимают
отношение сигнал/шум = 2:1 или 3:1). Этот предел потом оценивается анализом
ряда образцов с содержанием аналита близким к пределу (реальных или специально
приготовленных). Для неинструментальных методов предел обнаружения определяется
анализом образцов с известными концентрациями аналита и установлением
минимального уровня аналита, при котором он может быть достоверно обнаружен;
предел обнаружения (limit of
detection) - параметр предельных тестов - минимальная концентрация аналита в
образце, которая может быть обнаружена, но не определена количественно в
условиях анализа. Определение предела обнаружения варьируется в зависимости от
типа метода (инструментальный или неинструментальный). Для инструментальных
методов в основном определяют отношение сигнал/шум или измеряют величину
фонового сигнала, после чего рассчитывают минимальный уровень (обычно принимают
отношение сигнал/шум = 2:1 или 3:1). Этот предел потом оценивается анализом
ряда образцов с содержанием аналита близким к пределу (реальных или специально
приготовленных). Для неинструментальных методов предел обнаружения определяется
анализом образцов с известными концентрациями аналита и установлением
минимального уровня аналита, при котором он может быть достоверно обнаружен;
 количественного определения
(limit of quantitation) - параметр количественного определения для низших
уровней содержания веществ в пробе образцов, таких как примеси или продукты
разложения. Это минимальная концентрация аналита в образце, которая может быть
определена с приемлемой точностью в условиях анализа. Выражается концентрацией
аналита в образце. Определение, так же как и в случае предела обнаружения,
различается для инструментальных и неинструментальных методов. Процедура
аналогична, обычно используют значение фактора, равное 10;
количественного определения
(limit of quantitation) - параметр количественного определения для низших
уровней содержания веществ в пробе образцов, таких как примеси или продукты
разложения. Это минимальная концентрация аналита в образце, которая может быть
определена с приемлемой точностью в условиях анализа. Выражается концентрацией
аналита в образце. Определение, так же как и в случае предела обнаружения,
различается для инструментальных и неинструментальных методов. Процедура
аналогична, обычно используют значение фактора, равное 10;
 устойчивость (robustness) -
мера способности не подвергаться воздействию небольших, но запредельных
отклонений параметров методики - показывает точность и правильность в
нормальных условиях. Определяется проведением теста правильности при небольших
отклонениях параметров методики или свойств анализируемого объекта.
Рассчитывается погрешность по сравнению с результатами, полученными в
нормальных условиях. Если наблюдается влияние параметров методики, это
оговаривается в тексте методики.
устойчивость (robustness) -
мера способности не подвергаться воздействию небольших, но запредельных
отклонений параметров методики - показывает точность и правильность в
нормальных условиях. Определяется проведением теста правильности при небольших
отклонениях параметров методики или свойств анализируемого объекта.
Рассчитывается погрешность по сравнению с результатами, полученными в
нормальных условиях. Если наблюдается влияние параметров методики, это
оговаривается в тексте методики.
Глава 1. Анализ папаверина
гидрохлорида в субстанции и в лекарственных формах
Папаверин является алкалоидом, впервые
выделенным из опия в 1884 г. Мерком. По химической структуре он относится к
производным бензилизохинолина. В 1910 г. был осуществлен синтез папаверина.
Природный и синтетический папаверины идентичны в фармакологическом отношении.

Химическое название:
1-(3,4-диметоксибензил)-6,7-диметоксиизохинолин
Папаверина гидрохлорид субстанция представляет
собой белые или почти белые кристаллы или белый или почти белый кристаллический
порошок без запаха[1]. Инъекционный раствор - прозрачная бесцветная или слегка
желтоватая жидкость.
По физико-химическим свойствам папаверина г/хл
является солью слабого азотистого основания, обладает свойствами
восстановителя, что объясняется наличием в структуре 2 ароматических
фрагментов, связанных метиленовой группой, а также 4 метоксидных групп.[4]
Т.пл. 147°C.
Папаверин растворим в хлороформе, умеренно
растворим в воде, мало растворим в 96% этаноле, практически нерастворим в
эфире.[2]
1.1 Способы анализа папаверина
гидрохлорида в субстанции
.1.1 Подлинность
Подлинность субстанции можно определять как
химическим, так и физическим методами.
Химические реакции подлинности основаны на его
свойствах.
Для идентификации используют реакции со
специальными реактивами на алкалоиды, действие которых основано на окислении
папаверина:
· Под действием концентрированной азотной кислоты
папаверина гидрохлорид приобретает желтое окрашивание, которое переходит в
оранжевое при нагревании на водяной бане
· Нагревание его с концентрированной
серной кислотой приводит к появлению фиолетового окрашивания.

· Окрашенные продукты также образуются при
взаимодействии с реактивом Марки. При последующем добавлении бромной воды и
раствора аммиака появляется фиолетовый осадок, который после растворения в
этаноле окрашивает раствор в фиолетово-красный цвет (реакция является
специфичной для папаверина и используется в его фотоколориметрическом определении).
· Положительную реакцию дает
папаверина гидрохлорид с реактивом Фреде, при его обработке уксусным ангидридом
и концентрированной серной кислотой после нагревания на водяной бане появляется
желтое окрашивание с зеленой флуоресценцией.

· С перманганатом калия в кислой среде папаверина
гидрохлорид образует продукты, флуоресцирующие голубым светом.
Кроме того папаверина гидрохлорид дает некоторые
реакции с осадительными реактивами:
v Бромная вода выделяет из раствора желтый осадок.
v Спиртовой раствор йода - темно-красные
кристаллы.
v С пикриновой кислотой образуется желтый осадок.
v Также выпадают осадки под действием реактивов
Драгендорфа и Майера.
Субстанция дает характерную реакцию на
хлориды[1].
Физико-химические методы:
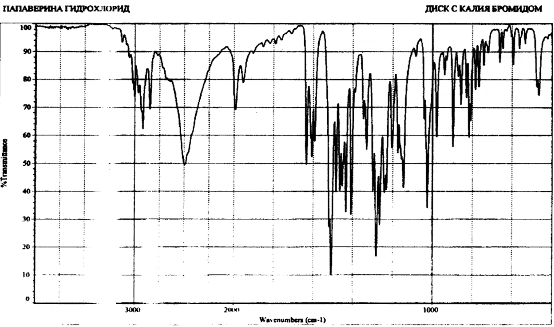
ü ИК-спектр
субстанции, снятый в диске с калия бромидом, в области от 4000 до 400 см-1 по
положению полос поглощения должен соответствовать рисунку спектра папаверина
гидрохлорида.[1]
ü УФ-спектр
поглощения 0,0005% раствора субстанции в 0,01 М растворе хлористоводородной
кислоты в области от 230 до 270 нм должен иметь максимум при 251 нм[1].
ü УФ-спектр поглощения 0,0025%
раствора субстанции в 0,01 М растворе хлористоводородной кислоты в области от
270 до 350 нм должен иметь максимумы при 285 и при 285нм и 09нм[1].
.1.2 Посторонние примеси
Содержание посторонних примесей устанавливается
методами тонкослойной хроматографии или ВЭЖХ.
ТСХ. Испытуемый раствор. 0,25 г
субстанции растворяют в 5 мл хлороформа.
Раствор сравнения. 0,5
мл испытуемого раствора разбавляют хлороформом до 100мл.
На линию старта пластинки со слоем силикагеля 60
F254 наносят 10 мкл
(500 мкг) испытуемого раствора, 10 мкл (2,5 мкг) и 2 мкл (0,5 мкг) раствора
сравнения. Пластинку с нанесенными пробами сушат на воздухе, помещают в камеру
со смесью толуол - этилацетат - диэтиламин (7:2:1) и хроматографируют
восходящим методом. Когда фронт подвижной фазы дойдет до конца пластинки, ее вынимают
из камеры, сушат на воздухе в течение 20 минут и просматривают в УФ-свете при
254нм.
Пятно любой посторонней примеси на хроматограмме
испытуемого раствора по совокупности величины и интенсивности поглощения не
должно превышать пятно на хроматограмме раствора сравнения (0,5 мкг, не более
0,1%). Суммарное содержание примесей, оцененное по совокупности величины и
интенсивности поглощения их пятен на хроматограмме испытуемого раствора в
сравнении с пятном на хроматограмме раствора сравнения (2,5 мкг), не должно
превышать 0,5%. Пятно на старте в расчет не принимают.
Результаты испытания считаются достоверными,
если на хроматограмме раствора сравнения (0,5 мкг) четко видно пятно.
.1.3 Количественное определение
Папаверина гидрохлорид количественно определяют
химическими и физико-химическими методами:
Химические методы:
1. Методом неводного титрования в смеси
муравьиной кислот и уксусного ангидрида (фармакопейный метод - ФС 42-3149-95).
Около 0,3 г препарата (точная навеска) растворяют в 1мл кислоты муравьиной,
прибавляют 10 мл ангидрида уксусного и титруют 0,1 М раствором кислоты хлорной
до ярко-желтого окрашивания (индикатор - раствор кристаллического фиолетового
0,15 мл). Параллельно проводят контрольный опыт.
. Методом нейтрализации в спиртовой среде
(фармакопейный метод - ГФ Х, с 356) Около 0,5 г препарата (точная навеска)
растворяют в 50 мл свежепрокипяченной и охлажденной воды, прибавляют 25
нейтрализованного по фенолфталеину спирта и титруют раствором натрия гидроксида
0,1 моль/л до розового окрашивания (индикатор фенолфталеин).
3. Аргентометрическим методом по
хлорид-иону.
Физико-химические методы:
1) Экстракционно-фотометрическое определение.
Основано на измерении светопоглощения комплексного соединения с изотиоцианатом
аммония и хлоридом железа(III),
а так же на избирательном взаимодействии с красителем оранжевым Ж.
2) Спектрофотометрическое определение.
Проводят в тех же растворителях и при тех же длинах волн, что и подлинность,
содержание рассчитывают по стандартному образцу[2].
) Экстракционно-титриметрическое
определение с использованием в качестве титранта лаурилсульфата натрия.
.2 Методы анализа папаверина
гидрохлорида в лекарственных формах
папаверин примесь хроматография
Папаверина гидрохлорид выпускается в нескольких
лекарственных формах, это таблетки, раствор для инъекций и суппозитории.
.2.1 Папаверина гидрохлорид в
растворе для инъекций
Подлинность:
1. Химические реакции:
o с кислотой азотной
концентрированной: 1 мл препарата помещают в фарфоровую чашку, выпаривают
досуха, охлаждают, прибавляют 2 капли конц. азотной кислоты; появляется желтое
окрашивание, которое при нагревании на водяной бане переходит в оранжевое.
o с серной кислотой концентрированной,
кислотой пикриновой, с реактивами Марки, Фреде, Эрдмана, Драгендорфа, Майера.
2. Физико-химические методы:
· УФ-спектр раствора препарата, взятого в той же
концентрации, что и для количественного определения в области от 270 до 359 нм,
имеет максимумы поглощения при длине волны около 284±1 и 309±1 нм.
Примеси:
Содержание примесей определяют методом
тонкослойной хроматографии (не больше 1%).
Количественное определение:
) Методом УФ-спектрофотометрии в сравнении с
РСО:
мл препарата помещают в мерную колбу
вместимостью 100 мл, доводят объем раствора 0,1 М раствором HCL
до метки и перемешивают.
мл полученного раствора помещают в мерную колбу
на 100 мл, доводят объем раствора 0,1 М раствором HCL
до метки и перемешивают.
Измеряют оптическую плотность полученного
раствора на спектрофотометре в максимуме поглощения при длине волны 309 нм в
кювете с толщиной слоя 10 мм. Параллельно измеряют оптическую плотность РСО
папаверина. В качестве раствора сравнения используют 0,1 М раствор кислоты
хлористоводородной.
Содержание папаверина г/хл в 1 мл препарата в
граммах вычисляют по формуле:

где D1
- оптическая плотность испытуемого раствора;
D0 - оптическая
плотность раствора РСО папаверина г/хл;
а 0 - навеска РСО папаверина г/хл в граммах.
) Методом неводного титрования в смеси
муравьиной кислот и уксусного ангидрида (фармакопейный метод - ФС 42-3149-95).
) Аргентометрическим методом по хлорид-иону.
) Методом нейтрализации в спиртовой среде
(фармакопейный метод - ГФ Х, с 356).
.2.2 Папаверина гидрохлорид в
таблетках
Подлинность:
1. Химические реакции
o См
. Физико-химические методы:
· ИК-спектроскопия (см. в п. 1.1.3.)
· УФ-спектрофотометрия (см. в п.
1.1.3.)
· Хроматография в тонком слое сорбента
· Экстракционно-фотометрический метод
Примеси:
Содержание примесей определяют методом
тонкослойной хроматографии (см. в п. 1.1.2.).
Количественное определение:
1) Методом УФ-спектроскопии
2) Методом неводного титрования в смеси
муравьиной кислот и уксусного ангидрида (фармакопейный метод - ФС 42-3149-95).
) Аргентометрическим методом по
хлорид-иону.
) Методом нейтрализации в спиртовой среде
(фармакопейный метод - ГФ Х, с 356).
.2.3 Папаверина гидрохлорид в
суппозиториях
Подлинность:
Химические реакции:
o См
Физико-химические методы:
· Одну свечу помещают в колбу вместимостью 50 мл,
прибавляют 10 мл воды, нагревают на водяной бане до расплавления, тщательно
взбалтывают, охлаждают до застывания основы и водный слой фильтруют. 2 мл
фильтрата помещают в фарфоровую чашку и выпаривают на водяной бане досуха. К
остатку прибавляют 8 капель кислоты азотной концентрированной; появляется желтое
окрашивание, которое при нагревании переходит в оранжево-красное.
· 2 мл фильтрата дают характерную
ракцию на хлориды (ГФ XI, вып. 1, с 159)
Примеси:
Содержание примесей определяют методом
тонкослойной хроматографии (см. в п. 1.1.2.).
) Одну свечу помещают в колбу вместимостью
50 мл, прибавляют 10 мл воды, нагревают на водяной бане до расплавления,
тщательно взбалтывают, охлаждают до застывания основы и водный слой фильтруют в
колбу для титрования. Промывают колбу и фильтр 5 мл воды, операцию повторяют
еще раз. К фильтрату добавляют 2-3 капли индикатора фенолфталеина и титруют
раствором натрия гидроксида 0,02 моль/л до розового окрашивания. Содержание
папаверина гидрохлорида в одной свече должно быть от 0,018 г до 0,022 г (по среднему
результату трех параллельных определений).
2) Методом неводного титрования в смеси
муравьиной кислот и уксусного ангидрида (фармакопейный метод - ФС 42-3149-95).
) УФ-спектрофотометрия
Глава 2. Валидация методик анализа
папаверина гидрохлорида в растворе для инъекций 2%
2.1 Приготовление
модельной смеси
Около 0,05 г (точная навеска) СО папаверина
гидрохлорида помещают в мерную колбу вместимостью 100 мл, растворяют в 50 мл
0,1 М раствора кислоты хлористоводородной и доводят тем же растворителем до метки
(раствор А).
мл полученного раствора переносят в мерную колбу
вместимостью 100 мл и доводят до метки тем же растворителем (раствор Б).
Изучают спектр поглощения раствора Б на
спектрофотометре в области 230 - 270 нм. Раствор имеет максимум при длине волны
251 нм.
.2 Линейность
(linearity)
В мерную колбу вместимостью 100 мл вносят 0,05 г
СО папаверина гидрохлорида растворяют в 50 мл 0,1 М раствора кислоты
хлористоводородной и доводят тем же растворителем до метки (раствор А).
В мерные колбы вместимостью 100 мл
последовательно вносят 1,0; 2,0; 3,0; 4,0; 5,0 мл раствора А и доводят до метки
тем же растворителем. Получают растворы с концентрацией 0,0005%, 0,001%,
0,0015%, 0,002%; 0,0025%.
Измеряют оптическую плотность каждого раствора
при длине волны 309 нм в кювете с толщиной слоя 1 см. Раствор сравнения - 0,1 М
раствор кислоты хлористоводородной.
Строят градуировочный график зависимости
оптической плотности от концентрации, рассчитывают уравнение градуировочного
графика и коэффициент корреляции. Данные заносят в таблицу 1.
Таблица 1 - зависимость оптической плотности от
концентрации
|
Объем
раствора А, мл
|
1,0
|
2,0
|
3,0
|
4,0
|
5,0
|
|
Концентрация
полученного раствора в %
|
0,0005
|
0,0010
|
0,0015
|
0,0020
|
0,0025
|
|
Оптическая
плотность
|
0,098
|
0,235
|
0,310
|
0,425
|
0,489
|

2.3 Правильность
(accuracy)
Приготовление трех растворов
модельных смесей.
Раствор А1 (модельная смесь 1) Точную
навеску модельной смеси 0,375 г помещают в мерную колбу вместимостью 25 мл,
растворяют в 0,1 М растворе кислоты хлористоводородной и доводят этим
растворителем до метки.
Раствор А2 (модельная смесь 2) Точную
навеску модельной смеси 0,500 г помещают в мерную колбу вместимостью 25 мл,
растворяют в 0,1 М растворе кислоты хлористоводородной и доводят этим растворителем
до метки.
Раствор А3 (модельная смесь 3) Точную
навеску модельной смеси 0,625 г помещают в мерную колбу вместимостью 100 мл,
растворяют в 0,1 М растворе кислоты хлористоводородной и доводят этим
растворителем до метки.
Далее:

Разведения модельных смесей
Раствор Б1. В мерную колбу
вместимостью 100 мл вносят 2,5 мл раствора А1 и доводят до метки 0,1
М раствором кислоты хлористоводородной.
Раствор Б2. В мерную колбу
вместимостью 100 мл вносят 2,5 мл раствора А2 и доводят до метки 0,1
М раствором кислоты хлористоводородной.
Раствор Б3. В мерную колбу
вместимостью 100 мл вносят 2,5 мл раствора А3 и доводят до метки 0,1
М раствором кислоты хлористоводородной.
Итоговые разведения для
спектрофотометрии.
Растворы В1, В2, В3
. В три мерные колбы вместимостью 50 мл вносят по 2 мл раствора Б 1 и доводят
до метки 0,1 М раствором кислоты хлористоводородной.
Растворы В4, В5, В6
. В три мерные колбы вместимостью 50 мл вносят по 2 мл раствора Б2 и
доводят до метки 0,1 М раствором кислоты хлористоводородной.
Растворы В7, В8, В9
. В три мерные колбы вместимостью 50 мл вносят по 2 мл раствора Б 3 и доводят
до метки 0,1 М раствором кислоты хлористоводородной.
Измеряют оптическую плотность каждого из 9
приготовленных растворов на спектрофотометре при длине волны 309 нм в кювете с
толщиной слоя 1 см.
Параллельно измеряют оптическую плотность
раствора СО папаверина гидрохлорида.
Приготовление раствора СО папаверина
гидрохлорида.
Около 0,05 г (точная навеска) папаверина
гидрохлорида растворяют в 0,1 М растворе кислоты хлористоводородной и доводят
этим растворителем до метки (раствор А).
мл полученного раствора переносят в мерную колбу
вместимостью 50 мл и доводят до метки тем же растворителем (раствор Б),
мл раствора Б содержит 0,00002 г папаверина
гидрохлорида.
Расчет содержания папаверина гидрохлорида в
процентах (открываемость R)
проводят по формуле:

 (1),
(1),
где: Ах - оптическая плотность исследуемого
раствора;
Ао - оптическая плотность раствора СО папаверина
гидрохлорида;
ах - масса навески исследуемого образца
папаверина гидрохлорида;
,00002 - содержание папаверина гидрохлорида в г
в 1 мл раствора СО.
Результаты заносят в таблицу № и рассчитывают
стандартное (SD) и относительное
стандартное отклонение (RSD).
Таблица 2 - Правильность
|
Разведение
|
В
1
|
В
2
|
В
3
|
В
4
|
В
6
|
В
7
|
В
8
|
В
9
|
|
Оптическая
плотность
|
0,190
|
0,198
|
0,208
|
0,444
|
0,433
|
0,440
|
0,539
|
0,545
|
0,547
|
|
Содержание
папаверина
|
|
|
|
|
|
|
|
|
|
2.4 Прецизионность
(precision)

Приготовить раствор Б2 модельной
смеси.
Растворы В1, В2, В3.
В три мерные колбы вместимостью 50 мл вносят по 1 мл раствора Б2 и
доводят до метки 0,1 М раствором кислоты хлористоводородной.
Растворы В4, В5, В6.
В три мерные колбы вместимостью 50 мл вносят по 2 мл раствора Б2 и
доводят до метки 0,1 М раствором кислоты хлористоводородной.
Растворы В7, В8, В9.
В три мерные колбы вместимостью 50 мл вносят по 3 мл раствора Б2 и
доводят до метки 0,1 М раствором кислоты хлористоводородной.
Измеряют оптическую плотность каждого из 9
приготовленных растворов на спектрофотометре при длине волны 309 нм в кювете с
толщиной слоя 1 см.
Параллельно измеряют оптическую плотность
раствора СО папаверина гидрохлорида.
Расчет содержания папаверина гидрохлорида в
граммах в 1 мл проводят по формуле:

 (2),
(2),
где: Ах - оптическая плотность исследуемого
раствора;
Ао - оптическая плотность раствора СО папаверина
гидрохлорида;
,00002 - содержание папаверина гидрохлорида в г
в 1 мл раствора СО;
Va - объем
аликвоты раствора Б, взятый для разведения, мл.
Результаты заносят в таблицу и рассчитывают
стандартное отклонение (SD)
и относительное стандартное отклонение (RSD).
Таблица 3 - Прецизионность
|
Разведение
|
В
1
|
В
2
|
В
3
|
В
4
|
В
5
|
В
6
|
В
7
|
В
8
|
В
9
|
|
Оптическая
плотность
|
0,209
|
0,214
|
0,224
|
0,352
|
0,369
|
0,363
|
0,698
|
0,712
|
0,719
|
|
Содержание
папаверина
|
|
|
|
|
|
|
|
|
|
Список литературы
1. ГФ 12. ФС 42-0267-07.
2. Беликов В.Г.
Фармацевтическая химия
. ФСП 42-0152-1850-01
. Арзамасцев