Эквивалентная масса химических соединений
Цель работы: пользуясь методом вытеснения водорода или другого газа, определить
эквивалентные массы металла и соли.
Экспериментальная часть
1. Определение
эквивалентной массы металла методом вытеснения водорода
1.1. Ход и данные опыта
В данном опыте, для определения
объема выделившегося водорода в реакции двухвалентного металла используется
пробор «бюретка» (рис. 1).
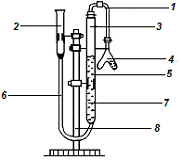
1) Трубка для передачи
выделившегося газа с сосуд с водой
) Емкость для вытесненной
жидкости
) Скопление газа в трубе
) Колба Оствальда
) Емкость для скопления
жидкости и газа с делениями
) Трубка, соединяющая емкость
для скопления газа и жидкости с емкостью для вытесненной жидкости
) Использующаяся в опыте
жидкость
) Штатив
Рис.1
Порядок выполнения опыта
В одно колено колбы Оствальда
поместим образец металла, а в другое раствор соляной кислоты. Затем наклоним
колбу так, чтобы соляная кислота соединилась с металлом. После окончания
выделения водорода, находим давление выделившегося водорода, как разность
атмосферного давления и давление насыщенных водяных паров. Далее с помощью
закона эквивалентов мы определяем молярную массу металла, по которой и
определяем металл.
Численные данные представлены в
таблице 1.
Таблица 1.
|
Наименование измерений
|
Обозначение
|
Численные значения
|
Единица измерения
|
|
Масса образца металла
|
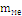
|
0,0158
|
Г
|
|
Температура опыта
|
T
|
293
|
K
|
|
Объем выделившегося H2
|
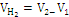
|
16,3
|
Мл
|
|
Атмосферное давление
|
Pатм
|
738
|
мм. рт. ст.
|
|
Давление насыщенных водяных паров
|

|
17,54
|
мм. рт. ст.
|
|
Давление выделившегося H2
|
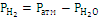
|
720,46
|
мм. рт. ст.
|
Расчеты:
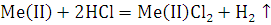
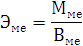
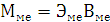
По закону эквивалентов:
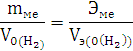
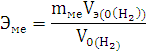
По уравнению состояния идеального
газа:
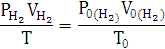


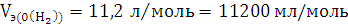

Элемент с ближайшим значением
молярной массы Mg.
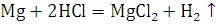
1.2 Анализ результатов опыта
. Какой металл
использовался в эксперименте. Кратко опишите его физические и химические
свойств.
В данном эксперименте использовался
магний. Mg - твердое вещество серебристого цвета (при н.у.). Относиться к
щёлочноземельным металлам. Двухвалентен. Активен. Проводит электрический ток.
Реагирует с кислотами и солями аммония, раскалённый магний реагирует с водой,
сгорает на воздухе, горит в углекислом газе.
2. Рассчитайте
абсолютную и относительную погрешности опыта
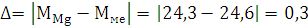 г/моль
- абсолютная погрешность
г/моль
- абсолютная погрешность
 -
относительная погрешность
-
относительная погрешность
3. При определении эквивалентной массы каких металлов раствор
кислоты можно заменить на раствор щёлочи? Приведите примеры.
С растворами щелочи реагируют
амфотерные металлы, такие как цинк, олово, алюминий. Примеры:


2. Определение
эквивалентной массы соли
2.1 Ход и данные опыта
В данном опыте наши действие
практически соответствуют первому, за исключением того, что в реакцию вступает
не металл, а соль - карбонат натрия. Для меньшей погрешности воду следует
заменить раствором NaCl. Пользуясь законом эквивалентов, найдем, эквивалентную массу
карбоната кальция. Численные данные представлены в таблице 2.
Таблица 2.
|
Наименование измеренийОбозначениеЧисленные значенияЕдиница
измерения
|
|
|
|
|
Масса CaCO3
|
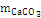
|
0,038
|
Г
|
|
Температура опыта
|
T
|
293
|
K
|
|
Объем выделившегося CO2
|

|
9,3
|
Мл
|
|
Атмосферное давление
|
Pатм
|
738
|
мм. рт. ст.
|
|
Давление насыщенных водяных паров
|

|
17,54
|
мм. рт. ст.
|
|
Давление выделившегося CO2
|

|
720,46
|
мм. рт. ст.
|
Расчеты:
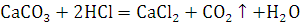
Согласно закону эквивалентов:



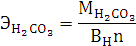

Согласно уравнению
Менделеева-Клапейрона:


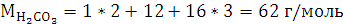
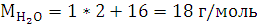
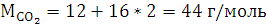

2.2 Анализ результатов опыта
. Определите
теоретическое значение эквивалентной массы CaCO3. Рассчитайте абсолютную и относительную погрешности опыта.
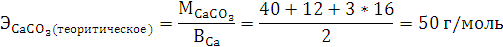

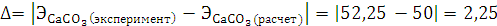 г/моль
- абсолютная погрешность
г/моль
- абсолютная погрешность
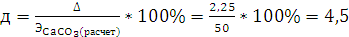 % -
относительная погрешность
% -
относительная погрешность
2. Объясните почему
при расчетах  использовали
значение эквивалентной массы
использовали
значение эквивалентной массы 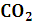 2 раза больше теоритического.
2 раза больше теоритического.
При расчете эквивалентной массы
карбоната кальция использовалось значение эквивалентной массы углекислого газа
в два раза больше теоретического, потому что в зависимости от реакции
эквивалент сложных соединений может изменяться.
3. Сделайте вывод о
влиянии характера реакции и значения эквивалента сложных веществ.
Эквивалент вещества может изменяться
в зависимости от реакции. Так при разложении 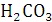 эквивалент
эквивалент  равен
22, в то время как теоретический (рассчитанный по формуле
равен
22, в то время как теоретический (рассчитанный по формуле 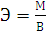 ) равен 11.
) равен 11.
эквивалент
химический магний водород
Ответы на контрольные
вопросы
1.
I)
Ответ: В оксиде мышьяка (V) его эквивалентная масса равна 15
г/моль, а в оксиде мышьяка (III) 25 г/моль.
II)
Эквивалент химического элемента
зависит от его валентности, так как в разных оксидах валентность мышьяка
разная, то и эквивалентные массы тоже разные.
2.