Некоторые особенности растворов
Содержание
1. Растворы
2. Некоторые особенности растворов
2.1 Твердые растворы
2.2 Растворы с эвтектикой
2.3 Растворы газов в жидкостях
2.4 Трехкомпонентные системы. Экстракция
Список использованной литературы
1.
Растворы
Растворы широко распространены в природе и
повсеместно используются на практике. Химически чистые вещества по существу
отражают их предельное состояние, которое, строго говоря, не достигается. Даже
металлы, получаемые методом вакуумной и зонной плавки, содержат ничтожное
количество примесей, достигающее 10-6%, а значит, являются твердыми
растворами.
В жидких растворах существенно изменяются
условия протекания химических реакций. Многие технологические процессы
протекают только в растворах (разделение промышленных и природных жидких смесей,
получение необходимых веществ методом экстракции, ректификации, кристаллизации
и т.д.). Исключительная роль во всех биологических процессах и большинстве
производственных технологий принадлежит водным растворам. Неводные растворы
применяют главным образом при производстве полимеров, красителей, лаков и
других веществ.
Технология некоторых отраслей
промышленности базируется на твердых растворах, свойства которых, в частности,
определяют прочность и работоспособность металлических сплавов и искусственных
материалов с заранее заданными характеристиками.
Качественное (фазовое) состояние и
количественные характеристики растворов определяются некоторыми константами
(например, температурой замерзания и кипения) и параметрами (составом,
концентрацией, давлением пара над раствором и др.).
2. Некоторые
особенности растворов
Помимо жидких существуют твердые растворы
и растворы газов в жидкостях, специфические свойства которых рассматриваются в
этой главе. Подобные растворы имеют важное значение в различных отраслях
промышленности (в производстве искусственных материалов, керамики, стекла, в
металлургии, легкой и пищевой промышленности, и др.) и во многих случаях
определяют специфику технологического процесса и свойства выпускаемой
продукции.
Знакомство с особенностями
трехкомпонентных систем (определением их состава, условиями распределения
третьего компонента между двумя, извлечением из смеси необходимых веществ)
расширяет представление о растворах.
2.1 Твердые
растворы
Твердыми растворами называют однородные системы,
состоящие из двух и более твердых компонентов. При рассмотрении под микроскопом
структура кристаллических твердых растворов представляется гомогенной - в виде
однородных кристаллических элементов.
Способность образовывать твердые растворы
свойственна всем кристаллическим твердым телам. В большинстве случаев она
ограничена узким интервалом концентрации растворенного твердого вещества,
значительно реже - при любых концентрациях.
В зависимости от способов получения, а
также от особенностей взаимодействия компонентов твердые растворы могут быть растворами
замещения, внедрения и вычитания.
В твердых растворах
замещения сохраняется
структура кристаллической решетки растворителя. Молекулы, атомы или ионы
растворенного вещества помещаются в узлах кристаллической решетки растворителя,
как бы замещают его атомы. Образованию подобных растворов способствуют близость
строения кристаллических решеток растворенного вещества и растворителя, а
следовательно, и близость кристаллохимических свойств.
Если атомы компонентов твердого раствора
существенно отличаются по размерам, то возможно внедрение атомов одного
элемента между узлами кристаллической решетки другого, и образуются так
называемые твердые растворы внедрения.
Подобные системы образуются при
растворении неметаллов (бора, водорода, кислорода, азота, углерода) в металлах.
Внедрение инородных атомов в промежутках между атомами металлов приводит к
росту напряжения в кристаллической решетке. В связи с этим концентрация
растворенного вещества в этих растворах относительно невелика. Наиболее
распространенным твердым раствором внедрения является раствор углерода в железе
- различные композиции чугуна и из легированной стали - это твердые растворы
внедрения.

Рис.1. Диаграмма
состояния системы с неограниченной растворимостью компонентов А и В в жидком и
твердом состояниях: 1 - линия ликвидуса; 2 - линия солидуса
В твердых растворах вычитания, которые образуются сравнительно редко, происходит
"выпадение" атомов из кристаллической решетки. Такие системы иногда
называют твердыми растворами с дефектами решетки.
Взаимная растворимость компонентов в твердом растворе может быть
либо неограниченной (непрерывные твердые растворы либо ограниченной (твердые
растворы с разрывом сплошности). Наиболее распространенными являются
твердые растворы с ограниченной растворимостью.
Твердые растворы широко распространены среди природных и
искусственно получаемых веществ. Важнейшие природно-образующиеся минералы
(слюда, полевые шпаты, роговые обманки и др.) являются твердыми растворами. К
искусственным твердым растворам относятся сплавы, керамика, ферриты и др.
Твердыми растворами являются и конструкционные, и нержавеющие стали, чугун,
латунь и др. Из неметаллических растворов следует упомянуть стекло.
Наиболее распространенным способом получения твердых растворов
является затвердевание расплавов или жидких растворов разнородных компонентов.
Кроме того, твердые растворы образуются при диффузии компонентов, находящихся в
твердой смеси при повышенной температуре, а также вследствие конденсации
газообразных веществ.
В зависимости от растворимости компонентов раствора различают
системы, компоненты которых взаимно неограниченно растворимы в жидком и твердом
состоянии, и системы, компоненты которых растворимы лишь в жидком состоянии, а
в твердом состоянии не образуют растворы. Это так называемые растворы с
эвтектикой.
Диаграмма состояния системы с неограниченной растворимостью двух
компонентов в жидком и твердом состояниях приведена на рис.1. На оси абсцисс
отложены мольные доли компонентов раствора А и В (Nа, Nb). (Часто вместо мольных долей состав твердых растворов
выражают при помощи массовой доли или процентного содержания.) По оси ординат
отложена температура системы. Для чистых компонентов системы температура
плавления компонента В превышает температуру плавления компонента А, т.е. t пл B > t пл A -
компонент В является более тугоплавким по сравнению с компонентом а.
В зависимости от фазового состава следует различать три области: I - жидкий раствор (расплав); II - равновесное сосуществование жидкого и твердого растворов; III - твердый раствор.
Кривую 1, определяющую начало перехода жидкого раствора в
твердый, называют линией ликвидуса, или просто ликвидус (от
латинского слова liquor - жидкость). Кривая 2, которая
характеризует переход всей системы в состояние твёрдого раствора, называют линией
солидуса, или просто солидус (от латинского слова solid - твердый).
Для систем, компоненты которых представляют конденсированные фазы
(жидкие или твердые растворы), число внешних условий, определяющих состояние и
вид системы, снижается на единицу - давление не оказывает практического влияния
на состояние системы. Поэтому для определения числа степеней свободы следует
воспользоваться формулой: С= К - Ф + 1. В областях I и III система
является гомогенной, состоит из одной фазы, и число степеней свободы равно двум
(С = 2 - 1 + 1 = 2), а в области II - единице (С
= 2 - 2 + 1 = 1). Если число степеней свободы равно единице, то каждой
температуре соответствует определенный состав жидкого и твердого растворов.

По правилу рычага отношение между числом молей компонентов в
жидкой nж и твердой nж фазах обратно пропорционально длине отрезков, лежащих на прямой,
параллельной оси абсцисс между линиями ликвидуса и солидуса.
2.2 Растворы
с эвтектикой
При отверждении расплава, который состоит
по крайней мере из двух компонентов и является жидким раствором, не обязательно
образуются твердые растворы. Диаграмма состояния системы, жидкая фаза которой
образует раствор, а твердая - не образует, представлена на рис.2.

Рис.2. Диаграмма состояния
системы с эвтектикой, образующей жидкие и не образующей твердые растворы: 1
- линия ликвидуса; 2 - линия солидуса (эвтектическая прямая)
Следует различать четыре области: I -
жидкий раствор; II - жидкий раствор компонентов А и В и твердых кристаллов
вещества А; // / - жидкий раствор компонентов А и В и кристаллов вещества В; IV
- два твердых компонента А и В, не образующие твердый раствор.

Линия ликвидуса (кривая 1) характеризует переход жидкой фазы в
твердую. Температура плавления компонентов А и В равна соответственно tплА и t пл В. Отрезок tплА - Э линии ликвидуса соответствует составу системы, когда начинается
выпадение кристаллов твердого вещества А в растворе (расплаве), содержащем
вещества А и В, т.е. началу образования двухфазной системы, а отрезок Э - t пл В началу выпадения кристаллов вещества В.
Линия солидуса (прямая 2) характеризует переход жидкой фазы в
твердую и образование системы из двух твердых компонентов, не образующих
твердый раствор. Линия солидуса в этих диаграммах выполняет роль эвтектической
прямой.
Разберем более подробно фазовое состояние системы и число степеней
свободы в четырех областях на основании правила фаз Гиббса для конденсированных
систем.
В области I система образует жидкий раствор и число степеней
свободы равно двум [С=К-Ф+1 = 2-1 + 1 = 2], т.е. можно произвольно в
определенных пределах изменять температуру и состав системы, не изменяя числа и
вида фаз.
В области II система
двухфазная, состоящая из раствора компонентов А и В и твердых кристаллов
компонента А. Число степеней свободы равно единице [С = 2 - 2 + 1 = 1], т.е.
можно изменять в пределах этой области лишь температуру, а состав при данной
температуре определяется отрезком линии ликвидуса (отрезок tплА - Э).
В области III так же, как и в области II, число степеней свободы равно единице, так как система
двухфазная, а ее состав зафиксирован отрезком Э - t пл В линии ликвидуса.
В области IV система состоит из двух фаз, а число степеней свободы
становится равным единице. Это дает возможность произвольно изменять
температуру, а состав фаз перестает быть переменным, поскольку всегда система
состоит из двух чистых твердых веществ А и В.
Точка Э - эвтектическая точка; она соответствует такому составу
системы, когда в равновесии находятся жидкие компоненты системы, образующие
расплав, с твердыми кристаллами компонента А и компонента В. Число фаз равно
трем, а число степеней свободы равно нулю [С=2-3 + 1 = 0]. Образуется
безвариантная трехфазная система, в которой нельзя менять ни температуру, ни
состав системы. Три фазы могут находиться в равновесии только в том случае,
когда температура системы равна эвтектической, и система имеет эвтектический
состав, определяемый точкой Э на диаграмме рис.2.
Процесс перехода расплава в твердое состояние происходит в
интервале температур от tл до tc, который сокращается по мере приближения
состава системы к эвтектическому. Только при эвтектическом составе,
соответствующем точке Э рис.2, наблюдается отверждение раствора при
определенной фиксированной температуре tс без
температурного интервала.
Наиболее распространенным и доступным методом исследования
фазового состояния системы и построения диаграмм состояния является термический
анализ. Этот метод основан на изменении температуры при охлаждении (или
нагревании) системы с течением времени. В системах, компоненты которых
прозрачны, термический анализ основан на визуальном (зрительном) наблюдении за
расплавом при медленном остывании (реже при медленном нагревании).
2.3 Растворы
газов в жидкостях
Газы могут растворяться в жидкостях,
образуя жидкие растворы. В связи с незначительной растворимостью газов их
растворы можно отнести к разбавленным. Количественно растворение газов в
жидкостях можно выразить различным способом: при помощи мольной доли
растворенного газа Nг или концентрации, а также при помощи коэффициента растворимости.
Коэффициент растворимости равен отношению объема растворенного газа Vг [л или м3], приведенного
к давлению 1,013*105 Па (1 атм), к объему растворителя Vp [л или м3]:

Коэффициент растворимости зависит от
температуры.
Коэффициент растворимости (а
следовательно, и растворимость газов) уменьшается с ростом температуры и
изменяется в довольно широких пределах, что объясняется различием в механизмах
растворения разных газов.
Растворение газа в жидкости происходит
либо в результате межмолекулярного взаимодействия молекул газа и жидкости, либо
является следствием химической реакции между молекулами растворителя и
растворенного вещества.
Кислород растворяется в воде в результате
межмолекулярного взаимодействия, что объясняет его относительно плохую
растворимость в воде. Подобная незначительная растворимость в воде характерна
для многих, в том числе и благородных, газов (Не, Ne, H2, СН4 и др.).
А высокая растворимость некоторых газов в
воде объясняется химическим взаимодействием; для аммиака это взаимодействие
происходит следующим образом: NНз + H2O  NH+4 +
ОН-.
NH+4 +
ОН-.
Растворению диоксида углерода (СО2)
способствует межмолекулярное взаимодействие в сочетании с химической реакцией,
приводящей к образованию угольной кислоты (СО2 + Н2О  H2CO3).
H2CO3).
Растворимость газов зависит не только от
природы растворяемого вещества, но и от свойств растворителя. Так,
растворимость азота в этаноле и ацетоне почти в 10 раз превышает его
растворимость в воде.
Равновесие в системе жидкость-газ
динамическое: какое-то количество молекул газа испаряется из раствора, такое же
количество растворяется. При установлении подобного равновесия при определенных
температуре и давлении жидкость насыщена газом. Растворимость газа в жидкости
прямо пропорциональна парциальному давлению газа над поверхностью жидкости pг. В соответствии с
законом Генри для разбавленных растворов, к которым относятся растворы газов,
можно записать
 ,
,
где kт - коэффициент
пропорциональности, или константа Генри, в данном случае для растворов газов; Nг
- мольная доля растворенного газа.
Константа Генри измеряется в Па и так же,
как и коэффициент растворимости, определяет содержание газа в растворе.
Обратим внимание на то, что константа
Генри постоянна при данной температуре, а при изменении температуры ее значение
изменяется.
Выражение для определения мольной доли
растворенного газа:

Две формулировки закона Генри
применительно к раствору газов в жидкостях:
) парциальное давление газа над
поверхностью его раствора прямо пропорционально мольной доле растворенного
газа.2) мольная доля растворенного газа (или концентрация растворенного газа)
пропорциональна парциальному давлению газа над раствором. Согласно закону
Генри, с увеличением давления растут растворимость и концентрация растворенного
газа. Закон Генри справедлив для сильно разбавленных растворов газов, близких к
идеальным. Так, при растворении даже таких плохо растворимых в воде газов, как
аргон, закон Генри остается справедливым для относительно низких температур и
давлений до 5 атм.
В области высоких давлений и сравнительно
больших концентраций закон Генри можно выразить следующим образом:
 ,
,
Растворимость газов снижается в
присутствии электролитов, что объясняется процессом сольватации. Молекулы
растворителя прочнее связываются с ионами электролитов, нежели с растворенными
молекулами газа; значительная часть молекул растворителя используется для
создания сольватной оболочки и выключается из участия в растворении газов.
Количественно снижение растворимости газов
в присутствии электролитов определяется выражением:
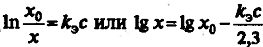 ,
,
где хо и х - растворимости газа
в воде и растворе электролита, выраженные в одних и тех же единицах; kэ - эмпирический
коэффициент, зависящий от природы газа и электролита, а также от температуры; с
- концентрация электролита.
Снижение растворимости газа в присутствии
солей и выделение при этом пузырьков газа называют высаливанием. Примером
высаливания служит выделение пузырьков газа при добавлении в пиво щепотки соли.
В отличие от жидких
растворов растворимость газов снижается при нагревании и увеличивается при
охлаждении.
Причину изменения растворимости газов в
зависимости от температуры можно уяснить, если обратиться к уравнению
Клаузиуса-Клапейрона:
 ,
,
где 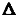 Нр - тепловой
эффект процесса растворения газа в жидкости.
Нр - тепловой
эффект процесса растворения газа в жидкости.
раствор эвтектика газ жидкость
Следует отметить, что фазовое равновесие
между газом и жидкостью существует в ограниченной области температур и
давлений.
2.4
Трехкомпонентные системы. Экстракция
Состав двухкомпонентных систем описывается
диаграммами состава (рис.1 и 2) и определяется значениями мольных долей
компонентов, отлагаемых на оси абсцисс. Состав трехкомпонентной системы
изображают в виде графиков. Наиболее распространенный из них - равносторонний
треугольник (рис.3).

Рис.3. Графическое изображение состава трехкомпонентной системы
Каждая сторона этого треугольника отражает состав двухкомпонентной
системы аналогично оси абсцисс рис.1 и 2. Любая точка внутри треугольника
характеризует состав трехкомпонентной системы, и наоборот, определенному
составу системы соответствует одна точка внутри треугольника.
Рассмотрим в качестве примера состав системы в точке Р. Для этой
цели из точки Р проведем три прямые, параллельные сторонам треугольника. Эти
прямые на сторонах треугольника будут отсекать отрезки, длина которых в
соответствии с принятым масштабом определяет содержание каждого компонента. В
соответствии с рис.3 NА = 0,4; NВ = 0,2 и NС =
0,4 или в процентах 40,20 и 40%.
Третий компонент D может быть введен в двухкомпонентную систему из
двух несмешивающихся жидкостей А и В. Когда вводится относительно небольшое
количество третьего компонента и он распределяется в обеих фазах одинаково, а
диссоциации и ассоциации молекул не происходит, то третий компонент
распределяется в двух жидких фазах в определенной пропорции, т.е.
 ,
,
где  ,
,  - концентрации компонента D в жидкости А и В соответственно.
- концентрации компонента D в жидкости А и В соответственно.
Уравнение отражает закон распределения, который можно
сформулировать следующим образом: отношение концентраций третьего компонента
в двух равновесных жидких фазах является величиной постоянной при данной
температуре и не зависит от концентрации вводимого компонента.
Постоянную kр в уравнении называют коэффициентом
распределения.
В случае диссоциации (распада молекул) или ассоциации (образования
ассоциатов из молекул) размеры частиц в разных растворителях будут различными.
В подобных случаях - уравнение теряет смысл, и можно воспользоваться более
общим выражением для коэффициента распределения:
 ,
,
где n - постоянная для данного растворителя.
После логарифмирования уравнения получим:

Закон распределения в логарифмической форме позволяет по известным
значениям  и
и  графическим путем определить lgkp и n.
графическим путем определить lgkp и n.
В производстве часто возникает необходимость извлечь вещество из
раствора, удалить из него примеси или повысить концентрацию растворенного вещества.
В этих случаях прибегают к экстракции.
Экстракцией называют извлечение из многокомпонентного раствора
одного или нескольких компонентов с помощью растворителя, обладающего
избирательной способностью растворять только подлежащие экстрагированию компоненты.
Экстракцию широко применяют в промышленности, в том числе и
пищевой. При помощи экстракции происходит извлечение необходимых веществ:
сахара из свеклы, растительного масла из семечек и др.
На основе закона распределения можно рассчитать эффективность
экстракции в зависимости от свойств растворителя и экстрагируемого вещества.
Коэффициент распределения характеризует возможность выделения растворенного
вещества.
Коэффициент распределения будет равен:  , где с1 - концентрация
вещества, оставшегося в системе после первой экстракции; с2 -
концентрация вещества, удаляемого из системы в результате экстракции.
, где с1 - концентрация
вещества, оставшегося в системе после первой экстракции; с2 -
концентрация вещества, удаляемого из системы в результате экстракции.
Концентрации с1 и с2 можно выразить
следующим образом:
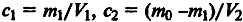 ,
,
где mo, m1 - массы экстрагируемого вещества
до и после экстракции; mo - m1 - масса вещества,
удаляемого в результате первой экстракции; V1, V2 - объем
растора, подвергшегося экстракции, и объем растворителя, используемого для
экстракции.
Подставляя в уравнение значения концентраций:

Для более полного извлечения экстрагируемого вещества при
ограниченном объеме растворителя экстракцию следует проводить не сразу всем
количеством растворителя, а несколькими малыми порциями примерно одного и того
же объема.
Список
использованной литературы
1.
Зимон А.Д. Физическая химия: Учебник для вузов
.
Физическая химия. Теоретическое и практическое руководство. Под ред.
Никольского Б. П.