Активированные кислородные метаболиты в биологических системах
Оглавление
Введение
Активированные
кислородные метаболиты в биологических системах. Антиоксиданты и ингибиторы
радикальных и окислительных процессов. Перекисное окисление липидов
Активированные
кислородные метаболиты. Общие сведения
Классификация
АКМ
Биологическая
роль АКМ
Антиоксиданты
Общие
сведения
Витамин С
Каротиноиды
Витамин Е
Селен
Глутатионпероксидаза
Перекисное
окисление липидов
Материалы и
методы
Общие
сведения
Выделение
микросом печени крысы
Исследование
индукции ПОЛ
Определение
концентрации белка по методу Бредфорда
Результаты и
обсуждение
Выводы
Список
литературы
Введение
Кислород является самым распространённым химическим элементом биосферы,
его соединения в состав всех живых организмов на планете. Наиболее широко
представлена восстановленная форма кислорода, или вода (H2O); для
высших форм жизни необычайно важен молекулярный кислород (O2),
реакция восстановления которого до H2O составляет основу
биоэнергетики организма человека и животных [1].
Около 90% потребляемого человеком молекулярного кислорода вовлекается в
реакции окислительного фосфорилирования, вместе с тем во всех живых организмах
постоянно протекают реакции с образованием активированных кислородных
метаболитов (АКМ): O¯2, 1O2, H2O2,
HO●, OCl¯, RO2 и др. Многие из этих
соединений являются радикалами, то есть имеют неспаренный электрон, поэтому
часто их называют свободными радикалами. Связанные радикалы, такие как
компоненты цепи транспорта электронов в митохондриях, также широко представлены
в клетках, однако их локализация в определённых структурах ограничивает
«свободное» взаимодействие с другими молекулами [2]. По оценке Гельмута
Эстербауэра, человек за 70 лет жизни потребляет 17 000 кг кислорода; за это
время в организме нарабатывается 800-1700 кг кислородных радикалов. АКМ, образующиеся
в процессе нормальной жизнедеятельности животной клетки, индуцируют в ДНК около
10 000 повреждений за сутки [3]. При этом генерация АКМ, очевидно, есть не
эволюционная ошибка (неудача), а, напротив, - характерный физиологический
процесс, результат революционного отбора [4].
Образование АКМ, известных как прооксиданты, наблюдается во многих
метаболических процессах и является обязательным атрибутом нормальной аэробной
жизни. Функционирование и развитие клеток, и организма в целом, в
кислородосодержащем окружении не могло бы быть возможным без существования
защитных систем, основу которых составляет ферментативные и неферментативные
антиоксиданты. Постоянное образование прооксидантов в живых организмах
уравновешено их дезактивацией антиоксидантами, поэтому для поддержания
гомеостаза необходима непрерывная регенерация антиоксидантной способности.
Отсутствие или сбои этой непрерывности сопровождаются накоплением окислительных
повреждений и приводят к возникновению окислительного стресса, который является
составным элементом целого ряда патологических процессов и заболеваний, таких
как воспаление, реперфузионное поражение тканей, бронхолёгочные заболевания,
старение, канцерогенез и др. [5][6].
Важную роль в антиоксидантной системе играет селен. Хотя сам по себе
селен и не является «прямым» антиоксидантом, он принимает активнейшее участие в
процессе синтеза фермента глутатионпероксидазы - мощнейшего антиоксидантного
вещества, предохраняющего клеточные мембраны от разрушительного воздействия
свободных радикалов. Без достаточного содержания селена этот важнейший фермент
просто не будет образовываться.
В качестве антиоксиданта и детоксикатора ядовитых веществ селен защищает
организм от сердечных заболеваний, усиливает иммунитет, увеличивает
продолжительность жизни. Действуя совместно с другими антиоксидантами -
витаминами Е и С, селен помогает улучшить мыслительные способности, снижает
депрессию, прогоняет усталость [7].
антиоксидант окислительный липид биологический
Активированные кислородные метаболиты в биологических
системах. Антиоксиданты и ингибиторы радикальных и окислительных процессов.
Перекисное окисление липидов
Активированные кислородные метаболиты. Общие сведения
АКМ - высокореакционные, преимущественно радикальные, кислородные
соединения, образующиеся в живых организмах в результате неполного
восстановления молекулярного кислорода или изменении спина одного из его
электронов, находящихся на внешних орбиталях.
Применительно к биологическим системам понятия «свободные радикалы» и
«АКМ» не совпадают - неспаренный электрон может быть локализован на атомах
углерода, серы, азота; так, для живых организмов важное значение имеют тиильные
радикалы глутатиона (GS●) или радикалы мочевой кислоты с
локализацией электрона на атомах Sи N. С другой стороны, такие
кислородсодержащие молекулы, как перекись водорода, синглетный кислород,
гипогалогениты не являются радикалами, хотя и взаимодействуют с органическими
молекулами через радикальные механизмы. Чтобы объединить данные соединения в
одну группу с радикалами, вводят понятие «активные формы кислорода» или
«активные метаболиты кислорода», которыми обозначают ферментативные продукты
активации кислорода. По аналогии с активными формами кислорода иногда говорят
об активных формах азота, обозначая так продукты преобразования NO-радикалов
(NO●, NO+, NO¯, NO2, ONOOH), активных
формах галогенов (HOCl, OCl¯,HOBr, HOI), активных формах липидов
(L●, LO●, LO2●,
LOOH) [5]. В биологическом плане наиболее удачно понятие «активированные
кислородные метаболиты», под которым подразумевается широкий класс кислородных
соединений радикальной и нерадикальной природы.
В живых организмах существуют два принципиально разных источника АКМ:
радикальные окислительные реакции и металлопротеиновые ферментативные системы.
В обоих случаях молекулярный кислород выступает акцептором электронов, а
появление АКМ является результатом неполного восстановления молекулы O2[7].
Классификация АКМ
Первоначально все радикалы, образующиеся в живом организме, было принято
делить на свободные, которые легко мигрируют в водных или липидных средах, и
связанные, структурно закреплённые и участвуюшие в цепях переноса электронов.
Такое деление достаточно условно, в частности, непонятно, к свободным или
связанным относятся в таком случаем убисемихинонные радикалы, которые
достаточно легко перемещаются в липидных мембранах.
Введённые в последующем понятия «активные формы кислорода и азота»,
«активные формы хлора», «активные формы липидов» отражали желание
исследователей строго определить и классифицировать весьма разнородный класс
соединений, объединённых нами под общим названием активированных кислородных
метаболитов (АКМ).Сегодня наиболее удачная классификация таких соединений
предложена Ю. А. Владимировым[8], согласно которой все образующиеся в организме
АКМ в зависимости от происхождения могут быть разделены на первичные, вторичные
и третичные; среди причин появления чужеродных форм АКМ также можно выделить 3
основных фактора: радиация, оптические излучения и ксенобиотики (см. табл. 1).
Деление АКМ наприродные и чужеродные оправдано с позиций их биологической
значимости. Действительно, основной функцией природных форм АКМ является
регуляторная, затем защитная, в определённых ситуациях, как правило,
патологических, они могут становиться токсичными и индуцировать развитие
деструктивных процессов, однако такие ситуации являются исключением, а не
правилом. Образующиеся при действии радиации или в процессе фотодинамической
терапии чужеродные формы АКМ, также как радикалы, возникающие в процессе метаболизма ксенобиотиков, обладают выраженным
цитотоксическим и деструктивным действием [7].
Таблица 1

Иногда в целях регуляторного воздействия применяются доноры NO●;
попытки усилить защитные функции организма посредством индукции образования АКМ
сегодня носят достаточно экзотический характер.
Первичные формы АКМ или радикалов образуются с участием
специализированных молекулярных механизмов, таких как мембранные НАДФН-оксидазы
(восстанавливают O2 в O2¯), NO-синтазы (продуцируют NO●)
или фотосенсибилизированные процессы, являющиеся основными источниками 1O2.
Как правило, эти продукты ферментативного восстановления O2 или его
активации, количество весьма ограничено: O2¯, H2O2, ОH●,
NO●, 1O2. Строение и заполнение
молекулярных орбиталей O2подчиняются квантовым законам, что
существенно ограничивает количество образующихся продуктов. Первичные АКМ
инициируют образование в реакциях свободнорадикального окисления большего числа
вторичных радикалов липидов, белков, сахаров, нуклеиновых кислот, многие из
которых более токсичны [8]. Деление на первичные и вторичные АКМ или радикалы вполне
оправдано, так как позволяет при патологических процессах выделить главные
молекулярные механизмы генерации АКМ. Однако, как и в случае с многими другими
понятиями свободнорадикальной биологии, дать строгие определения первичных,
вторичных и третичных радикалов сложно, так же как сложно точно определить
понятие антиоксиданта [7].
Биологическая роль АКМ
Общая особенность АКМ - высокая реакционная способность и малые значения
времён жизни в биологических субстратах, что делает их эффективным инструментом
локального действия [9]. Так, действие OH-радикала (радиус диффузии 23 Å) [10]ограничено размером средней
ограниченной молекулы (например, величина молекулы пепсина - молекулярная масса
35 кДа - составляет 37 × 74 Å). Анион-радикал O2¯ и синглетный кислород обладают
большим радиусом действия, сравнимым с размером клетки, однако уже на клеточном
уровне их эффект строго локализован наличием высокоэффективного ферментативного
антиоксиданта - супероксиддисмутаза (СОД), а также других антиоксидантов - таких,
как витамин E, который инактивирует 1O2 посредством
физического взаимодействия на расстоянии ~ 50 Å [11]. Сфера влияния радикалов NO●
распространяется уже на определённые клеточные структуры, такие как
мышечные клетки сосудов, что вызывает их релаксацию, при этом оксид азота
принципиально не отличается от гормональных мессенджеров и имеет свой
«рецептор» - растворимую гуанилатциклазу. Наибольшим дальнодействием,
проявляющимся на тканевом и организменном уровнях, обладают продукты
радикальных реакций; так, процессы ПОЛ приводят к образованию альдегидов,
эпоксидов, липидных перекисей, которые ингибируют синтез ДНК и деление клеток и
в то же время индуцируют развитие опухоли. По-видимому, ПОЛ и его продукты,
выступая в роли «первичного медиатора» стресса или «SOS-ответа», представляют
один из наиболее ранних регуляторных механизмов, который в процессе эволюции
трансформировался в ферментативную эйкозаноидную регуляцию. Окисленные
фосфолипиды по свойствам сходны с фактором активации тромбоцитов и могут имитировать
действие цикотина на клетки непосредственно через специфический для него
рецептор.
Высокая реакционная способность АКМ делает их чрезвычайно токсичными для
биологических систем на всех уровнях - от молекулярно-клеточного до
организменного. В конце 40-х годов толчком для широкого изучения токсических
эффектов АКМ послужили исследования действия радиации на живые организмы. В
настоящее время можно утверждать, что АКМ занимают ведущее место в патогенезе
радиационного поражения; деструкции тканей, вызванной развитием воспалительной
реакции, и связанного с хроническим воспалением опухолеобразования;
постишемических, реперфузионных и гипероксических повреждений; а также целого
ряда бронхолёгочных, сердечнососудистых и других заболеваний. Вместе с тем
механизм патофизиологического действия АКМ во многих случаях не ясен, так как
утверждение о патофизиологической роли АКМ обычно строится на двух косвенных
аргументах: а) интенсивность продукции АКМ коррелируют с развитием
патологического процесса; б) ингибиторы АКМ обладают защитным действием.
Открытие явления дыхательного «взрыва» в фагоцитах послужило началом
широкого изучения микробицидного действия АКМ, их роли в защите организма. При
этом ярко выявилось, что генетически обусловленные нарушения механизмов генерации
АКМ (больные с хронических гранулематозом или дефицитом миелопероксидазы) или
их ингибирование лекарственным препаратами приводит к снижению неспецифического
иммунитета и является причиной либо гибели организма от инфекций, либо развития
хронических патологий.
В последние годы выявлен широкий спектр физиологических эффектов АКМ, к
которым прежде всего относятся регуляция клеточной пролиферации и тонуса
сосудов, индукция транскрипции определённых генов [12]. Показано
функционирование АКМ в качестве вторичных внутриклеточных мессенджеров. Так,
АКМ непосредственно участвуют в активации онкогенов c-focи с-myc, а также гена
c-jun, кодирующего главную форму фактора транскрипции AP-1, в ответ на
ионизирующую радиацию [13].O2¯и H2O2
активируют фактор транскрипции NF-кB, который вызывает экспрессию генов,
кодирующих ряд цитокинов и вирусов, в том числе ВИЧ, а NO●подавляет
активацию NF-кB, индуцируя экспрессию ингибитора фактора транскрипции IкBαи стабилизируя его. Стимуляция
НАДФН-оксидазы нейтрофилов сопровождается активацией тирозинкиназ, при этом
повышение накопления фосфотирозина обусловлено не только активацией АКМ
фосфорилирования тирозина, но и ингибированием дефосфорилирования. В индукции
синтеза белков теплового шока, повышающих резистентность клеток к высоким
температурам, радиации, токсическому действию ионов тяжёлых металлов и
лекарственных препаратов, основная роль отводится перекиси водорода.
Выделяемая из облучённых фоторецепторов H2O2 увеличивают
длину и количество микроворсинок клеток пигментированного эпителия, что
способствует более тесному контакту этих двух типов клеток и реализации
антиоксидантных функций эпителия. NO●и CO●
связываются с гемовой частью гуанилатцитклазы и обратимо изменяют синтез цГМФ,
являясь важным компонентом внутри- и внеклеточной коммуникации. NO●
участвует в посттранскрипционном контроле метаболизма железа [14].
Таким образом, образование АКМ в организме нельзя рассматривать, как
существующий, но не обязательный элемент процесса жизнедеятельности.
Окислительные процессы с участием АКМ является неотъемлемым звеном
существования высших форм живых организмов, негэнтропийное состояние которых
поддерживается посредством снижения электронной упорядоченности молекулярного
кислорода в результате его восстановления. Однако многие вопросы регуляторной
функции АКМ, их взаимодействия с антиоксидантами, физиологической и
патофизиологической роли сегодня всё ещё остаются спорными [7].
Антиоксиданты
Антиоксидант - это любое вещество, которое, присутствуя в низких по
сравнению с окисляемым субстратом концентрациях, существенно задерживает или
ингибирует его окисление [15].
По химической природе биоантиокислители представляю собой широкий класс
соединений: ферменты (СОД, каталаза ГПО), фенолы и полифенолы (токоферолы,
эвгенол, конидендрин, пирокатехин, производные галловой кислоты), флавоноиды
(рутин, кверцетин), стероидные гормоны (лецитин, кефалин) и многие другие
соединения. В зависимости от растворимости различают жирорастворимые (витамины
E, A, K, стерины, убихинон) и водорастворимые (витамины С, B6, PP,
серотонин, SH-содержащие соединения) биоантиокислители [16], по молекулярной
массе выделяют группу низкомолекулярных антиоксидантов (глутатион, аскорбат, β-каротин, α-токоферол, мочевая кислота) и
высокомолекулярных, не способных проникать через биологические барьеры
(ферритин, каталаза, пероксидазы и др.) [17].
По принципу антиокислительного действия в биологических системах все
антиоксиданты могут быть разделены на антиоксиданты косвенного
(опосредованного) действия и антиоксиданты прямого (направленного) действия.
Такое деление удобно при рассмотрении патологических процессов,
сопровождающихся развитием окислительного стресса, в этом случае все
соединения, повышающие синтез эндогенных антиоксидантов, нормализующие
метаболические процессы и стабилизирующие клеточные структуры, могут быть
отнесены к антиоксидантам косвенного действия. Естественно, что эффективность
антиоксидантов косвенного действия проявляется только в живых системах.
Соединения, непосредственного подавляющие окислительные процессы с участием АКМ
invitroиinvivo можно рассматривать как антиоксиданты прямого действия. В
зависимости от точки приложения действие антиоксиданта может осуществляться
посредством одного или нескольких механизмов:: ингибирование радикальных форм АКМ,
способных отрывать атом водорода с образованием органических радикалов;:
изменение структурной организации, затрудняющее окисление;: локальное снижение
концентрации и предотвращение его включения в окисление;: взаимодействие с
органическими радикалами и предотвращение развития ценных окислительных
процессов;: связывание или окисление ионов металлов переменной валентности,
индуцирующих разложение перекисей и образование радикалов;: перевод перекисей в
стабильные продукты окисления: спирты альдегиды, кетоны.
Соединения, реализующие свой антиоксидантный эффект посредством
механизмов II, III, V, VI, иногда называются превентивными антиоксидантами, в
то время как пути Iи IV характерны для ингибиторов АКМ, действие которых в
достаточной степени специфично [7].
По мере развития наших знаний об окислительных процессах с участием АКМ
изменяется и представление об антиоксидантных механизмах защиты. До недавнего
времени рассматривалась преимущественно патогенная функция АКМ, реализующаяся
посредством активации процессов ПОЛ в биомембранах; при этом считалось, что как
в норме, так и при патологических процессах необходимо ингибировать наработку
АКМ и снижать активность ПОЛ[16]. Исследования последних лет выявили участие
АКМ в регуляции тонуса сосудов, клеточной пролиферации, синтеза
простагландинов, в микробицидном действии фагоцитов, в регуляции метаболических
процессов в качестве внутриклеточных мессенджеров [18]. При этом поднимается
вопрос о целесообразности в определённых ситуациях ингибирования наработки АКМ,
что имеет важное практическое значение, так как с позиций существующих
представлений сложно объяснить лечебный эффект введения перекиси водорода в
низких концентрациях или аутотрансфузии УФ-облучённой крови. Применение
антиоксидантных витаминов (Е, С) и β-каротина в целях профилактики
заболеваний в последние годы также ставится под сомнение [7].
Необходимо отметить, что понятия «антиоксидант» и «антиоксидантная
защита» имеют очень размытый характер; перефразируя Германа Мелвилла, подробная
систематизация антиоксидантных соединений равносильна попытке классифицировать
составляющие мирового хаоса. Так, антиоксидантами можно назвать все вещества,
снижающие активность ферментативных реакций наработки АКМ (например,
аллопуринол), а также многие противовоспалительные препараты, ингибирующие
развитие метаболического «взрыва» в фагоцитирующих клетках. Иногда вводится
понятие «вторичная антиоксидантная система», которым обозначают
специализированные ферментативные механизмы устранения окислительных
повреждений в клетках, такие протеиназы, фосфолипазы, экзо- и эндонуклеазы и
др. Своевременное удаление повреждённых молекул повышает устойчивость клеток к
токсическому действию АКМ, и поэтому с позиций биологической системы и
биологической значимости радикальных окислительных процессов такие
ферментативные системы могут рассматриваться как антиоксиданты[7].
Рассмотрим основные антиоксиданты и их механизм действия.
Витамин С
Аскорбиновая кислота (витамин С; γ-лактон 2,3-дегидро-L-гулоновой
кислоты; 2-оксо-L-треогексо-1,4-лактон-2,3-ендиол) была впервые выделена в 1928
г. Альбертом Сент-Дьёрдьи. Её биосинтез происходит главным образом из
углеводов: из галактозы либо из глюкозы. Она очень нестабильна и легко
разрушается при нагревании в щелочных условиях, а также под действием кислорода
в присутствии ионов металлов переменной валентности, катализирующих её
окисление с образованием неактивных продуктов.
Аскорбиновая кислота - наиболее важный антиоксидант плазмы человека, где
её содержание в норме составляет 20-60 мкМ; после курса приёма витамина С его
уровень возрастает до 100-200 мкМ.
В биологических средах аскорбиновая кислота обладает чрезвычайно широким
спектром антиоксидантных свойств; в число обезвреживаемых ею АКМ входят HOCl
(что при ревматоидном артрите особенно важно для синовальной жидкости, где мала
концентрация эффективного плазменного ингибитора HOClальбумина[15]), радикалы O2●¯, HO2●,
RO2● и HO●, синглетный кислород и
др.
В клетках АК может также восстанавливать тиильный (GS●)
и тиопероксильный (GSO2●) радикалы глутатиона.
Помимо прямого антиоксидантного действия витамин С инициирует включение железа
плазмы в состав тканевого ферритина, что приводит к снижению содержания
свободных ионов железа [7].
В экспериментальных исследованиях было показано, что аскорбиновая кислота
может восстанавливать α-токоферильный радикал, тем самым возвращая α-токоферолу антиоксидантные свойства
[19].
В присутствии Fe3+или Сu+аскорбат становится мощным
прооксидантом (также это зависит от концентрации субстрата и условий протекания
окислительных реакций).В качестве стабилизатора аскорбиновый кислоты может
выступать мочевая кислота, которая ингибирует радикалы аскорбата и
предотвращает его окисление железом [20].
Каротиноиды
Из натуральных продуктов выделено и охарактеризовано более 600 различных
каротиноидов, среди которых наиболее изученными и часто встречающимися являются
ликопин, α-, β-, γ- каротины. Каротиноиды относятся к
группе жирорастворимых растительных пигментов.
Наличие обобщённой системы π-электронов в молекулах каротиноидов
приводит к низким значениям электронно-возбуждённых состояний молекул и служит
причиной, что данные соединения могут легко окисляться и восстанавливаться с
образованием радикалов. Показано, что каротиноиды - эффективные антиоксиданты,
действующие в отношении алкоксильных и перекисных радикалов, синглетного
кислорода, NO-радикалов и пероксинитрита [21].
Полиеновые углеводороды, и прежде всего каротиноиды, являются наиболее
эффективными природными тушителями синглетного кислорода: константы скоростей
взаимодействия основных каротиноидов с 1O2 находятся в
пределах 109-1010 М-1 с-1.
Константа скорости взаимодействия β-каротина с 1O2 составляет
14 ×
109 М-1 с-1, при
этом одна молекула β-каротина вызывает конверсию 200-1000 молекул 1O2,
что можно объяснить физическим механизмом тушения посредством переноса энергии
на триплетный уровень β-каротина, который находится на 22 ккал/моль ниже
уровня синглетного кислорода:
1O2
+ β-каротин → O2 + 3(β-каротин).
Такое свойство β-каротина делает его эффективным антиоксидантом в различных
фотоиндуцированных процессах, сопровождающихся образованием 1O2,
вместе с тем эффективность каротинов незначительна при окислении, вызванном H2O2и
ионами металлов переменной валентности. Анализ ингибирования 1O2
разными по строению соединениями каротиноидной природы показал, что
эффективность ингибирования возрастает с увеличением количества сопряжённых
двойных С-С связей, наличие эпоксидной группы в наибольшей степени повышало
эффективность по сравнению с карбонильными или гидроксильными заместителями
[7].
β-каротин может участвовать в
регенерации токоферильного радикала с образованием катион-радикала β-каротина, как это следует из реакции:
α-ТфО● + H+
+ β-каротин → α-ТфОН + β-каротин●+.
Учитывая, что β-каротин представляет собой полиненасыщенное соединение,
он сам может легко окисляться по радикальному механизму и выступать в качестве
прооксиданта - индуктора свободнорадикальных реакций, особенно при увеличении
его концентрации или pO2в клетках. Антиоксидантные свойства β-каротина сильно зависят от содержания
кислорода: при низких pO2 (меньше 150 мм рт. ст.) он проявляет
высокую антирадикальную активность, в то время как при высоких парцеальных
давлениях (≈ 760 мм. рт. ст.) кислорода становится прооксидантом [22].
Витамин Е
Витамин Е (α-токоферол) как жирорастворимый фактор, необходимый
для размножения крыс и содержащийся в высоких концентрациях в масле из
проростков пшеницы и семян салата, был открыт в 1922 г. американскими учёными
Гербертом М. Эвансом и Кэтрин С. Бишоп.
Соединения, родственные витамину Е (витамеры), представляю собой группу
производных хроман-6-ола (6-гидроксихромана) - токоферолов, отличающихся
степенью метилирования и местоположением метильных групп в хромановом ядре [7].
Биологическое действие витамина Е преимущественно связывается с его
антиоксидантными свойствами, которые в большей или меньшей степени проявляются
на всех уровнях организации - от субклеточных частиц в мембранных образований
до организма в целом. Впервые антиоксидантное действие α-токоферолов было показано в 1954-м
году Алом Л. Тэппелом. На сегодняшний день классическая теория антиоксидантного
действия токоферолов, построенная на большом количестве экспериментальных
данных по окислению жирных кислот в присутствии витамина Е, предполагает
передачу атома водорода с молекулы токоферола (Тф-ОН) на пероксильный радикал
(ROO●) с образованием гидроперекиси:
Тф-OH + ROO● → Тф-O● + ROOH.
α-Тф-OH + O2¯ → α-Тф-O● + HO2¯
возможно также восстановление токофероксильного радикала при
взаимодействии с O2¯:
α-Тф-O● + O2¯ → α-Тф-O● + O2
α-Тф-O¯ + H+ → α-Тф-OH
В микросомах витамин Е одинаково эффективно ингибирует образование
перекисей как в реакциях НАДФН-зависимого ПОЛ, так и при аскорбат-зависимом
окислении, при этом сохраняется целостность мембранных липидов и активность
ферментативных систем гидроксилирования [7].
Селен
Элементарный селен - это гомоцепной неорганический полимер с
винтообразными макромолекулами, уложенными параллельно. В цепях атомы связаны
ковалентно, а молекулы-цепи объединены молекулярными силами и частично -
металлической связью.
Селен и его соединения используются в различных областях деятельности, в
том числе в медицине и в производстве БАД. В частности, селен признан одним из
важнейших антиоксидантов; этот элемент способствует детоксикации производных
кислорода в организме (свободных радикалов) и играет немаловажную роль в борьбе
с раком.
Важнейшей ролью селена является его вхождение в состав
глутатионпероксидазы - фермента предохраняющего клетки от токсического действия
перекисных радикалов.
Селен не может синтезироваться, а должен поступать с пищей извне.
Следовательно, нет селена - нет глутатионпероксидазы. Имеется связь между
селеном и витамином Е - они влияют на разные этапы образования органических
перекисей: токоферолы подавляют (предупреждают) перекисное окисление
полиненасыщенных жирных кислот, а содержащая селен глутатионпероксидаза разрушает
уже образовавшиеся перекиси липидов, перекись водорода. Глутатионпероксидаза,
не содержащая селен, - глутатион-S-трансфераза - разрушает только перекись
водорода (как и каталаза). При достаточном поступлении в организм витамина Е
проявления дефицита селена значительно нивелируются. Наибольшее количество
селена содержится в белках с высоким содержанием цистина: образуются
трисульфиды, которые подобно сульфгидрильным группам мембранных белков,
регулируют стабильность и проницаемость мембран. При дефиците селена и снижении
активности глутатионпероксидазы повышается гемолиз эритроцитов вследствие
действия перекиси водорода и липоперекисей. На активность глутатионпероксидазы
влияет уровень содержания витаминов С и А, которые способствуют усвоению
селена, его транспорту и утилизации. Витамин Е предупреждает окисление селена,
способствует его сохранению. Добавка селена при Е-дефицитном рационе тормозит
накопление липоперекисей, ликвидирует или предупреждает симптомы Е-витаминной
недостаточности. Восстановленныйглутатион и глутатионпероксидаза превращают
липоперекиси в менее токсичные оксикислоты и этим предупреждают повреждение
биоструктур. Пополнение фонда глутатиона происходит за счет аминокислот,
которые содержат серу [7].
Глутатионпероксидаза
Для инактивации перекиси водорода в клетках высшых животных существует
одно важное семейство ферментов - глутатионпероксидаз (систематическое название
«глутатион: перекись-водорода-оксидоредуктаза»), существование которого
показано Гордоном Милзом в 1957 г. В 1973 г. Джон. Т. Ротрак с соавт.
установили, что в состав ГПО входит селен, и каждая молекула фермента содержала
4 атома Se.
Помимо это клеточной изоформы, получившей при дальнейшей классификации
порядковый номер 1 (ГПО1), глутатионпероксидаза представлена селеновыми
изоферментами - «желудочно-кишечным» (ГПО2, выделен из цитозоля клеток печени и
кишечника), внеклеточным (ГПО3, выявляется в плазме и молоке), ГПО
гидроперекисей фосфолипидов (ГПО4) и не содержащими Seизозимами-«секреторным»
(ГПО5, обнаруживаемая в придатках яичек) и ГПО7, а также экзотический ГПО6, в
состав которой селен либо входит (человек, свинья), либо не входит (мышь,
крыса) [7]. Все ГПО в большей или меньшей степени катализируют реакцию
восстановления глутатионом нестойких органических гидропероксидов, включая
гидропероксиды полиненасыщенных жирных кислот, в стабильные соединения -
оксикислоты:
GSH + ROOH → GSSG + ROH + H2O
В результате взаимодействия с гидропероксидом ROOH селеноцистеиновый
остаток фермента переходит из селенола в селененовую кислоту, с которой затем
связывается GSHс образованием селененилсульфида:
ГПО-SeH + ROOH→ROH + ГПО-SeOH
ГПО-SeOH + GSH → H2O + ГПО-Se-SG
Прореагировав со второй молекулой глутатиона, ГПО возвращается в исходное
состояние:
ГПО-Se-SG + GSH → ГПО-SeH + GSSG
ГПО способны также утилизировать H2O2:
GSH + H2O2→GSSG + 2H2O
Кроме того, недавно обнаружено, что селеносодержащие ГПО проявляют
пероксинитритредуктазную активность, восстанавливая ONOO¯ до нитрит-аниона NO2¯и тем самым предотвращая опасные
реакции окисления и нитрования, в которые активно вступает пероксинитрит.
Стехиометрия пероксинитритредуктазной реакции аналогична классической
глутатионпероксидазной реакции с участием гидропероксидов: взаимодействуя с
ONOO¯, фермент окисляется до селеновой кислоты и затем
восстанавливается до исходного состояния двумя молекулами глутатиона; скорость
реакции составляет 8 × 106M-1c-1[25].
Также селеновые ГПО играют важную роль в регуляции биосинтеза
эйкозаноидов, контролируя содержание органических перекисей и поддерживая так
называемый «перекисный тонус». Так, циклооксигеназа, переводящаяарахидоновую
кислоту в циклоэндогидроперекисьPGH2, активируется гидроперекисью,
высокое содержание которой приводит к самоинактивации фермента. Обычная
физиологическая концентрация гидроперекисей в клетках млекопитающих составляет
около 10-10 М, и её повышение до 10-6 М вызывает
активацию циклооксигеназы. Предпологается, что липоксигеназа, отвечающая за
синтез лейкотриенов, простациклиновые и тромбоксановыесинтетазы, также являются
объектами перекисной регуляции [26]. С этой точки зрения становится ясно,
насколько важна функция ГПО в патогенезе воспалительных процессов.
Перекисное окисление липидов
На сегодняшний день все физико-химические аспекты развития процессов
свободнорадикального перекисного окисления липидов (ПОЛ) биологических мембран
изучены достаточно хорошо. ПОЛ - вырожденно-разветвленный цепной процесс,
условно разделенный на стадии: зарождение цепей, развитие цепных реакций и их
разветвление, обрыв цепей. Регуляция процесса возможна на всех его стадиях -
при инициировании это достигается применением ловушек свободных радикалов
(фенольные антиоксиданты, токоферолы, и пр.); при разветвлении - устранением
высокоактивных и часто токсичных промежуточных продуктов с помощью как низкомолекулярных
антиоксидантных компонентов (например, глутатион, аскорбиновая кислота, ионы
металлов переменной валентности в определенных концентрациях или их связывающие
соединения и пр.), так и различные антиоксидантные ферменты (СОД,
глутатионпероксидаза, каталаза и пр.). Наконец, обрыв цепи возможен с помощью
дисмутации радикалов или их замены на менее реакционноспособные радикалы
ингибиторов. В настоящее время описано множество природных антиоксидантов с
известными свойствами, как правило, являющихся ловушками свободных радикалов.
Учитывая важность ПОЛ как в возникновении и развитии различных
патологических состояний, так и в регуляции нормальных процессов
жизнедеятельности организма на всех его уровнях, не утрачен интерес к
разработке новых препаратов, способных тем или иным способом оказывать
направленное действие на протекание ПОЛ в клетке. К новым препаратам, активным
в отношении ПОЛ, прежде всего, обычно предъявляется требование ингибировать
развитие реакций этого процесса в качестве ловушек свободных радикалов
кислорода. Однако, в связи с многовекторностью действия различных
антиоксидантных систем, можно определить ряд потенциально полезных
мембранопротекторных свойств даже для нецеленаправленно получаемых новых
веществ. К ним относится, во-первых, гидрофобность молекулы вещества, то есть
способность его легко проникать сквозь мембрану, что позволит соединению, как
минимум, проникнуть в липидный бислой, а при определенных свойствах нового
вещества и стабилизировать его (так называемый структурный антиоксидант).
Во-вторых, наличие фенольных структур в его составе может придать соединению
свойства фенольного антиоксиданта, который обладает прямой антирадикальной
активностью. В-третьих, при определенных условиях гетероциклические соединения
с различными функциональными заместителями могут служить переносчиками
электронов, что особенно важно при функционировании дыхательных цепей
внутриклеточных мембран (митохондриальной, микросомальной и т.д.) как для
регуляции, так и для нормализации их работы при утрате нормальной концентрации
естественных акцепторов свободных электронов. И наконец, синтетические
органические вещества, имеющие в своем составе эссенциальные микроэлементы,
вероятно, при определенных условиях могут выступать в качестве транспортных форм
для этих элементов, прежде всего -для Se, необходимого для функционирования
одного из ключевых антиоксидатных ферментов -глутатионпероксидазы, особенно с
учетом их гидрофобных свойств и низких эффективных концентраций. Однако, все
эти предположения, безусловно, требуют экспериментального подтверждения.
Материалы и методы
Общие сведения
В наших исследованиях были изучены антиоксидантные свойства 18 новых
гетероциклических соединений (4 из них - селеносодержащие), полученных в
лаборатории органического синтеза Луганского национального педагогического
университета имени Тараса Шевченко. Сначала были определены наиболее
перспективные с точки зрения антиоксидантной активности соединения и
установлены величины их оптимальной концентрации для простой модельной системы
с лецитином яичного желтка, который служил элементарным субстратом процессов
ПОЛ (этот эксперимент не входил в данную работу). Далее представлялось
целесообразным изучить поведение этих веществ в опытах invitro, включающих
более сложный объект - природные биологические мембраны.
В качестве подобного объекта мы использовали микросомы печени крыс,
выделенные с помощью дифференциального центрифугирования мембраны
эндоплазматического ретикулума, поскольку эта структура богата субстратами ПОЛ
- полиненасыщенными жирными кислотами; в её составе функционируют цепи переноса
электронов, что создает условия для образования радикальных форм кислорода;
многие ферменты микросом относятся к металлопротеинам, т.е. связаны с металлами
переменной валентности, что также играет роль в активации ПОЛ. Использование
микросом позволяет в определенной мере стандартизовать условия проведения
опыта.
Постановка эксперимента заключалась в искусственном индуцировании
перекисного окисления липидов мембран микросом с помощью аскорбиновой кислоты и
ионов железа (сольМора). Добавление этих компонентов в реакционную среду
способствовало образованию активированных кислородных метаболитов
(гидроксильных радикалов, пероксидных радикалов жирных кислот и т.д.). После
инкубации в течение 30 минут в пробах спектрофотометрически определялось
количество вторичного продукта ПОЛ - малонового диальдегида. По уровню его
накопления судили об антиоксидантной активности добавляемых в реакционную среду
исследуемых веществ. Для сравнения использовали ионол. Контролем служили
образцы без активных веществ, но с добавлением растворителя (диметилсульфоксид,
или ДМСО), который сам обладает некоторым антиоксидантным эффектом.
Выделение микросом печени крысы
Для выделения микросом мы декапитировали крысу, быстро вырезали печень и
положили ее на 3 мин. на сахарозный лед для охлаждения. Затем осушили печень
фильтровальной бумагой, взвесили 3-4 г и продавили через пресс. Далее её
гомогенизировалии поместили в среду выделения (фосфатный буфер, сахароза и
ЭДТА).
Полученный раствор центрифугировали 15 мин. при 2 тыс. об./мин. В осадок
выпали обрывки клеток, ядра (ядерная фракция, которую необходимо удалить).
Далее надосадочную жидкость повторно центрифугируют 10 мин. при 5800
об./мин. В осадок выпадают митохондрии. Окончательно полученный супернатант и
является микросомами печени крыс.
Исследование индукции ПОЛ
Для исследования индукции ПОЛ готовили 20% гомогенаты печени крыс в 100
мМ трис-HClбуфере, pH 7,4 и фильтровали его через 3 слоя нейлона. Интенсивность
аскорбат-зависимого ПОЛ исследовалисразу после их приготовления, определяя
накопление МДА в этот момент времени и через 30 минут инкубации гомогенатов при
37°C постоянном помешивании в среде. Среда инкубации дополнительно содержала
0,5 мМ аскорбат и 12 мкМ моль Мора. Гомогенат вносили по 0,1 мл на 2,0 мл среды
инкубации, при этом концентрация белка была около 0,5 - 1 мг в 1 мл. В среду
барботировали воздух. Пробы для определения количества образовавшегося МДА
брали после осаждения белка ТХУ (трихлоруксусной кислотой). При этом записывали
спектр поглощения окрашенного продукта на спектрофотометре, определяя Е
532-580. Количество МДА рассчитывали, принимая коэффициент экстинкцииравным 1,56
× 10-5
М-1 см-1.
Определение концентрации белка по методу Бредфорда
Метод Бредфорда - один из колориметрических методов количественного
определения белков в растворе. Метод основан на реакции красителя кумасси
(coomassie) с аргинином и гидрофобными аминокислотными остатками. Связанная
форма имеет голубую окраску с максимумом поглощения при 595 нм. Таким образом,
увеличение адсорбции раствора при длине волны, равной 595 нм, пропорционально
количеству белка в растворе.
В спектрофотометрическую кювету с длиной оптического пути 1 см мы вносили
0,1 мл раствора белка в 0,1 н NaOH, добавляли 2 мл раствора кумасси,
перемешивали при комнатной температуре 2-3 минуты и быстро измеряли оптическую
плотность смеси при 595 нм, используя в качестве контроля кювету, содержащую
0,1 мл 0,1 н NaOH и 2 мл красителя.
Результаты и обсуждение
Как видно из приведенных данных, преимущественное большинство соединений,
показавших в модельной системе антиоксидантный эффект, обнаруживало подобную
активность и в более сложной системе. Однако были и исключения. В общем,
подобное поведение антиоксидантов не является неожиданным. Известно, что
усложнение системы, в которой проводятся испытания антиоксидантных свойств,
приводит иногда к снижению эффективности препарата [27].
Именно этим фактом мы руководствовались, применяя в опыте концентрации
веществ несколько более высокие, чем полученные для них величины ранее. Более
того, в исключительных случаях может изменяться сама направленность эффекта - с
антиоксидантной до прооксидантной. Это связано с синергическим эффектом при
взаимодействии нескольких слабых факторов в живом объекте, приводящим к их
резкому усилению.
Например, в клетке в определенных условиях может значительно возрастать
энергия слабых радикальных соединений, их превращение в активаторов ПОЛ, тогда
как в норме сами по себе они являются ингибиторами ПОЛ именно из-за своих
радикальных свойств и не представляют опасности из-за низкой энергетичности.
Это показано, в частности, в опытах с применением витамина Е. Разумеется, в
каждом подобном случае причины изменения эффектов одного и того же соединения в
разных условиях опыта могут быть совершенно различны, но все они, безусловно,
связаны с взаимодействием того или иного соединения с какими-то структурами в
изучаемой системе.
Как и в предыдущем исследовании, соединения I (DVD-2521), II (KDA-150),
III (KDA-132), IV (BO-20), , V (DVD-8843), VI (DVD-2808), VII (DVD-26), VIII
(NAA-85) проявили антиоксидантную активность, причем, в данном случае - в
присутствии микросом. Это говорит о том, что, как минимум, эти вещества могут
быть ловушками свободнорадикальных форм кислорода. Следовательно, их можно
отнести к истинным антиоксидантам. Объяснить это можно различно.
Ожидаемо проявили сильные антиоксидантные свойства селеносодержащие
соединения (I, V, VI). Вызвано это тем, что селен играют одну из самых важных
ролей в антиоксидантной системе человека, взаимодействует с витаминаи А и Е,
принимает непосредственное участие в синтезе глутатионпероксидазы - сильнейшого
антиоксиданта (как уже описывалось выше). И в следствие этого возникает такой
сильный антирадикальный эффект.
Остальные 5 веществ, вероятно, смогли проявить антиоксидантную активность
благодаря большому количеству сопряжённых двойных связей, которые выполняют
роль свободнорадикальных ловушек. Также можно предположить, что в отличии от
других соединений, которые будут разобраны ниже, молекулы данных являются более
компактными (имеют меньшие размеры).
Остальные вещества не обнаружили антиоксидантного эффекта на микросомах,
что, вероятно, можно объяснить следующим образом.
В нашем случае вещество XIII (Л-8) проявило при инкубировании с
микросомами отчетливый прооксидантный эффект, т.е. активировало ПОЛ (более чем
на 40 %), тогда как в опытах с лецитином это вещество ингибировало
липопереокисление, по-видимому, за счет улавливания и инактивации
свободнорадикальных форм кислорода. Принимая во внимание структуру данного
соединения, можно сделать вывод, что Л-8 действительно может связывать
свободнорадикальные формы кислорода. В растворе лецитина это вызывает их
инактивацию, поэтому процесс ПОЛ ингибируется, причем с примерно одинаковой
эффективностью при разных концентрациях вещества, т.е. лимитирующим фактором,
вероятно, является концентрация радикалов в среде. Однако при наличии
мембранного липидного бислоя гидрофобная и довольно громоздкая молекула Л-8
проникает вглубь мембраны, задерживаясь там вместе со связанными кислородными
радикалами. При встраивании молекулы Л-8 структура мембраны становится более
рыхлая, радикалы кислорода получают свободный доступ к ненасыщенным жирным
кислотам мембранных фосфолипидов, т.е. к субстратам ПОЛ. Проще говоря, мы
считаем, что Л-8 может не только связывать, но и транспортировать радикальные
формы кислорода в липидный бислой, встраиваясь в него и механически
дестабилизируя его. Однако, для доказательства этого предположения целесообразно
было бы сравнить влияние Л-8 на ПОЛ в лецитиновых липосомах. В подобной
постановке лецитин находился бы не просто в растворе, а в составе липидного
бислоя, состоящего исключительно из молекул лецитина.
Аналогичные выводы можно сделать, анализируя поведения соединения
XII(DVD-0749). Следует отметить лишь, что его молекула по величине почти в 2
раза меньше Л-8, но также не является компактной молекулой. Вместе с тем, очень
похожее визуально на DVD-0749 соединение XI (DVD-4702) проявляет умеренно антиоксидантные
свойства в обоих случаях - и в простой безмембранной системе с субстратом ПОЛ
лецитином, и при наличии этого же компонента (наряду с другими) в составе
мембран микросом. Очевидно, что структурные отличия являются причиной разного
поведения этих соединений, однако на данном этапе исследований не
представляется возможным объяснить, каким образом.
Соединения XV (DVD-3779) и XIV (ВО-35) также, как и три вышеописанных,
являются ловушками свободнорадикальных форм кислорода и, вероятно, могут
переносить их в липидный мембранный бислой с разной степенью эффективности и в
зависимости от типа этого бислоя.
Отдельно следует сказать о соединениях, которые были растворимы в воде -
VIII (NAA-23)и XVIII (NAA-177). Они показали слабую антиоксидантную активность.
Причем в случае с NAA-177 она не зависела от концентрации вещества в растворе с
лецитином. В системе с микросомами препараты не функционировали как
антиоксиданты. Вероятно, это связано с непроницаемостью для них липидного
мембранного бислоя за счет их заряженности. Возможно, эти соединения могут
проявить себя в другом биологическом качестве, например, они вполне могут
действовать как нуклеофилы, участвуя в разобщении процессов дыхания и
окислительного фосфорилирования в митохондриях.
Таблица 2
|
Порядковые номера, названия и формулы препаратов
|
Концентрация препаратов (мкМ)
|
Концентрация МДА (нмоль на 1 мг белка за 1 мин)
|
Ингибирование относительно контроля (%), сравнительная
гистограмма с ионолом.
|
|
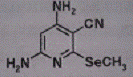 I. DVD-2521 I. DVD-2521
|
2,5
|
1,05±0,009
|
52 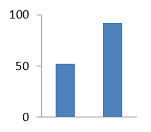
|
|
10
|
1,74±0,011
|
20 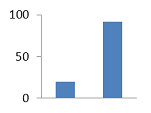
|
|
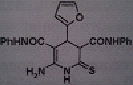 II. KDA-150 II. KDA-150
|
2,5
|
1,82±0,010
|
17 
|
|
10
|
1,67±0,008
|
26
|
|
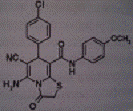 III. KDA-132 III. KDA-132
|
2,5
|
1,23±0,011
|
44
|
|
10
|
1,31±0,015
|
40 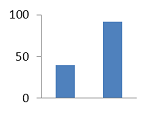
|
|
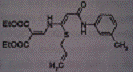 IV. BO-20 IV. BO-20
|
1,92±0,020
|
12 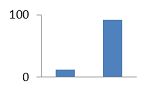
|
|
10
|
1,46±0,011
|
33 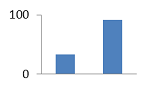
|
|
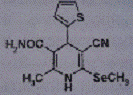 V. DVD-8843 V. DVD-8843
|
10
|
1,38±0,009
|
37 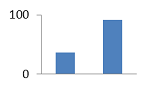
|
|
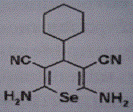 VI. DVD-2808 VI. DVD-2808
|
10
|
1,23±0,011
|
44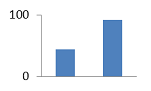
|
|
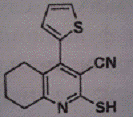 VII. DVD-26 VII. DVD-26
|
10
|
1,54±0,015
|
29 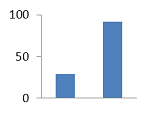
|
|
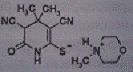 VIII. NAA-23 VIII. NAA-23
|
10
|
2,13±0,017
|
2
|
|
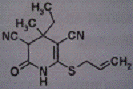 IX. NAA-84 IX. NAA-84
|
10
|
2,00±0,017
|
8
|
|
 X. NAA-85 X. NAA-85
|
10
|
1,54±0,010
|
29 
|
Гистограмма всех показателей ингибирования в процентном соотношении
относительно контроля
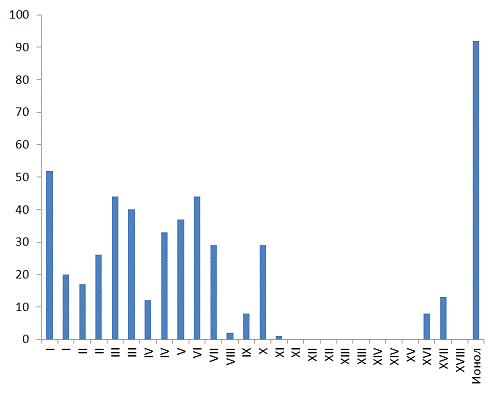
Выводы
. Мы проверили 18 новых гетероциклических и селенсодержащих веществ на их
возможные антиоксидантные свойства в перекисном окислении липидов. Часть
соединений дали ингибирующий эффект, другие же никак не подействовали или даже
проявили прооксидантные свойства.
. Проведя этот эксперимент, мы выяснили, что очень актуальным и
целесообразнымв данный момент является синтезирование новых препаратов,
способных проявлять антиоксидантные свойства, а именно - ингибировать реакции
процессов перекисного окисления липидов за счёт ловушек свободных радикалов
кислорода. Причиной актуальности является огромная роль ПОЛ в регуляторных
процессах всего организма, а также развитии различных патологических состояний.
. Особое внимание стоит уделить селенсодержащим соединениям, так как:
а) Большинство из них дали сильный ингибирующий эффект;
б) Селен играет одну из самых главных ролей в антирадикальной системе
человека за счёт содержания в главном антиоксиданте - глутатионпероксидазе,
которая без поступления этого элементаизвне не может синтезироваться.
Список литературы
1. Иванов
К.П. Основы энергетики организма: Теоретические и практические аспекты. Том 2.
Биологическое окисление и его обеспечение кислородом. - СПб.: Наука, 1993. - c.
272.
.
EsterbauerH. Cytotoxicityandgenotoxicityoflipid-oxidation // Am. J. Clin.
Nutr.- 1993.-Vol. 57, Suppl.- p. 779.
. Dawson
T.M., Bredt D.S., Fotuhi M. et. al. Nitric oxide synthase and neuronal NADPH
diaphorase are identicial in brain and peripheral tissues // Proc. Natl. Acad.
Sci. USA.- 1991.- Vol. 88.- p. 779.
. Barja G.
Oxygen radicals, a failure or a success of evolution? // Free Radic. Res.
Commun.- 1993.- Vol. 18.- p. 63.
. Зенков
Н.К., Ланкин В.З., Меньщикова Е.Б. Окислительный стресс.
Биохимическийипатофизиологическийаспекты.- M.: Наука/Интерпериодика, 2001.- c.
340.
. Sies H.
Oxidative stress. - From basic research to clinical application// Am. J. Med.-
1991.- Vol. 91, Suppl. 3C.- p.31.
.
МеньщиковаЕ. Б., ЛанкинВ. З., ЗенковН. К., БондарьИ. А., КруговыхН. Ф.,
ТруфакинВ. А. Окислительный стресс. Прооксиданты и антиоксиданты. - М., 2006. -
стр. 12-13, 21-22, 141-143, 193-196, 228-231, 383, 389-390
. Владимиров
Ю.А. Свободные радикалы в биологических системах // Сорос.образоват. журн.-
2000.- № 12.- c. 13.
. Зенков
Н.К., Меньшикова Е.Б. Активированные кислородные метаболиты в биологических
системах // Успехи соврем.биологии.- 1993.- Т. 113, вып.3.- c. 286.
. Vanasbeck
B.S. Involvment of oxygen radicals and blood cells in the pathogenesis of ARDS
by endotoxin and hyperoxia // Appl. Cardiopulm. Pathophysiol.- 1991.- Vol. 4.-
p. 127.
. Dimascio
P., Devasagayam T.P.A., Raiser S., Sies H. Carotenoids, tocopherols, and thiols
as biological singlet molecular oxygen quenchers // Biochem. Soc. Trans.-
1990.- Vol. 18.- p. 1054-1056.
. Li J. M.,
Shah A.M., Endothelial cell superoxide generation: regulation and relevance for
cardiovascular pathophysiology // Am. J.Physiol. Regul. Comp. Physiol.- 2004.-
Vol. 287.- p. 1014.
. Poli G.,
Leonarduzzi G., Biasi F., Chiarpotto E. Oxidative stress and cell signaling //
Current Med. Chem.- 2004.- Vol. 11.- p. 1163.
. Landar A.,
Darley-Usmar V.M. Nitric oxide and cell signaling; modulation of redox tone and
protein modification // Amino Acids.- 2003.- Vol. 25.- p. 313.
. Halliwell
B., Gutteridge J.M.C. Free radicals in biology and medicine (2nded.).-
Oxford: Clarendon, 1989.-p. 320, 433.
. Абрамова Ж.
И., Оксенгендлер Г.И. Человек и противоокислительные вещества.- Л.: Наука,
1985.- с. 80.
. Кения М.
В., Лукаш А. И., Гуськов Е. П. Роль низкомолекулярных антиоксидантов при
окислительном стрессе // Успехи соврем.биологии.- 1993.- Т. 113, вып. 4.- с.
456.
. Cross A.
R., Jones O. T. G. Enzymic mechanisms of superoxide production // Biochim.
Biophys.Acta.- 1991.- Vol. 1057.- p. 281.
. Nikki E.
Action of ascorbic acid as a scavenger of active and stable oxygen radicals //
Am. J. Klin. Nutr.- 1991.- Vol. 54.- p. 1119.
. Sevanian
A., Davies K. J. A., Hochstein P. Serum urate as an antioxidant for ascorbic
acid // Am. J. Klin. Nutr.- 1991.- Vol. 54.-p. 1129.
21. Kikugawa K. Hiramoto K. Tomiyama S. Asano Y.
β-Carotene effectively scavenges toxic nitrogen oxides; nitrogen dioxide
and peroxynitrous acis //
Febs Lett.- 1997.- Vol. 404.- p. 175.
. Lowe G. M.,
Vlismas Л., Young A. J. Carotenoids as prooxidants? // Mol Aspects Med.- 2003.
Vol. 24.- p.363-364.
. Azzi A.,
Stocker A. Vitamin E: non-antioxidant roles // Progr. LipidRes.- 2000.- Vol.
39.- p. 231.
. Gotoh N.,
Niki E. Rates of interactions of superoxide with vitamin E, vitamin C and
relates compounds as measured by chemiluminescence // Biochim. Biophys.Acia.-
1992.- Vol. 1115.- p. 201.
. Briviba K.,
Kissner R., Koppenol W. H., Sies H. Kinetic study of the reaction of
glutathione peroxidase with peroxynitrite // Chem. Res. Toxicol.- 1998.- Vol.
11.- p. 1398-1399.
. Link E. M.
Enzymic pathways involved in cell response to H2O2 //
Free Radic. Res. Commun.- 1990.- Vol. 11.- p. 89.
. Зенков Н.
К., Кандалинцева Н. В., Ланкин В. З., Меньщикова Е. Б. Фенольные
биоантиоксиданты - Новосибирск, 2003.- с. 120.