Композиционные материалы в системе AlN-Al2O3-ZrO2-ZrN
ВЫПУСКНАЯ
КВАЛИФИКАЦИОННАЯ РАБОТА
КОМПОЗИЦИОННЫЕ
МАТЕРИАЛЫ В СИСТЕМЕAl2O3-ZrO2-ZrN
Введение
Одним из перспективных материалов является диоксид циркония, твердые
растворы которого с оксидами II-IV группы характеризуется высокой огнеупорностью
низкой теплопроводностью в широком диапазоне температур. При изготовлении
плотной керамики из диоксида циркония применяют традиционные способы, наиболее
близкими из которых являются технологические приемы, применяемые при
изготовлении корундовых изделий. Для получения прочных и термостойких изделий
одними из важнейших являются следующие задачи:
стабилизация высокотемпературной кубической модификации диоксида циркония
для предотвращения полиморфных переходов при эксплуатации изделий;
получение, по возможности, мелкокристаллической структуры материала;
получение высокоплотного композиционного материала с минимальной
пористостью и высокими механическими свойствами.
Известно, что нитриды обладающие низкой адгезией к металлам и оксидам и
проводящие электрический ток перспективны в качестве добавок к керамике на
основе ZrO2.
Добавки нитридов, особенно в ультрадисперсном состоянии способны повысить
механические, трибологические характеристики, а также дают возможность получить
материалы с повышенным уровнем тепло- и электропроводности.
В данной работе предпринята попытка получения плотных, износостойких
материалов на основе диоксида циркония с добавлением нитрида алюминия и нитрида
циркония.
1 Аналитический обзор
керамический композиционный материал цирконий алюминий
1.1 Система цирконий-кислород
Диоксид циркония представляет собой порошок от белого до желтого с
сероватым оттенком цвета, используемый для изготовления технической керамики,
является искусственным материалом, так как природные цирконийсодержащие минералы
и породы сильно загрязнены посторонними включениями [1].
В литературе сообщалось о существовании следующих фаз в системе
цирконий-кислород. Твердый раствор кислорода в a-Zr, твердый раствор кислорода в b-Zr, Zr4O, Zr3O,
Zr2O, ZrO, Zr2O3, ZrO2, ZrO3,
твердый раствор Zr в ZrO2.
Получены убедительные доказательства существования оксидов Zr4O,
Zr3O, Zr2O, которые рассматриваются как гексагональные
структуры.
Летучее соединение ZrO образуется при реакции металлического циркония с
диоксидом циркония.
Оксид Zr2O3 был получен в виде зеленоватого порошка
при сгорании ZrH2.
Наиболее важным и хорошо изученным соединением является диоксид циркония
ZrO2, обладающий развитым полиморфизмом. Сообщалось о существовании
следующих форм диоксида циркония: моноклинной, тетрагональной, кубической,
метатетрагональной, низкотемпературной кубической, тригональной,
высокотемпературной моноклинной, стеклообразной. В настоящее время
общепризнанно существование трех полиморфных форм: моноклинной, тетрагональной
и кубической.
° 2300°2 D ZrO2 D ZrO2 (1)
мон. 1000°
тетр.2300° куб.
Диаграмма состояния системы цирконий-кислород приведена на рисунке 1.
Моноклинная форма имеет следующие параметры кристаллической решетки:
а = 5,1477А;= 5,2030 A; = 5,3156 A;
b = 99°23¢;
относится к пространственной группе Р21/с с четырьмя молекулами ZrO2
в элементарной ячейке.
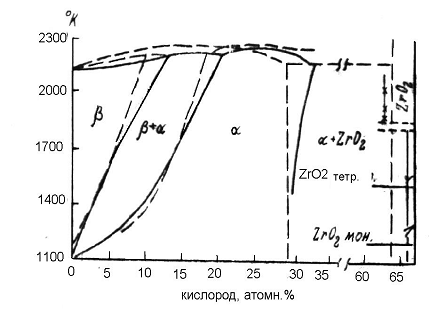
Рисунок
1 - Диаграмма состояния системы цирконий - кислород.
Рентгеновская
плотность Dх = 5852 кг/м3
Пикнометрическая
плотность 5680 кг/м3
Микро
твердость 10000 МПа
Модуль
Юнга 180 ГПа
В
интервале температур от 1000 до 1200°С бадделеит
переходит в тетрагональную форму, при этом происходит объемное сжатие на
7,7%.При охлаждении до температуры около 1000°С совершается
обратный переход из тетрагональной в моноклинную форму, но уже с объемным
расширением на 7,7%.
По
данным термографических исследований скорость нагревания сильно влияет на
температуру, при которой наблюдается максимальная скорость превращения. В этот
момент количество диоксида циркония, перешедшего в тетрагональную модификацию,
составляет 40-50%.
При
скорости нагрева 10°С в минуту переход сопровождается эндотермическим
эффектом при 1160°С. Этот переход полностью обратим, но обратный переход
происходит при более низких температурах (960°С при той же
скорости охлаждения). Примеси, условия получения материала и тепловая история
могут в значительной мере изменять температурный интервал перехода. Показано,
что полиморфные превращения моноклинного диоксида циркония (m- ZrO2)
в тетрагональный диоксид циркония (t-ZrO2) являются бездиффузионными
мартенситовыми.
Количество
дефектов, препятствующих перемещению «дислокаций перемещения», влияет на
температуру и кинетику процесса.
Тетрагональная
модификация диоксида циркония при отсутствии гафния как примеси имеет
примитивную тетрагональную ячейку с параметрами а=5,09 А и с=5,18А. Кроме
высокотемпературной области тетрагональная фаза может существовать в интервале
0-500°С, когда она получается из легко разлагающихся солей
циркония. При нагревании до 700-800°С или длительном
хранении низкотемпературная тетрагональная фаза необратимо переходит в
моноклинную форму.
Тетрагональная
фаза диоксида циркония может существовать при значительной дефектности по
кислороду вплоть до ZrO1,7 при 1800°С.
Сохранить
тетрагональную фазу в чистом диоксиде циркония путем закалки не удается.
Вопрос
о стабилизации кубической модификации диоксида циркония в чистом
стехиометрическом соединении не решен окончательно. Параметр решетки кубического
диоксида циркония а=5,07А.
При
разложении диоксида циркония возможно образование низкотемпературной кубической
формы (до 2000°С), которая при нагревании и хранении также необратимо
переходит в моноклинную.
Данные
о возможности существования стеклообразного диоксида циркония впоследствии были
опровергнуты [2].
Способы
получения диоксида циркония из цирконовых концентратов можно подразделить на
две группы: прямые способы, которые не предусматривают перевод циркония в
раствор, и способы, включающие растворение циркония.
Метод
плазменного плавления циркона. При температуре 1676±10°С цирконий начинает диссоциировать на оксиды [3].
4 Û ZrO2 + SiO2 (2)
Процесс
ускоряется с повышением температуры. При последующем быстром охлаждении
обратная реакция практически не имеет места. Промышленная реализация способа
осуществляется при использовании плазменного реактора. Продукт может быть
получен в виде сфероидальных частиц диаметром 0,125 - 0,25 мм, включающих
мелкие вытянутые или сферические частицы моноклинного и тетрагонального ZrO2,
распределенные в стекловидной матрице кремнезема [4].
Для
очистки диоксида циркония от кремнезема используют методы физического и
химического разделения.
В
плазменном реакторе можно получить стабилизированный диоксид циркония при
термообработке ZrO2 в смеси с CaO или J2O3,
синтез протекает в течение нескольких мс [5].
Плавление
циркона в дуговых печах. Этот метод также основан на способности циркона к
термической диссоциации; он осуществляется в присутствии восстановителя,
благодаря чему кремний удается отделить от циркона еще на стадии плавки.
Спекание
циркона с добавками щелочноземельных оксидов. При добавке щелочных и
щелочноземельных оксидов температура диссоциации циркона понижается вследствие
связывания кремнезема оксидными добавками. При определенном дозировании
оксидных добавок можно получить в качестве продукта реакции смесь ZrO2
с силикатом металла, оксид которого был введен в шихту.
Образующиеся
в качестве продукта реакции силикаты отделяют от ZrO2 химическими
или физическими методами.
Диоксид
циркония можно получать непосредственно при гидротермальной обработке циркона
гидроксидом магния или кальция при 300-380°С.
Методы
прямого получения диоксида циркония являются наиболее экономичными и находят
применение для получения обычного и стабилизированного диоксида циркония, когда
не требуется высокая чистота материалов. Для получения более чистого оксида
циркония используют методы, включающие перевод циркония в раствор и его
последующее селективное осаждение [6].
Диоксид
циркония характеризуется высокой (2700°С) температурой
плавления. При температуре выше 500°С является ионным
проводником. Керамика из диоксида циркония хорошо механически обрабатывается до
высокой чистоты поверхности, обладает более низким коэффициентом трения по
сравнению с металлами. Диоксид циркония обладает высокой химической стойкостью
к кислотам и щелочам (кроме H2SO4 и HF), расплавам
щелочей, стекол и металлов[7].
Материалы
на основе оксида циркония получили техническое применение в качестве огнеупоров
в силикатном производстве и металлургии ,стержней накаливания в осветительной
технике, светофильтров в оптической промышленности, высокотемпературных
электролитов в электрохимии и т.д.
В
последние годы они привлекают внимание материаловедов как перспективная
матричная основа для разработки высокотемпературных керамических материалов,
поскольку оксид циркония обладает высокими прочностными и огнеупорными
характеристиками. Наличие в этой системе целой серии фазовых переходов
открывает дополнительные возможности, например, существенно пластифицировать
материал благодаря мартенситному переходу из тетрагональной в моноклинную фазу
[8].
Кубические
твердые растворы со структурой типа флюорита на основе диоксида циркония широко
используются в качестве твердых электролитов с кислородной проводимостью. При
оценке возможности их длительной эксплуатации необходимо помнить , что для ряда
систем , включающих ZrO2 , характерной особенностью является распад твердых
растворов структуры флюорита в определенном интервале температур [9].
По
электрофизическим характеристикам основным требованиям в большой степени
удовлетворяет диоксид циркония, стабилизированный оксидом иттрия. [10].
.2. Система цирконий-азот
Порошкообразный нитрид ZrN - вещество желто-коричневого цвета. Спеченные
при высокой температуре штабики из нитрида циркония хрупки и характеризуются
лимонно-желтым изломом.
В порошкообразном состоянии он стоек на холоду против действия многих
минеральных кислот, особенно соляной, азотной, хлорной. При нагревании
растворимость резко увеличивается как в концентрированных, так и в разбавленных
кислотах.
Полностью растворяется в концентрированной H2SO4, в
смеси азотной и плавиковой кислот и в концентрированной серной кислоте с
добавкой сернокислого калия [11].
В растворах щелочей с концентрацией до 20% устойчив даже при кипячении,
но разлагается кипящими 40%-ными растворами в течении 6 часов.
Тонко измельченный нитрид циркония (0,8-1,0 мкм) реагирует с водой с
выделением аммиака. Кислородом воздуха не окисляется до 900-1000 °С и является одним из наиболее
устойчивых в этом отношении нитридов. Окисление нитрида усложняется
образованием тетрагональной двуокиси ZrO2 при высоких температурах,
главным образом выше 1200°С,
и моноклинной при низких температурах.
При окислении в интервале 400-600°С образуется так называемая аморфная двуокись циркония,
которая частично может стабилизироваться оставшимся кубическим ZrN. При более
высоких температурах (700-1000°С) образуется моноклинная форма ZrO2 [12].
На кривой нагревания нитрида обнаружен один эндотермический эффект в
интервале 580-680°С,
отвечающий окислению его кислородом воздуха. Окисление протекает через стадию
образования оксинитридов, которые при повышении температуры до 700°С полностью разлагаются с
образованием моноклинной двуокиси циркония.
При нагреве в водороде он устойчив до очень высоких температур [13].
Основным методом приготовления нитрида циркония является непосредственное
азотирование порошка циркония в среде азота, оптимальная температура 1200°С [14].
Медленнее происходит процесс насыщения циркония азотом в диссоциированном
аммиаке: необходима температура не ниже 1400°С.
Другой метод получения нитрида циркония, впервые примененный Фридерихом и
Зиттигом, заключается в восстановлении углем диоксида циркония в среде азота:
2
+ 2C + 1/2 N2 ®ZrN
+ 2CO (3)
при температурах до 1300°С. Полученный продукт содержит кроме нитрида циркония 7-10% примеси,
нерастворимой в серной кислоте и состоящей из ZrO2 и некоторых
других загрязнений. По данным метода не возможно получить чистый нитрид
циркония.
Авторы [15] разработали метод получения нитрида
циркония восстановлением диоксида циркония магнием в присутствии азота:
2
+ 2Mg + 1/2 N2 = ZrN + 2MgO (4)
Технологически при восстановлении ZrO2 магнием в среде азота
при 1100°С образуется нитрид циркония, по
свойству близкий к ZrN, Недостатком этого метода является необходимость отмывки
продукта восстановления от оксида магния, что удлиняет и усложняет
технологический процесс.
Нитрид циркония можно получить также методом наращивания из газовой фазы.
Как видно из диаграммы состояния системы Zr-N (рисунок 2) максимальная
растворимость азота в β-Zr составляет 5 % ат. при температуре перитектической
реакции и снижается до нуля при температуре α-β превращения, равной 862ºС. Растворимость азота в α-Zr
составляет при
температуре образования α-твёрдого раствора 24 % ат. и понижается с уменьшением
температуры, достигая 21,5 % ат. при 800ºС.
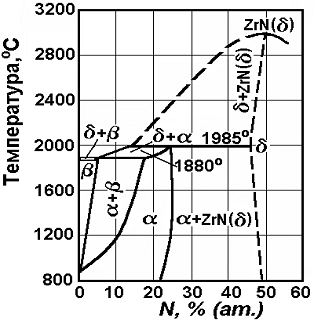
Рисунок 2 - Диаграмма состояния системы Zr-N
Согласно [16], в системе Zr-N, кроме твёрдых растворов азота в α-
и β-Zr,
существует кубический
(типа NaCl) мононитрид ZrN. По данным [17], область гомогенности фазы ZrN при
1500ºС определяются составами ZrN0,51-ZrN1,00,
периоды решётки, в пределах которой увеличивается с увеличением содержания
азота от 4,584 до 4,577 Å. Температура плавления ZrN была принята равной
2980±50ºС. Более поздними исследованиями [18]
было установлено, что нитрид циркония, содержащий даже очень малое количество
кислорода, имеет более низкую температуру плавления.
Параметр решетки ZrNx меняется с изменением состава весьма необычно. При
субстехиометрических составах решетка слегка расширяется при удалении из нее
азота; причины этого не известны.
Система Zr-N изучалась также в работах [19,20] , где исследовалось повышение температуры a-b-превращения при добавлении азота. Растворимость азота
в a-Zr равнялась около 20ат.%. Данные,
полученные в этих работах, совпадают с позднее полученными результатами,
опубликованными в работе [21].
Таким образом, согласно [22], мы приходим к выводу, что в системе
обнаружено одно стабильное соединение. Хотя ранее, в работе [23] были сообщения о существовании еще одного нитрида с 13ат.% N
.
Однако, как отмечалось в [24], действием аммиака на
тетрагалогениды циркония получены нитридные фазы, содержащие азот больше, чем в
нитриде ZrN.
Согласно[24], действием аммиака на Zr при 750°С, а также на ZrCl4 и ZrB4
при более высоких температурах был получен нитрид ZrxN
темно-голубого цвета с 0,940>x>0,812.
Основной областью использования нитрида циркония является его применение
в качестве огнеупорного материала с высокими точками плавления и значительной
стойкостью против окисления. Из нитрида циркония изготавливают тигли для плавки
некоторых тугоплавких материалов.
.3 Система алюминий-азот
Алюминий образует с азотом два соединения - нитрид алюминия AlN и триазид
алюминия Al(N3)3 - очень гигроскопичное взрывчатое
вещество белого цвета. AlN имеет одну гексагональную модификацию типа вюрцита.
Порошок AlN обычно белого, монокристаллы - водянисто-белого цвета (прозрачны);
при загрязнении примесями оксикарбида алюминия Al2OC приобретает
голубоватую окраску. Нитрид алюминия обладает твердостью 9 по шкале Мооса,
плотностью 3,27 г/см3.Плотная керамика из AlN имеет твердость по
Кнупу (500 г) 12 ГПа, модуль упругости 300-310ГПа, прочность при изгибе 300-450
МПа; ТКЛР в интервале 25-1000°С 4,8-5,6·10-6К-1;
удельное электросопротивление 1012-1013Ом·см; при 25°С и частоте 106Гц tgd = (2-10)·10-4 и e = 8,5-10 [7]. Данные по температуре плавления AlN весьма разноречивы (от
2000 до 2500°С), что
понятно, так как нитрид алюминия разлагается до достижения температуры
плавления на компоненты, температура начала разложения определяется
особенностями условий проведения определения «температуры плавления» [22 ].
Нитрид алюминия относится к классу ковалентных бескислородных соединений,
однако ионная компонента связи в нем около 20%, в связи с чем AlN относится к
диэлектрикам. Определенная доля ионной компоненты связи приводит к некоторому
упрочнению решетки, что вызывает увеличение ширины запрещенной зоны [25]. Воздействием высоких давлений и температур на
гексагональный нитрид алюминия, кристаллическую структуру AlN изменить не
удавалось [26]. Однако в условиях термообработки
AlN, обеспечивающих диффузию кислорода в решетку нитрида, обнаружено
образование многослойных политипов, формирование которых связано с
высокотемпературным расслоением ТР замещения 2H - AlN - O [27]. В AlN наблюдается sp3 - гибридизация атомных
орбиталей, координационное число атомов Al и N равно четырем, но из-за несовпадения
центра электронной плотности с центром тетраэдра ( отношение с/а = 1,600 вместо
1,633 при этом каждый атом смещен вдоль оси с к основанию тетраэдра на 0,005
нм) углы между связями в AlN колеблются от 107,7 до 110,5°, а расстояния Al - N от 1,885 до
1,917Å.
На порошкообразный нитрид алюминия очень слабо на холоду действуют вода,
соляная, серная, азотная кислоты, царская водка, холодная плавиковая кислота на
AlN не действует. При нагревании в H2SO4 (1:1) нитрид
алюминия полностью разлагается за четыре дня по реакции: 2AlN+H2SO4+6H2O=2Al(ON)3+(NH4)SO4.
Нитрид алюминия разлагается с выделением аммиака при действии концентрированных
горячих растворов щелочей: AlN+3H2O+OH-gAl(OH)4-+NH3
[22 ].
Сухие галогены медленно действуют на нитрид алюминия; хлор начинает
разлагать его только при 760°С с образованием AlCl3 [28].
Сухой хлористый водород практически не оказывает никакого влияния. При
нагревании с серой и фосфором наблюдается частичное разложение, парами
хлористой серы разлагаются быстро, а PCl3 на нитрид не действует [29].
На нитрид алюминия не действует расплавленный алюминий (до 2000°С), галлий (до 1300°С), борный ангидрид (до 1400°С).
Окисление порошка на воздухе начинается при температуре 1200°С, при этой же температуре AlN
начинает реагировать с углеродом. Нитрид алюминия активно взаимодействует с
базальтом (1400°С;
0,5 ч), с медным штейном (1300°С; 0,5 ч), медленнее - с никелевым штейном (1250°С;5 ч), слабо - с медным шлаком (1300°С; 5 ч).
Высокую стойкость обнаруживает нитрид алюминия по отношению ко многим
полупроводниковым соединениям, в частности к полупроводникам типа АIIIBV,
что позволяет использовать контейнеры из нитрида алюминия для получения
монокристаллов этих соединений [28].
Большинство известных способов получения нитрида алюминия позволяют
синтезировать только технический продукт, совершенно не пригодный для
полупроводниковых целей.
Наиболее распространенным методом является непосредственный синтез
нитрида алюминия из элементов по реакции:
Al + N2 = 2AlN (5)
Она является гетерогенной, и ее скорость в значительной степени
определяется величиной поверхности раздела фаз, т.е. дисперсностью алюминия. В
качестве исходного сырья, как правило, используется мелкодисперсный алюминий, в
качестве нитрирующего агента - очищенный азот или газообразный аммиак.
Особенность азотирования порошка алюминия - наличие на частицах оксидных
пленок (g-Al2O3),
которые удаляются, по-видимому, по реакции образования низших летучих оксидов
алюминия: Al2O3 + 4Al = 3Al2O. С нарушением
такой пленки при перестройке Al2O3 в Al2O азот
проникает к ювенильной поверхности алюминия, и протекает азотирование. При этом
образуется тонкая пленка нитрида алюминия, плохо проницаемая для азота.
Согласно исследованиям, проведенным в работе [30], целостность пленки нарушается лишь при температуре выше
1500°С. Для предотвращения этого
затруднения вместо азота предложено использовать очищенный аммиак:
Al + 2NH3 = 2AlN + 3H2 (6)
В этом случае на поверхности алюминия также образуется нитридная пленка,
но при температуре около 950°С целостность пленки нарушается, в результате чего реакция протекает
довольно быстро.
Таким образом, для ускорения реакции образования нитрида необходимо
использовать наиболее тонкие алюминиевые порошки, которые позволяют более полно
провести реакцию азотирования с образованием нитрида.
Такие нитриды алюминия с выходом 95-100% получают нагреванием
металлического алюминия в среде сухого очищенного азота при 400-1100°С в присутствии добавок
металлического лития, взятого в количестве 0,5-3% от веса Al.
Нитрид алюминия, не содержащий окиси алюминия, можно получить при
взаимодействии азота со смесями, состоящими из AlN(41,6-60%), AlF3
(17%), остальное - порошок алюминия. Азотирование проводят при 825 - 850°С. Затем при нагревании до 1400°С удаляют AlF3, который
возгоняется и сублимируется в отдельном сосуде. В конечном периоде реакции
температуру медленно повышают до 1900°С. При 1500°С азот заменяют аргоном для предотвращения чрезмерной эрозии реакционного
сосуда. В результате получают продукт, содержащий 97% нитрида алюминия, который
обладает меньшей твердостью, чем AlN, полученный другими способами.
Оценивая перечисленные выше методы азотирования порошкообразного
алюминия, следует отметить, что основным их недостатком является постоянное
загрязнение конечного продукта окисью алюминия. Это вполне закономерно, так как
уже исходный мелкодисперсный алюминий, обладая большой удельной поверхностью и
склонностью к окислению даже при низких температурах, всегда будет содержать
определенное количество окиси алюминия.
Дальнейшим развитием работ по непосредственному синтезу нитрида алюминия
из элементов явился процесс получения в электрической дуге, подробно описанный
в работе [31]. Полученный продукт содержит до 95%
AlN.
Нитрид алюминия удобно получать также через аммиакат фтористого алюминия
в среде аммиака при 1200 - 1400°С. Состав нитрида алюминия, полученного этим способом : 65,8 - 65,99% Al;
34,1 - 34,2% N, суммарное содержание примесей магния, кальция, кремния, бария,
железа, молибдена 0,03 - 0,04% [32].
Высокие физико-технические свойства нитрида алюминия - тугоплавкость,
электроизоляционные свойства, сохраняемые при высоких температурах, твердость и
высокая износостойкость, термостойкость, устойчивость в агрессивных химических
средах и расплавленных металлах и сплавах - делают его перспективным материалом
для высоких температур.
Известные огнеупорные свойства обеспечивают перспективы его использования
в качестве материала футеровок ванн, из AlN изготавливают тигли для плавки
металлов и выращивания полупроводниковых соединений [32].
Интересна и важна роль нитрида алюминия в сталях и железе. Показано, что
AlN обеспечивает в определенных условиях (до 0,08% N в форме дисперсного
нитрида) одновременное увеличение прочности, пластичности и улучшение
свариваемости стали.
1.4 Система ZrN-ZrO
В работах [33,34] были синтезированы кубические (типа
NaCl) оксинитриды ZrNzOy с малым содержанием кислорода
(от у=0,01¸0,04 до
0,1), тогда как, согласно [35], в системе Zr-N-O возможно
образование непрерывного ряда твердых растворов ZrN-ZrO.
Образцы ZrNzOy синтезировали высокотемпературным
(1500°С) вакуумным (10-5
мм.рт.ст.) спеканием брикетированных смесей исходных компонентов ZrO2,
Zr, ZrN0,76O0,14, ZrN0,87O0,12 в
течение 50ч.
Как видно из рисунка 3, область гомогенности кубического (типа NaCl) оксинитрида
ZrNzOy примыкает к стороне Zr-N концентрационного
треугольника Zr-N-O. Однофазному образцу с максимальным содержанием кислорода
соответствует состав ZrN0,72O0,31, а препарат состава ZrN0,65O0,36
двухфазный. Это соответствует представлениям [36,37] об ограниченной растворимости кислорода в ZrNz. Необходимо
отметить, что периоды решетки гексагонального твердого раствора a-ZrNzOy,
например, в образце состава ZrN0,10O0,92 (a=3,244A;
c=5,372A) заметно отличались от соответствующих чистому металлу (а=3,233А,
с=5,146А).
Кроме того, система ZrN-“ZrO” изучалась в работе [38], авторы которой при конечной температуре 1600 и 2000°С спеканием брикетированных смесей
исходных компонентов ZrN, “ZrO” в течение 12ч в среде аргона (р=400мм рт.ст.)
синтезировали смесь препаратов ZrNzOy c z+y»1 и исследовали последние методами
химического, рентгенографического и металлографического анализов. Установлено,
что образец с максимальной концентрацией кислорода содержал ~55 мол.% «ZrO».
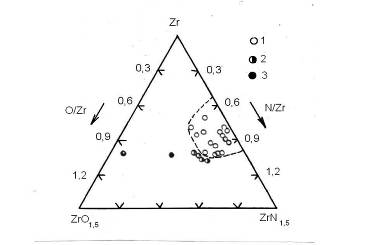
-однофазные образцы;
-двухфазные образцы;
-трехфазные образцы;
Рисунок3 - Фазовый состав системы Zr-N-O при 1500°С.
.5 Исследование взаимодействий в системе ZrO2-ZrN-AlN
В работе [39] были исследованы системы ZrO2-ZrN
и ZrO2-AlN
Для изучения взаимодействий в системе ZrO2-ZrN были
приготовлены составы через 10%мольных по следующей методике: образцы готовились
из порошков исходной дисперсности 15-20 мкм, перемешиванием исходных
компонентов в металлической ступке в среде этилового спирта в течение 15-20
минут. Затем образцы высушивались, пластифицировались 10% раствором каучука в
бензине и прессовались в виде таблеток диаметром 10мм и высотой 10мм.
Синтез образцов производился в среде азота в электрической печи
сопротивления при температуре 1840°С и изотермической выдержке 1 час. Далее образцы измельчались
в металлической лабораторной ступке до размеров менее 60мкм и отправлялись на
рентгенофазовый анализ.
С помощью автоматизированной системы IDENT4 были установлены следующие
фазы диоксид циркония кубический, нитрид циркония кубический, диоксид циркония
моноклинный.
В работе [39] говориться о взаимодействии с
образованием кубической фазы на основе ZrN , который является растворителем для
ZrO2 кубического. Подтверждением этого является смещение пиков
нитрида циркония в сторону больших углов.
Температуры термообработки 1840°С оказалось не достаточно для получения гомогенного твердого
раствора ZrNO. Скорее всего, с учетом имеющихся литературных данных, при
содержании ZrO2 более 10% мольных образование твердого раствора с
полным взаимным растворением компонентов невозможно.
При изучаемых в работе условиях термообработки образуется большое
количество кубического ZrO2 с небольшой долей моноклинной фазы, что
позволяет надеется на получение материалов с полностью кубической фазой ZrO2
без добавления стабилизаторов (например J2O3).
Количественный анализ пористости показал, что с ростом концентрации
нитрида циркония пористость увеличивается от 3%объемных для 10% ZrN до 15%
объемных при эквимолярном составе.
Для системы ZrO2-AlN анализ рентгенограмм термообработанных
смесей ZrO2-AlN, показал, что при 1840°С в системе количество Al2O3 не
увеличивается и практически отсутствует. Диоксид циркония находится в основном
в виде моноклинной модификации, количество кубической фазы диоксида циркония
незначительно. Исходный AlN плохо идентифицируется в продуктах термообработки,
на рентгенограммах присутствует в виде слабых пиков смещенных в сторону больших
углов. Высказывается предположение, что идет образование сложного вещества
оксинитрида алюминия.
Микроструктура спеченных материалов показала, что в системе ZrO2-AlN
пористость выше, причем она увеличивается с ростом содержания AlN. При
содержании AlN 40% и более прочность снижается и истинную пористость трудно
установить из-за сильного выкрашивания шлифа.
1.6 Планирование эксперимента при построении диаграмм состав-свойство
Для технолога большое значение представляет знание зависимости различных
свойств материала от состава. Оптимальной является ситуация, когда указанные
зависимости представлены в виде диаграмм состав - свойство. Все возрастающие
требования к материалам, получаемым методами керамической технологии, приводят
к увеличению числа компонентов в шихте или полуфабрикате, что влечет за собой
трудности в графической интерпретации диаграмм состав - свойство. Так, свойства
3-компонентой системы можно изобразить только в перспективном виде, и ее точное
прочтение становится затруднительным. Поэтому представляет интерес описание
зависимостей состав - свойство с помощью математических моделей в виде
полиномиального уравнения типа уравнения, где аргументами xi , ....., xj
являются концентрации компонентов. При этом отпадает необходимость в
пространственном представлении сложных поверхностей многокомпонентных систем,
так значение соответствующего свойства можно определить из уравнения простым
расчетом, либо для графического изображения зависимости построить, также
расчетным путем, линии равных значений на концентрационном треугольнике.
Построение диаграмм состав - свойство с помощью методов математического
планирования эксперимента сводится к следующей схеме:
выбор модели;
составление и реализация матрицы планирования;
вычисление коэффициентов уравнения;
проверка адекватности модели;
в случае адекватности модели - построение модели в виде линий равных
значений и расчет доверительных интервалов;
в случае неадекватности модели - переход к модели более высокой степени.
Выбор модели
Если система состоит из k независимых компонентов, то функцию изменения
какого либо свойства, как отмечалось выше, можно представить в виде
полиномиального уравнения (7):
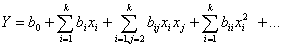 , (7)
, (7)
где:
Y - изучаемое свойство системы; х1, ..., хk -
концентрация компонентов в системе; bo, bi, ... -
коэффициенты уравнения.
Уравнение
(7) представляет собой полином n степени от k переменных и имеет число
коэффициентов b, равное числу сочетаний 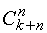 .
.
Шеффе
предложил описывать зависимости состав - свойство с помощью так называемых
приведенных полиномов на основании условия нормировки суммы независимых
переменных (8):
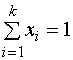 , (8)
, (8)
С
учетом нормированности суммы компонентов модель полного квадратичного приближения
для тройной системы описывается уравнением (9):
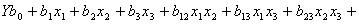
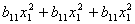 (9)
(9)
так
как 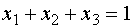 , то, умножив обе части уравнения на bо,
получим
, то, умножив обе части уравнения на bо,
получим
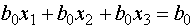 . (10)
. (10)
После подстановки (9) в (10) и преобразования получаем приведенный
полином
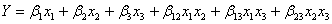 , (11)
, (11)
Число
коэффициентов, которые необходимо определить экспериментально, уменьшилось с 10
до 6. В таблице 1 представлены данные по числу опытов, которые необходимо
провести для построения математических моделей различной степени при
соответствующим числе компонентов.
Таблица
1 - Число опытов для получения моделей разных степеней для некоторых
многокомпонентных систем для случая приведенного полинома
|
Число компонентов (k)
|
Квадратичная модель, n=2
|
Кубическая модель, n=3
|
Модель 4-го порядка, n=4
|
Неполная кубическая модель, n=3
|
|
3
|
6
|
10
|
15
|
7
|
|
4
|
10
|
20
|
35
|
14
|
|
5
|
16
|
35
|
70
|
25
|
|
6
|
21
|
56
|
126
|
41
|
|
8
|
36
|
120
|
330
|
92
|
Поверхности отклика в многокомпонентных системах имеют, как правило,
достаточно сложный характер. Для описания таких поверхностей необходимы
полиномы высоких степеней и, следовательно, большое количество опытов. На
практике приходится выбирать между приемлемым числом опытов и достаточной
степенью полинома, которая, как привило, не превышает четвертую, а число
варьируемых компонентов ограничивают тремя - четырьмя. описаны отдельными
полиномами, относительно невысокой степени.
Таким образом, выбор модели сводиться к установлению числа варьируемых
компонентов рассматриваемой системы (если система содержит много компонентов,
то целесообразно часть из них задать постоянным количеством сверх 100% по
отношению к варьируемым, число которых ограничивают 3-4) и заданием степени
полинома, описывающего функцию отклика.
Так модель второй степени для 3-компонентной системы будет иметь вид,
соответствующий уравнению (11).
Модель неполной третьей степени -
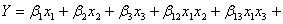
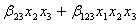 (12)
(12)
модель
третьей степени -
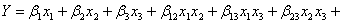
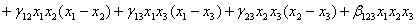 (13)
(13)
а
модель четвертой степени -
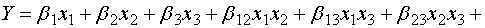

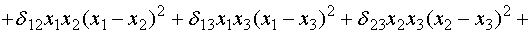
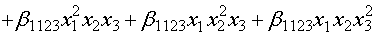 . (14)
. (14)
Составление и реализация матрицы планирования
По выбранной аналитической модели составляется матрица планирования, то
есть определяются те составы системы, экспериментальное исследование которых
поможет рассчитать коэффициенты модели. Количество составов должно быть не
меньше числа коэффициентов полинома выбранной модели, а расположение составов
на диаграмме - обеспечивать “одинаковую” точность определения коэффициентов для
всей системы. Решений о размещении экспериментальных точек может быть
множество, однако на практике наиболее широко применяются симплекс-решетчатые,
симплекс-центроидные планы Шеффе и некоторые другие.
Суть симплекс-решетчатого метода состоит в том, выбранные составы
располагаются в определенных местах симплекса, обозначаемого диаграмму составов
системы. По Н.С. Курнакову состав k - компонентной системы задается (k-1) -
мерным симплексом. Симплексом в общем случае называется простейшая
геометрическая фигура, образованная множеством (а+1) независимых точек в а
-мерном пространстве и обладающая минимальным количеством вершин. Шеффе
предложил размещать экспериментальные составы в определенных точках симплекса:
в вершинах, на середине ребер, в центре граней, в центре симплекса, в
зависимости от выбранной модели. Расположение точек на симплексе, получившее
название симплексной решетки для разных моделей представлено на рисунке 1.
Такое расположение отвечает требованию равномерного распределение точек, а
кроме того позволяет легко решать систему полученных уравнений для нахождения
коэффициентов полинома без применения сложного математического аппарата. Так
наличие экспериментальных составов в вершинах симплекса дает возможность
рассчитать коэффициенты bi. Например,
в i-вершине хi=1 остальные хj=0, следовательно, Yi=
bixi, откуда bi = Yi. Аналогично точки,
лежащие на середине ребер, помогают рассчитать коэффициенты bij и так далее. После выбора модели
переход к соответствующей симплексной решетке происходит автоматически, и
составление матрицы планирования сводится к определению состава
экспериментальных точек. Состав может быть задан в массовых долях, объемных,
мольных. Массовые дули удобны в плане дозировки компонентов. Именно поэтому
после определения составов в мольных или объемных долях следует сделать
перерасчет на массовые для определения состава шихты, соответствующей
определенной точке симплекса.
Пример составления матрицы планирования приведен в таблице 2.
Индексы у точек вводятся следующим образом:
их общее число равно степени полинома;
число неодинаковых индексов указывает на количество компонентов в данной
смеси;
число одинаковых индексов показывает долю компонента в смеси.
Симплексные решетки для трехкомпонентной системы
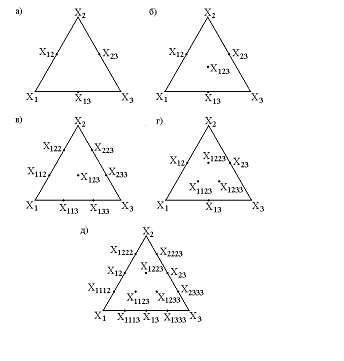
а - модель второй степени; б - модель неполной третьей степени; в -
модель третьей степени; г- модель неполной четвертой степени; д - модель
четвертой степени
Рисунок 4 - Симплексные решетки для трехкомпонентной системы.
Таблица 2 - Матрица планирования для трехкомпонентной системы,
соответствующая модели третьей степени
|
№ опыта
|
Обозначение состава
|
Объемное соотношение компонентов в долях
|
Массовое соотношение компонентов в долях
|
Значение функции отклика, Yi
|
|
|
х1
|
х2
|
х3
|
х1
|
х2
|
х3
|
|
|
1
|
х1
|
|
1
|
|
0
|
|
0
|
|
|
|
|
|
|
|
Y1
|
|
2
|
х2
|
|
0
|
|
1
|
|
0
|
|
|
|
|
|
|
|
Y2
|
|
3
|
х3
|
|
0
|
|
0
|
|
1
|
|
|
|
|
|
|
|
Y3
|
|
4
|
х112
|
|
0,667
|
|
0,333
|
|
0
|
|
|
|
|
|
|
|
Y112
|
|
5
|
х122
|
|
0,333
|
|
0,667
|
|
0
|
|
|
|
|
|
|
|
Y122
|
|
6
|
х223
|
|
0
|
|
0,667
|
|
0,333
|
|
|
|
|
|
|
|
Y223
|
|
7
|
х233
|
|
0
|
|
0,333
|
|
|
|
|
|
|
|
|
|
Y233
|
|
8
|
х113
|
|
0,667
|
|
0
|
|
0,333
|
|
|
|
|
|
|
|
Y113
|
|
9
|
х133
|
|
0,333
|
|
0
|
|
|
|
|
|
|
|
|
|
Y133
|
|
10
|
х123
|
|
0,333
|
|
0,333
|
|
0,333
|
|
|
|
|
|
|
|
Y123
|
Например, х1123 - это состав плана 4-й степени, три разных
индекса указывают на трехкомпонентную систему, всего индексов четыре (два раза
1 и по одному 2 и 3), следовательно, каждому индексу соответствует 0,25 (25%)
компонента, т.е. данный состав содержит 50% первого компонента и по 25% второго
и третьего.
Планы Шеффе обладают свойством композиционности, т.е. способностью
достраиваться до моделей более высоких степеней. Так переход от модели 2-й
степени до модели неполной 3-й степени требует постановки всего одного опыта в
центре симплекса (х123), а до неполной 4-й степени - трех опытов (х1123,
х1223, х1233).
Точки симплексных решеток не имеют физического смысла при построении
диаграмм состав - свойство, так как они могут только чисто случайно совпадать с
сингулярными точками.
После реализации соответствующего плана проводят вычисление коэффициентов
полинома и производят статистический анализ результатов эксперимента.
Для проверки полученной модели на адекватность необходимо знать
среднеквадратичную погрешность опыта. Для определения среднеквадратичной
погрешности опыта необходимо провести следующие расчеты:
. Для каждого из составов по данным r параллельных опытов определяется
среднее значение Tj.
. Вычисляется оценка дисперсии (S2) для каждой серии
параллельных опытов по формуле:
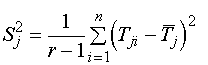 (15)
(15)
где i - номер опыта; j - номер состава.
. Вычисляется средняя дисперсия m серий параллельных опытов, т.н.
дисперсия воспроизводимости:
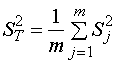 (16)
(16)
и
производится оценка дисперсии среднего значения:
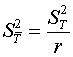 (17)
(17)
. Вычисляется среднеквадратичная погрешность опыта:
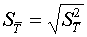 (18)
(18)
На
основании дисперсии опыта может быть рассчитана точность предсказания функции
отклика в какой-либо точке симплекса. За меру точности предсказания принимается
дисперсия предсказанного значения, которая рассчитывается по формуле:
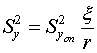 , (19)
, (19)
где
Sy2 - дисперсия предсказанного значения функции отклика;
S2yопыт - дисперсия опыта; r - число наблюдений в точке
симплекса, одинаковое для всех точек (в случае неодинакового числа наблюдений
расчет значительно усложняется); x - величина,
определяемая положением состава на симплексе.
Для
различных моделей тройных систем значения x берут с “контурных
карт”, а в случае их отсутствия и для систем с большим числом компонентов
рассчитывают по соответствующим формулам.
Проверка адекватности модели
Так как планы, используемые в методе симплексных решеток, являются
полностью насыщенными (число опытов равно числу определяемых коэффициентов
уравнения), то для проверки адекватности (соответствия реальной ситуации) не
остается степеней свободы. В связи с этим для проверки адекватности ставятся
опыты в контрольных точках. Количество точек и их расположение зависят от
интересующей исследователя области диаграммы, постановки задачи, сложности
опытов, экономических соображений и т.д. Общие рекомендации по выбору
контрольных точек сводятся к следующему: во-первых, к необходимости изучения
области симплекса представляющей наибольший интерес для исследователя, а
во-вторых, к возможности использования данных контрольных опытов (или части из
них) для перехода к модели более высокой степени. Например, при построении
модели неполной третьей степени в тройной системе необходимо определить
свойства у семи составов (см. рис.1) . В этом случае целесообразно провести
опыты еще в трех точках, соответствующих составам: х1123, х1223,
х1233. Для модели неполной третьей степени они будут проверочными, в
случае неадекватности этой модели три указанные точки помогут перейти к модели
неполной четвертой степени, а уже точка х123 станет проверочной.
Адекватность модели проверяется расчетом для контрольных точек значений
статистического критерия Стьюдента по формуле:
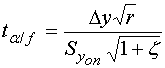 (20),
(20),
где
Dy = çyэксп - yрасч
ç- абсолютная величина разности между экспериментально
определенным и рассчитанным по модели значением свойства в контрольной точке; 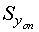 - среднеквадратичная ошибка опыта; a - уровень значимости (обычно a = 0,05), вероятностная
величина, показывающая, каков риск ошибиться в правильности гипотезы и связана
с Р - доверительной вероятностью, величиной определяющей степень вероятности
принимаемой гипотезы (a = 1- Р); f - число степеней свободы при определении
дисперсии опыта f=N·( r-1); N - число составов при определении дисперсии
опыта.
- среднеквадратичная ошибка опыта; a - уровень значимости (обычно a = 0,05), вероятностная
величина, показывающая, каков риск ошибиться в правильности гипотезы и связана
с Р - доверительной вероятностью, величиной определяющей степень вероятности
принимаемой гипотезы (a = 1- Р); f - число степеней свободы при определении
дисперсии опыта f=N·( r-1); N - число составов при определении дисперсии
опыта.
Полученная модель признается адекватной в случае tэксп < tтабл. Величина tтабл
берется из таблицы значений критерия Стьюдента для данного уровня значимости(a) и числа степеней свободы(f).
Менее строго можно сделать вывод об адекватности модели в случае, когда
величина çyэксп
- yрасч ç сравнима со среднеквадратичной погрешностью опыта.
Исследование локальных концентрационных участков системы
Во многих случаях для исследования представляет интерес не вся область
концентраций компонентов, а только ее часть. Для применения метода симплексного
планирования необходимо, чтобы локальный участок представлял бы собой симплекс
(треугольник, тетраэдр и т.д.) подобный исходному с вершинами Z1,
Z2, Z3. Если локальный участок
представлен другой фигурой, например, четырехугольником, то это может
существенно затруднить расчеты. Для системы с псевдокомпонентами также
справедливо условие нормировки.
Исследование локального участка, например, может иметь место при
исследовании свойств фарфоровых масс, где за исходные компоненты принимаются
составляющие шихты: глина (каолин), полевой шпат и кварц. Поскольку получить
фарфор, используя любой из компонентов в чистом виде невозможно, то исследуется
локальная область на основе псевдокомпонентов Z1 (состоящего из 20%
полевого шпата, 30% кварца и 50% глины), Z2 (состоящего из 30%
полевого шпата, 20% кварца и 50% глины) и Z3 (состоящего из 30%
полевого шпата, 30% кварца и 40% глины). Составление матрицы планирования в этом
случае сводится сначала к определению опытных составов в псевдокомпонентах, а
потом к пересчету на исходные компоненты.
Для удобства расчетов имеет смысл в полученных уравнениях перейти от
псевдокомпонентов к исходным компонентам Х1, Х2, Х3.
Целесообразно также представить результаты графически в виде проекций линий
равных значений физико-механических свойств на симплекс. Полученные зависимости
позволяют определить точку (область), соответствующую составу, который
характеризуется экстремальным значением оптимизируемого свойства. Может
получиться так, что исследуемая зависимость не носит экстремальный характер,
как это представлено на диаграмме состав-свойство (рисунок 2) для
характеристики прочности и теплопроводности керамического (глиняного) кирпича
при разном составе шихты. Но и в данном случае определение зависимости
состав-свойство имеет большое практическое значение, так как позволяет выбрать
состав для производства кирпича с допустимым значением прочности, но повышенной
теплопроводностью [40].
2. Цель и задачи работы
Целью данной работы является оценка возможности получения материалов в
системе ZrO2 - ZrN - AlN - Al2O3 c высокими
механическими свойствами.
Для выполнения поставленной цели необходимо решить следующие задачи:
анализ научно-технической литературы по двойным диаграммам состояния и
технологии получения материалов на их основе;
изучение взаимодействия в системах ZrO2 - AlN, ZrO2
- ZrN - AlN;
изучение физико-механических свойств полученных материалов.
3 Экспериментальная часть
.1 Характеристика исходных элементов
Для изучения системы ZrO2-ZrN-AlN использовались порошки
материалов, указанные в таблице 4.
Таблица 4 - Характеристика исходных веществ.
|
Наименование вещества
|
Химическая формула
|
Марка
|
ГОСТ, ТУ
|
|
Нитрид циркония
|
ZrN
|
ч
|
ТУ 6-09-4050-75
|
|
Оксид циркония
|
ZrO2
|
ч
|
ТУ 6-09-965-63
|
|
Нитрид алюминия
|
AlN
|
ч
|
-
|
Исходные вещества изучены методом рентгенофазового анализа, который
показал следующее.2
Диоксид циркония является моноклинной модификацией в виде бадделеита
(рисунок 5).
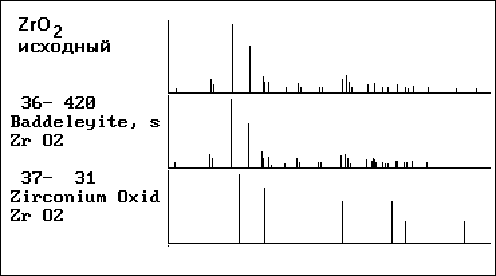
Рисунок 5 - Штрих-рентгенограмма исходного диоксида циркония
ZrN
В нитриде циркония присутствует примесь диоксида циркония (рисунок 6).
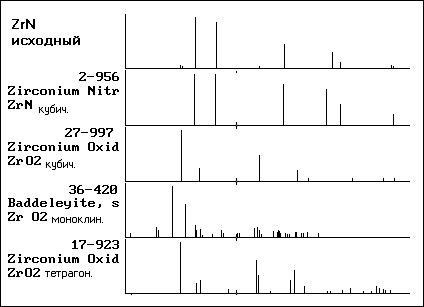
Рисунок 6 - Штрих-рентгенограмма исходного нитрида циркония
Полученный результат хорошо согласуется с литературными источниками. По
данным работы [15] при получении нитрида циркония восстановлением углеродом
диоксида циркония в среде азота:
2
+ 2C + 1/2 N2 ®ZrN
+ 2CO (21)
при температурах до 1300°С полученный продукт содержит кроме нитрида циркония 7-10% примеси,
нерастворимой в серной кислоте и состоящей из ZrO2 и некоторых
других загрязнений.
Исходный нитрид алюминия представлен в основном гексагональной фазой
(рисунок 7). Оксид алюминия в любых формах и металлический алюминий
отсутствуют. Кроме того, в качестве примесей в незначительном количестве
присутствуют гидратные формы оксида алюминия - бемит, гиббсит и байерит.
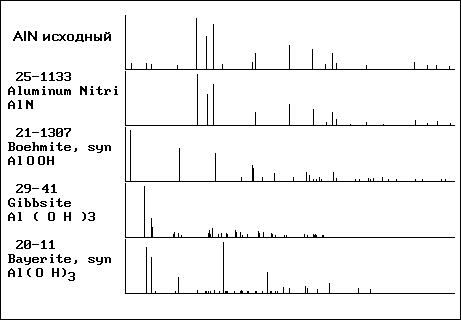
Рисунок 7 - Штрих рентгенограмма исходного нитрида алюминия.
Данный факт объясним, так как ультрадисперсный нитрид алюминия при
хранении вследствие высокой удельной поверхности окисляется, причем
образующийся такой же ультрадисперсный оксид алюминий активно взаимодействует с
парами воды воздуха.
Возможна и прямая реакция нитрида алюминия парами воды по схеме:
+ H2O = Al2O3×H2O +NH4OH
Подтверждением этого является исходящий от исходного нитрида алюминия
очень слабый запах аммиака.
В качестве вспомогательных использовались вещества и материалы, указанные
в таблице 5.
Таблица 5 - Вспомогательные вещества и материалы.
|
Наименование
|
ГОСТ, ОСТ, ТУ
|
Назначение
|
|
Спирт этиловый
|
C2H5OH
|
ГОСТ 18300-87
|
Среда для помола
|
|
Парафин
|
-
|
|
Пластификатор
|
|
Азот
|
N2
|
ГОСТ 9293-74
|
Среда для спекания
|
|
Сера элементарная
|
S
|
ТУ6-09-2546-77
|
Материал для заливки шлифов
|
|
Шлифовальные пасты
|
-
|
ГОСТ25593-83Е
|
Обработка шлифов
|
|
Шары твердосплавные из ВК6
|
WC+6%Co
|
ГОСТ3882-74
|
Мелющие тела
|
|
|
|
|
|
|
|
.2 Методика исследования
Для получения необходимых сведений об исследуемых материалах
определялись: фазовый состав, линейная усадка, плотность, пористость, твердость
по Виккерсу, коэффициент трещиностойкости и предел прочности при поперечном
изгибе.
.2.1 Рентгенофазовый анализ
Для рентгенофазового анализа синтезированных образцов твердого раствора
применялся метод порошка. Образцы измельчались в титановой ступке до размеров
частиц 60 мкм. Рентгенограммы снимались на рентгеновском дифрактометре ДРОН-3М.
Съемки осуществлялись со скоростью 4°/мин с использованием CuKa - излучения с Ni - фильтром.
Промер рентгенограмм проводился с точностью до 0,05 °. Расчет параметров решетки и
межплоскостных расстояний осуществляется на персональном компьютере по
программе «IDENT4»и «PDWin».
.2.2 Определение линейной усадки.
Усадка твердых сплавов при спекании определяется по формуле:
Y = ( ( l0 - l1 ) / l0 )*100%, [%], (21)
где l0 - длина отпрессованного образца до спекания, м;1
- длина образца после спекания, м .
.2.3 Определение плотности
Плотность спеченных твердых сплавов определялась в соответствии с
ГОСТ20018-74 по формуле:
r=mi*rb/(mi - mb), кг/м3, (22)
где mi - масса сухого образца, кг;
rb -
плотность воды, кг/м3;b - масса образца в воде, кг.
.2.4 Микроскопические исследования
Дисперсность порошков, пористость и средний размер зерен твердой фазы
спеченных твердых сплавов определялись на компьютерном комплексе с оптическим
металлографическим микроскопом МИМ-10 с помощью компьютерной программы
«ВидеоТест-3.2».
.2.5 Определение предела прочности при поперечном изгибе
Предел прочности при изгибе определялся на образцах 3´3´35 мм на установке, сконструированной НИИ ГИРИКОНД, в
соответствии с ГОСТ 20019-74.
Расчет велся по формуле:
s изг = P×К/b×h2 , МПа, (23)
где P - разрушающая сила, Н;
К - коэффициент базы испытаний;- ширина образца, м ;- высота образца, м .
.2.6 Определение твердости по Виккерсу
Твердость по Виккерсу определялась на шлифовальных образцах на приборе
ТВ. Измерения проводились в соответствии с ГОСТ 2999-75 при нагрузке 20 кг
(200Н).
Значение твердости по Виккерсу определялось по формуле:
V = 1,8544×P/d2,ГПа,
(24)
где Р - нагрузка, Н;- размер
диагонали отпечатка.
.2.7 Определение коэффициента
трещиностойкости или критического коэффициента интенсивности напряжений К1с
Определение К1с
проводилось по методу индентирования пирамидой Виккерса. Длина трещины
определяется с помощью оптического устройства твердомера ТП-7р-1 ГОСТ 23677-79
с точностью до 1 мкм. Для получения более достоверных результатов, численное
значение К1с определялось по двум формулам. По данным [41] К1с вычисляется по формуле:
К1с=0.035•а•Нv 3/5•E•Ф2/5/ Ф•l1/5, (25)
где а - половина диагонали
отпечатка, мкм;
Нv - твердость по
Виккерсу, Гпа;
Е - модуль Юнга, ГПа;
Ф - коэффициент
пропорциональности, для твердых сплавов Ф=3;- длина трещины, мкм.
Длина трещины l показана на
рисунке 8.
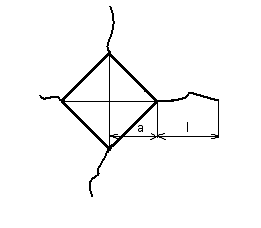
Рисунок 8 -
По данным [42] значение К1с определяется по формуле:
К1с= 0,00153×Нv×с2/а×а1/2, МПа×м1/2,
(26)
где Нv - твердость
по Виккерсу, ГПа;
с - половина диагонали
отпечатка, мкм;
а - длина трещины, мкм
Длина трещины a показана на
рисунке 9.
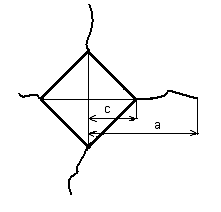
Рисунок 9.
3.2.9 Планирование эксперимента при построении
диаграмм состав - свойство
В приложении Д представлена программа расчета моделей
симплекс-решетчатого планирования эксперимента с построением линий равных
значений для IBM-совместимых компьютеров (среда программирования -
“Turbo-Basic”).
.2.10 Обработка результатов эксперимента
Обработка результатов эксперимента проводилась в
соответствии с СТП 2.075.008-81 по стандартным программам с использованием
персонального компьютера.
.3 Технология опытных образцов
Как было установлено ранее (см. аналитический обзор), при содержании
нитрида алюминия и нитрида циркония более 40% спеченные материалы обладают
повышенной пористостью и малой прочностью.
Вследствие этого, при изучении тройной системы (рисунок 10) было принято
решение ограничиться областью составов с содержанием ZrO2 60% и
более.
Нитрид алюминия, обладающий размером частиц менее 0,2 мкм, может оказать
влияние только при содержании не менее 5 % мас., таким образом, и по этому
компоненту вводилось ограничение по содержанию с интервалом 5-40%.
Таким образом, для реализации модели неполной третьей степени
симплекс-решетчатого планирования эксперимента для системы ZrN-AlN-ZrO2
была выбрана область составов в треугольнике (60% ZrO2 + 40% AlN) -
(95% ZrO2 + 5% AlN) - (60% ZrO2 + 5% AlN + 35% ZrN).
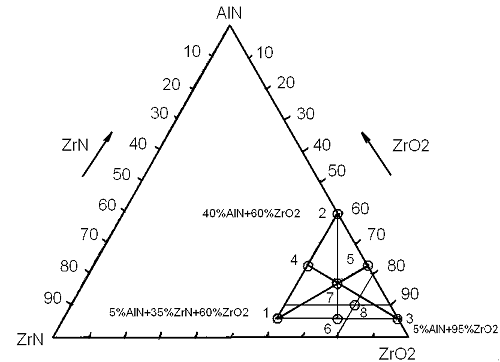
Рисунок 10 - План эксперимента модели неполной третьей степени в системе
псевдокоординат (5%AlN+20%ZrN+75%ZrO2) - (40%AlN+60%ZrO2) - (5%AlN+75%ZrO2)
Опытные составы в соответствие с планом эксперимента представлены в
таблице 6. Состав № 8 в план эксперимента не входил и использовался для
проверки адекватности модели.
Таблица 6 - Составы исследованных композиций в системе AlN + ZrN + ZrO2
|
№состава
|
Процентное содержание компонентов смеси, %
|
Количество компонентов смеси в расчете на 75 г каждого
состава, г
|
|
ZrO2
|
ZrN
|
AlN
|
ZrO2
|
ZrN
|
AlN
|
|
1
|
60
|
35
|
5
|
45
|
26,25
|
3,75
|
|
2
|
60
|
-
|
40
|
45
|
-
|
30
|
|
3
|
95
|
-
|
5
|
71,25
|
-
|
3,75
|
|
4
|
60
|
17,5
|
22,5
|
45
|
13,12
|
16,88
|
|
5
|
77,5
|
-
|
22,5
|
58,12
|
-
|
16,88
|
|
6
|
77,5
|
17,5
|
5
|
58,12
|
13,13
|
3,75
|
|
7
|
72
|
11,3
|
16,7
|
54
|
8,47
|
12,53
|
|
8
|
80
|
10
|
10
|
60
|
7,5
|
7,5
|
Исходные компоненты в указанных в таблице 6 соотношениях загружали в
вибромельницу для измельчения и перемешивания в среде этилового спирта. Время
измельчения 40 часов. Соотношение материал : шары : спирт = 1 : 10 : 1. Далее
шихту высушивали при температуре 70°С в вакуумном сушильном шкафу. Затем шихту отделяли от
мелющих тел, просеивая через решето с ячейкой 4 мм. В качестве пластификатора
использовали 8%-ный раствор парафина в бензине в количестве 4% мас. парафина по
сухому весу. Далее шихту протирали через сито с размером ячеек в свету 0,1 мм.
Из приготовленной шихты на гидравлическом прессе, под давлением 80 МПа,
прессовались образцы в виде палочек размером 3´3´35 мм.
Образцы спекались в графитовой печи в среде азота. Режим спекания был
выбран таким образом, чтобы обеспечить медленный нагрев образцов на стадии
выгорания пластификатора и полную дегазацию образцов (подъем температуры 400°С в час, выдержка при 600°С - 30 минут); осуществлялся контроль
по вакууму; затем напуск азота и нагрев до изотермической выдержки при
температуре спекания (1700°С, 1750°С и 1800°С); плавное охлаждение образцов для
снятия термических напряжений (3 часа).
На спеченных образцах определялись: усадка, плотность, предел прочности
при изгибе, твердость, трещиностойкость, микроструктура, по методикам описанным
выше.
.4 Рентгенофазовый анализ образцов после спекания
При проведении рентгенофазового анализа образцов в системе AlN - ZrN -
ZrO2 установлено следующее.
2
- AlN
При анализе рентгенограмм термообработанных смесей для системы ZrO2
- AlN подтвержден ранее установленный факт присутствия в продуктах реакции a-Al2O3 [39].
Диоксид циркония (рисунок 11) находится в виде кубической модификации.
Исходный AlN плохо идентифицируется в продуктах термообработки, на
рентгенограммах присутствует в виде слабых пиков смещенных в сторону больших
углов, что связано, скорее всего, с образованием сложного оксинитрида алюминия.
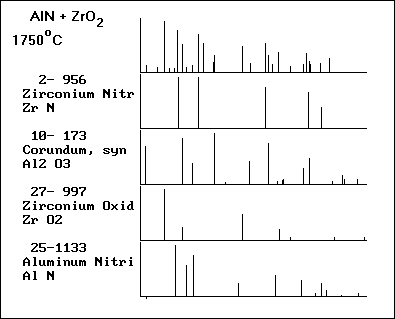
Рисунок 11- Штрих-рентгенограмма смеси 40% AlN + 60%Z rO2
после термообработки при 1750°С в среде азота
- ZrN - ZrO2
При анализе рентгенограмм термообработанных смесей для системы AlN - ZrN
- ZrO2 установлено, что в продуктах реакции идентифицируется
кубический нитрид циркония (рисунок 12).

Рисунок 12- Штрих-рентгенограмма смеси 40% AlN + 35% ZrN + 60% ZrO2
после термообработки при 1750°С в среде азота
Помимо этого присутствует кубическая модификация диоксида циркония и
примесь a-Al2O3.
Аналогично двойной системе ZrO2 - AlN исходный AlN плохо
идентифицируется в продуктах термообработки, на рентгенограммах присутствует в
виде слабых пиков смещенных в сторону больших углов
.5 Исследование свойств материала
Симплекс-решеточное планирование эксперимента реализовано по методике,
описанной разделе 1, с выбором в качестве основного плана эксперимента модели
неполной третьей степени, включающей 7 основных точек. Схема эксперимента в
системе псевдокоординат (5%AlN+20%ZrN+75%ZrO2)
- (40%AlN+60%ZrO2)
- (5%AlN+75%ZrO2) представлена на
рисунке 20. Составы исследованных композиций приведены в таблице 6. Состав 8 не
входил в план эксперимента и использовался для проверки уравнений регрессии на
адекватность.
Образцы для физико-механических испытаний изготавливали по
технологической схеме, описанной выше и спекали в при температуре 1700, 1750 и
1800оС в среде аргона.
Свойства изученных материалов представлены в таблице 20.
Таблица 20 - Свойства композиционных материалов в системе AlN + ZrN + ZrO2
|
№состава
|
Усадка, %
|
Плотность, г/см3
|
Пористость, % об.
|
|
1700оС
|
1750оС
|
1800оС
|
1700оС
|
1750оС
|
1800оС
|
1700оС
|
1750оС
|
1800оС
|
|
1
|
23,7
|
24,3
|
23,9
|
5,751
|
5,902
|
5,843
|
4,6
|
9,3
|
7,0
|
|
2
|
34,4
|
32,1
|
35,9
|
4,175
|
4,557
|
4,599
|
25,9
|
24,4
|
|
|
3
|
25
|
24,3
|
24,2
|
5,796
|
5,705
|
5,678
|
5,2
|
5,0
|
|
|
4
|
30,5
|
29,7
|
30,4
|
4,755
|
5,014
|
5,115
|
14,3
|
13,0
|
10,0
|
|
5
|
30,7
|
31,2
|
32,2
|
5,045
|
5,265
|
5,098
|
25,1
|
7,4
|
|
|
6
|
23,3
|
24,1
|
23,9
|
5,583
|
5,798
|
5,705
|
8,8
|
5,1
|
4,2
|
|
7
|
28
|
28,8
|
28,6
|
5,371
|
5,210
|
4,957
|
29,0
|
7,2
|
|
|
8
|
25,7
|
26
|
25,7
|
5,201
|
5,201
|
5,087
|
11,6
|
6,0
|
|
Предел прочности при изгибе определяется для каждого состава и
температуры спекания минимум по шести образцам. Результаты обрабатывались в
соответствии с планом эксперимента по программе на языке Basic и представлены в
приложении №. В программе рассчитываются коэффициенты регрессии в уравнении
зависимости свойств от состава, проводится проверка адекватности принятой
модели (по составу № 8).
После проверки коэффициентов регрессии на значимость и оценки
доверительных интервалов уравнения регрессии для предела прочности при изгибе
для различных температур спекания (1700оС, 1750оС, 1800оС
соответственно) выглядели следующим образом:
1700=820X1+268X2+303X3-1260X1X2-01X1X3+216X2X3+2350X1X2X3
(31)1750=768X1+637X2+495X3-685Х1X2-1019X1X3-26X2X3+2873X1X2X3
(32)1800=497Х1+370X2+242X3-47X1X2+472X1X3+963X2X3-
2464X1 X2X3 (33)
По уравнениям (31-33) построены линии равных значений прочности при
изгибе в пределах изученной области концентраций при всех температурах спекания
(рис.48-50).
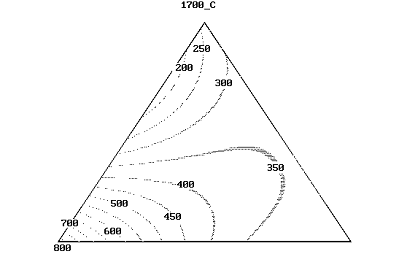
Рисунок 48 - Линии равных значений предела прочности при поперечном
изгибе композиционных материалов в системе AlN + ZrN + ZrO2
при температуре спекания 1700°С
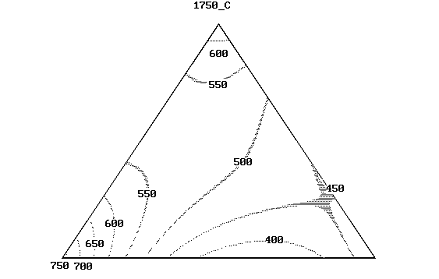
Рисунок 49 - Линии равных значений предела прочности при поперечном
изгибе композиционных материалов в системе AlN + ZrN + ZrO2
при температуре спекания 1750°С
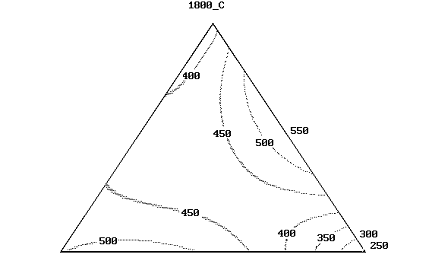
Рисунок 50 - Линии равных значений предела прочности при поперечном
изгибе композиционных материалов в системе AlN + ZrN + ZrO2 при температуре спекания 1800°С
Аналогичной обработке подвергались данные по усадке. При всех
температурах спекания наблюдается тенденция увеличения усадки с ростом содержания
нитрида алюминия (рисунки 51-52).
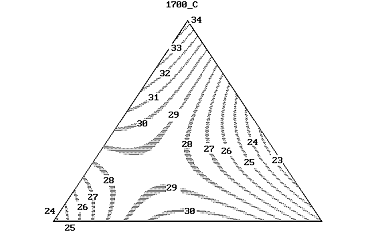
Рисунок 51 - Линии равных значений усадки композиционных материалов в
системе AlN + ZrN + ZrO2 при температуре
спекания 1700°С
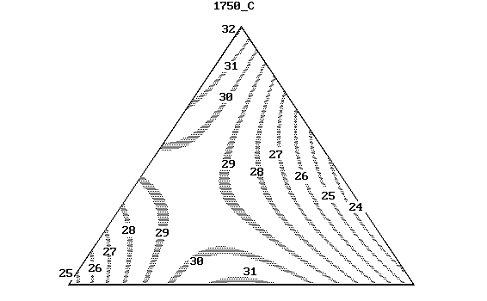
Рисунок 52 - Линии равных значений усадки композиционных материалов в
системе AlN + ZrN + ZrO2 при температуре
спекания 1750°С
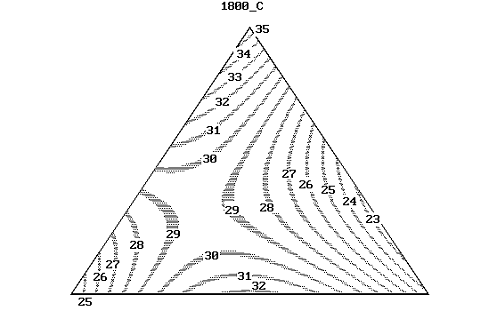
Рисунок 53 - Линии равных значений усадки композиционных материалов в
системе AlN + ZrN + ZrO2 при температуре
спекания 1800°С
На отдельных образцах определена твердость по В и К1С.
Результаты
Микроструктура композиционных материалов при увеличении 1200´ представлена на рисунках 54-56.

Состав
1

Состав
3

Состав
5

Состав
7
Рисунок 54 - Микроструктура композиционных материалов в системе AlN + ZrN + ZrO2 при температуре спекания 1700°С (увеличение 1200´)

Состав1

Состав
3

Состав5

Состав
7
Рисунок 55 - Микроструктура композиционных материалов в системе AlN + ZrN + ZrO2 при температуре спекания 1750°С (увеличение 1200´)
|
 
|
|
|
Состав 1
|
Состав 4
|
|

|
|
Состав 6
|
|
Рисунок 56 - Микроструктура композиционных материалов в
системе AlN + ZrN + ZrO2 при температуре спекания 1800°С (увеличение 1200´)
|
Размер зерна
Таблица№ - Размер зерен фазовых составляющих материалов в системе
AlN-ZrN-ZrO2
|
№ состава
|
Размер зерна ZrN, мкм
|
Размер зерна ZrO2, мкм
|
Размер зерна AlN, мкм
|
|
Tспек = 1700°С
|
|
1
|
3,0548
|
6,4821
|
3,6999
|
|
2
|
3,2384
|
7,0289
|
5,6597
|
|
3
|
2,9318
|
9,0482
|
2,6794
|
|
4
|
3,3127
|
10,4053
|
5,0272
|
|
5
|
2,7618
|
10,9146
|
5,4778
|
|
6
|
2,8128
|
10,1750
|
2,7249
|
|
7
|
2,7568
|
12,6626
|
4,1013
|
|
8
|
3,2637
|
12,0759
|
3,7577
|
|
Tспек = 1750°С
|
2,7329
|
8,8735
|
4,8673
|
|
2
|
3,2035
|
8,1741
|
12,0582
|
|
3
|
2,9518
|
11,6098
|
5,3028
|
|
4
|
3,5610
|
8,3425
|
7,9872
|
|
5
|
3,2251
|
8,4688
|
5,0002
|
|
6
|
3,5240
|
9,7686
|
5,9198
|
|
7
|
3,5957
|
11,6594
|
7,8740
|
|
8
|
2,7497
|
8,5287
|
7,1713
|
|
Tспек = 1800°С
|
|
1
|
3,6865
|
6,7503
|
4,8840
|
|
4(1)
|
3,3923
|
9,3762
|
6,2230
|
|
4(2)
|
3,8748
|
17,0883
|
10,6976
|
|
6
|
3,0270
|
6,2401
|
4,6485
|
Таблица № - Твердость по Виккерсу и коэффициент интенсивности критических
напряжений K1C для материалов в системе AlN-ZrN-ZrO2
|
Номер состава
|
Hv, ГПа
|
К1С, МПа×м1/2
|
К1С, МПа×м1/2
|
|
Состав1
|
10,3
|
18,1
|
11,5
|
|
Состав2
|
12.3
|
17,5
|
11,2
|
|
Состав4
|
11,0
|
17,7
|
11,3
|
|
Состав7
|
9,4
|
19,7
|
10,7
|
Список использованных источников
1. Иманов
Г.М., Козловский Л.В., Ротенберг Б.А. Технология керамических конденсаторов. -
Издательство «ООО» ОМ-ПРЕСС», Санкт-Петербург, 2004 г.,с.232.
2. Рутман
Д.С., Торопов Ю.С., Плинер С.Ю. Высокоогнеупорные материалы из диоксида
циркония. М.: Металлургия, 1985, с. 136.
. Рутман
Д.С., Торопов Ю.С., Плинер С.Ю. Высокоогнеупорные материалы из диоксида
циркония. М.: Металлургия, 1985, с. 136.
. Wong
A., Mc Pherson J.P. - J. Mater. Sci., 1979, v. 14, № 3, p. 680-686.
. Chem.
And Eng. News, 1971, v. 49, № 35, p. 20.
. Javorsky
P.J. - Ceram. Age, 1962, v. 78, № 6, p. 64-69.
. Химическая
технология керамики: Учеб. пособие для вузов/ Под ред. проф. И.Я. Гузмана. -
М.: ООО РИФ «Стройматериалы», 2003. - 496., ил.
. Наумов
И.И., Ольховик Г.А., Великохатный О.И., Апаров Н.Н. Электронная структура и
характер связи в кубическом диоксиде циркония , содержащие кислородные вакансии
и ионы кальция .// Препринт ИФПМСО АН СССР , Томск. - 1990. - N17.- 16с.
. Оксид
циркония . Тезисы докладов всесоюзной конференции . Звенигород, 23 - 25
сентября 1991 г. Л.: Наука , 1991.
. Воронько
Ю.К. , Зуфаров М.А. , Осико В.В. , Соболь А.А. , Спиридонов Ф.М. Фазовые
превращения в твердых растворах на основе диоксида циркония. - М.: Наука ,
1983.
11. Попова
О.И., Кабанник Г.Т. Кислотоустойчивость и методы анализа нитридов Ti, Zr, Nb и
Ta.- Журн. Неорг. Химии, 1960, т. 5, №4, с. 930-934.
12. Glasson
D.R., Jayaweera S.A.A. Formation and reactivity of nitrides. II Calcium and
magnesium nitrides and calcium cyanamide. IV Titanium and zirconium nitrides. -
J. Appl. Chem., 1968, vol. 18, №6, p. 182-184; p. 77-83.
. Киффер
Р., Бенезовский Ф. Твердые материалы. Пер. с нем. М., «Металлургия», 1968.
384с.
. Верхоглядова
Т.С., Дубовик Т.В., Самсонов Г.В. Азотирование порошков переходных металлов с
образованием нитридных фаз. - Порошковая металлургия, 1961, №4, с. 9-20.
. Меерсон
Г.А., Рой С. Исследование условий получения нитрида и гидрида циркония
непосредственно из двуокиси. - Порошковая металлургия, 1963, №6, с. 71-77.
16. Тот Л.
Карбиды и нитриды переходных металлов. М.: Мир. - 1974. - 294 с.
17. Rudy
E., Benesovsky F. The system Hf-B-N and Zr-B-N - Monatsheft Chem. - 1961. - Bd
92, №2. - P.415-441.
. Ероньян
М.А., Аварбэ Р.Г., Никольская Т.А. Влияние давления азота на температуру
плавления ZrNx/ Изв. АН СССР. Неорганические материалы. - 1976. - т.
12. - № 2. - с. 247-249.
19. Mallott
M. of al. - J. Electrochem. Soc., 1953, 100, 103.
20. Bar
J. Dl., Fast J. -Ree. Trans.Electrochem. Soc., 1948, 93, 223.
. Domagala
R., Pherson D.Mc., Hansen M. - J. Metals, 1953.
. Самсонов
Г. В. Нитриды. - Киев: Наук. Думка, 1969. - 377с.
. Guladner
W., Wooten L. - Trans. Chem., 1939, 55, 459.
. Ja
za R., Robenau A., Nitschke J. - Z. anorg. Chem., 1964, 332, 136.
. Самсонов
Г.В. Неметаллические нитриды. М.: Металлургия, 1964, 264с.
26. Олейник
Г.С., Шевченко О.А., Кузнецова М.А. Механизм формирования самоармированных AlN
- материалов// Электрон. микроскопия и прочность материалов. - Киев, 1994, с.
78-93.
27. Neuenschwander
E. Herstellung und Characteristerung ion ultrafeiren Karbiden, Nitriden und
Metallen. - J. Less - Conemon Metals, 1966, vol.11, №5, p.365-375.
. Long
G., Foster L.M. Aluminium nitride containers for the synthesis of GaAs. - J.
Electrochem. Soc, 1962, vol. 109, № 12, p. 1176-1180.
29. Бусев А.
Нитриды. - Учен. зап. Ленингр. пед. ин-та, 1940, т. 29, с. 303-336.
30. Rabenau
A. Preparation of aluminium and gallium hydrides. - In: Compound semicon
doctors. Ed. by R. Willardson, H. Baring. Vol. 1. N. J., Reinhold pabl. Corp.,
L. Chapman and Hall, Ltd., 1962, p. 174-189.
. Lejus
A. - M., Thery J., Gilles J. - C., Collongues R. Sur la preparation et les
proprietes du nitrure d‘aluminium. - Compt. Rend., 1963, vol.257, №1, p. 157-160.
. Андреева
Т.В., Горячев Ю.М., М. Диэлектрики и полупроводники// Киев: Высшая школа, 1974.
Вып. 6, с. 101-103.
33. Смагина
Е.И., Куцев В.С., Ормант Б.Ф. Зависимость теплот и свободных энергий
образования нитридов циркония от состава и строения. - Докл. АН СССР, 1957,
т.115, № 2, с. 354-357.
34. Смагина
Е.И., Куцев В.С., Ормант Б.Ф. Исследование равновесия в системе Zr-N при
высоких температурах. - Ж. физ. хим., 1960, т. 34, № 10, с. 2328-2335.
. Шевченко
А.С., Андреевский В.А., Калинин В.П., Лютиков Р.А. Изучение ренткеновской и
пикнометрической плотностей фаз внедрения на основе циркония. - Порошк.
металлургия, 1970, № 1. с . 89-91.
. Schoberg
N. Ternary Metallic Phases in the Ta-C-N, Ta-C-O and Ta-N-O Sistems. - Acta.
Chem. Scand., 1954, vol.8, № 3, p. 620-623.
. Швейкин
Г.П., Алямовский С.И., Гельд П.В. О некоторых закономерностях образования
трехкомпонентных фаз внедрения в системах Me-C-N, Me-C-O, Me-N-O с участием
переходных металлов IV-V групп. Свердловск: УКРАН СССР, 1966, вып. 9. с. 9-16.
. Constant
K., Kieffer R., Ettmayer P. Uber das pseudoternare System «ZrO»-ZrN-ZrC. -
Monatsheft, Chem., 1975, bol. 106, № 4, s. 823-830.
. Лебедева
О.Е. Разработка износостойкой керамики на основе AlN-ZrO2-ZrN:
Дипломная работа/СПбГТИ. - СПб. - 2004. - 65 с.
. Методы
математического планирования эксперемента в технологии керамики. Лит. указ. -
Л., 1981. - с. 33.
. Механические
свойства карбида хрома и покрытий из сплавов на его основе/ Клименко В.И.,
Маслюк В.А., Каюк В.Г., Пушкарев О.И. - Порошковая металлургия. - 1988. - №1 -
с. 64-68.
. Орданьян
С.С., Семенов С.С., Пантелеев И.Б. Лабораторный практикум по керметам: Учеб.
пособие/ ЛТИ им. Ленсовета. - Л.;1987. - 86 с.
. Глаговский
Б.А., Московенко И.Б. Низкочастотные акустические методы контроля в
машиностроении. - Л: Машиностроение.-1977.- 208 с.
. Правила
устройства электроустановок.- М.: Главгосэнергонадзор России, 1998.- 607 с.
. Кирюшкин
А.А., Капитоненко З.В., Ивахнюк Г.К. Охрана труда и окружающей среды: Метод.
Указания к дипломному проекту. СПб.: СПБГТИ(ТУ).- 2005.- 27с.
. Охрана
труда в химической промышленности/ Г.В. Макаров., А.Я Васин., Л.К. Маринина и
др.- М.: Химия.- 1989.- 496 с.
. Захаров
Л.Н. Техника безопасности в химической лаборатории.-Л.: Химия.-1991.- 336 с.
. Справочник
по оказанию скорой и неотложной помощи. Под. ред. Е.И. Чазова. Изд. 3-е,
стереотипное. М., «Медицина», 1977, с. 672.
Приложения
Приложение А
Оформление дипломной работы выполнялось в соответствии с требованиями
ГОСТ 7.32-2001 «Отчет о научно-исследовательской работе. Структура и правила
оформления» и в соответствии с СТП СПбГТИ 017-97 «КС УКДВ. Виды учебных
занятий. Положение о выпускной квалификационной работе дипломированного
специалиста (инженера). Общие требования».
Нормативная документация, использованная в ходе выполнения дипломной
работы, представлена в таблице.
Таблица - Перечень нормативных документов.
|
Обозначение нормативного документа
|
Наименование нормативного документа
|
|
ГОСТ 7.1- 84
|
СИБИД. Библиографическое описание документа. Общие
требования и правила составления.
|
|
ГОСТ 7.32-2001
|
СИБИД. Отчет о научно-исследовательской работе. Структура и
правила оформления.
|
|
ГОСТ 7.9-95
|
СИБИД. Реферат и аннотация.
|
|
ГОСТ 8.417- 81
|
ГСИ. Единицы физических величин.
|
|
ГОСТ 12.1.007-76 ССБТ
|
Вредные вещества. Классификация и общие требования
безопасности.
|
|
ГОСТ 12.1.005- 88 ССБТ
|
Общие санитарно- гигиенические требования к воздуху рабочей
зоны.
|
|
ГОСТ 12.4.021- 75 ССБТ
|
Системы вентиляционные. Общие требования.
|
|
ГОСТ 20018-74
|
Сплавы твердые спеченные. Метод определения плотности
|
|
ГОСТ 18300-87
|
Спирт этиловый ректификованный технический. Технические
условия
|
|
ГОСТ 9293-74
|
Азот газообразный и жидкий. Технические условия
|
|
ГОСТ 25593-83Е
|
Материалы шлифoвальные. Классификация. Зернистость и
зерновой состав. Методы контроля
|
|
ГОСТ 3882-74
|
Сплавы твердые спеченные. Марки
|
|
ГОСТ 20019-74.
|
Сплавы твердые спеченные
|
|
ГОСТ 2999-75
|
Металлы и сплавы. Метод измерения твердости по Виккерсу
|
|
ГОСТ 23677-79
|
Твердомеры для металлов. Общие технические требования
|
|
ТУ 6-09-2546-77
|
Сера Элементарная с содержанием основного вещества 99,999 %
|
|
СТП 2.054.011- 82
|
Порядок проведения патентного исследования.
|
|
СНиП 23- 05- 95
|
Естественное и искусственное освещение производственных
помещений. Нормы проектирования.
|
|
НПБ 105- 03
|
Общие санитарно- гигиенические требования к воздуху рабочей
зоны.
|
Приложение Б
Охрана труда и окружающей среды
Работа в химической лаборатории, на предприятиях никогда не относилась к
категории безопасных.
Необходимый уровень безопасности и безвредности труда в сфере науки и
производства призвана обеспечить система охраны труда.
Проблема сохранения здоровья трудящихся решается следующими аспектами
охраны труда:
· Правовые и организационные вопросы охраны труда;
· Производственная санитария и гигиена труда;
· Техника безопасности;
· Пожарная безопасность.
Опасные и вредные производственные факторы
При выполнении работы в лабораториях наиболее вредными для человека
факторами являются: движущиеся механизмы и их элементы; повышенный уровень
шума; высокие температуры при обжиге образцов; наличие в воздухе
высокодисперсной пыли.
Группа химически опасных и вредных производственных факторов обязана
вредному воздействию на организм человека различного сырья. Характеристика
веществ, используемых в дипломной работе и характер их воздействия на организм
человека, представлены в таблице 1.
Содержание вредных веществ в воздухе рабочей зоны определялось по ГОСТ
12.1.005-88 ССБТ.
По степени воздействия на организм человека вещества подразделяются на
следующие классы:
1. чрезвычайно опасные;
2. высокоопасные;
. умереннооиасные;
. малоопасные.
Класс опасности веществ определен по ГОСТ 12.1.007-76 ССБТ.
Таблица1- Характеристика физико-химических, пожаровзрывоопасных и
токсичных свойств сырья.
|
Вещества
|
Физико-химические свойства
|
Пожаровзрывоопасные свойства
|
Токсические свойства
|
|
|
Агрегатное состояние
|
T кип, 0С
|
Tпл, 0С
|
Плотность, кг/м3
|
Температура, 0С
|
Пределы распространения пламени
|
Характер действия на организм человека
|
Класс опасности
|
ПДК р.з., мг/м3
|
|
|
|
|
|
|
Вспышки
|
Самовоспламенения
|
Температурные, 0С
|
Концентрационные, об. %
|
|
|
|
|
|
|
|
|
|
|
|
Нижний
|
Верхний
|
Нижний
|
Верхний
|
|
|
|
|
AlN(нитрид алюминия)
|
а
|
Возгорание 2000°
|
2200(0,4МПа)*
|
3,26
|
Пожаро - и взрывобезопасен
|
Аэрозоль обладает фиброгенными свойствами, раздражает
слизистые оболочки глаз.
|
4
|
6
|
|
ZrO2(диоксид циркония)
|
а
|
4300
|
2700*
|
5,85
|
Пожаро - и взрывобезопасен
|
Аэрозоль обладает фиброгенными свойствами, раздражает
слизистые оболочки глаз.
|
4
|
6
|
|
ZrN(нитрид циркония)
|
а
|
-
|
2990
|
7,09
|
Пожаро - и взрывобезопасен
|
Аэрозоль обладает фиброгенными свойствами, раздражает
слизистые оболочки глаз.
|
3
|
4
|
|
Вещества
|
Физико-химические свойства
|
Пожаровзрывоопасные свойства
|
Токсические свойства
|
|
|
Агрегатное состояние
|
T кип, 0С
|
Tпл, 0С
|
Плотность, кг/м3
|
Температура, 0С
|
Пределы распространения пламени
|
Характер действия на организм человека
|
Класс опасности
|
ПДК р.з., мг/м3
|
|
|
|
|
|
|
Вспышки
|
Самовоспламенения
|
Температурные, 0С
|
Концентрационные, об. %
|
|
|
|
|
|
|
|
|
|
|
|
Нижний
|
Верхний
|
Нижний
|
Верхний
|
|
|
|
|
|
Бензин
|
ж.
|
33,37
|
-60,6
|
7209,3
|
-35
|
10
|
-30
|
10
|
0,65
|
8,04
|
Общетоксическое, сенсиби- лизирующее воздействие на ЦНС,
наркотик I
типа
|
100
|
4
|
|
|
ВТС КМ5026
|
тв.
|
-
|
56
|
890
|
-
|
-
|
-
|
-
|
-
|
-
|
Мелкодисперсная пыль не токсична, поражает легкие
|
0,5
|
2
|
|
|
Сера
|
тв.
|
444,6
|
119
|
2070
|
207
|
232
|
-
|
-
|
35
|
-
|
Пары серы токсичны, вызывают отравление организма
|
2
|
3
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Категория помещений по взрывопожарной и пожарной опасности
Химическая лаборатория относится к В1-В4, пожароопасной, так как в
лаборатории находятся трудногорючие вещества и материалы (пыль).
По классу взрывоопасной зоны - к В-1б, в соответствии с [44]. В
лаборатории горючие газы и ЛВЖ находятся в количестве, не превышающем 5 %
свободного объема помещения. К тому же, при необходимости, работа с горючими
газами и ЛВЖ производится под вытяжными зонтами.
Для уточнения категории помещения, необходимо рассчитать пожарную
нагрузку согласно НПБ 105-03.
Расчет пожарной нагрузки
Удельная пожарная нагрузка рассчитывается по формуле:
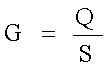 ,
,
гдеплощадь
размещения пожарной нагрузки, м2;пожарная нагрузка, МДж/м2
Формула
для расчета пожарной нагрузки:

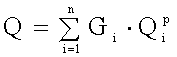 .
.
где
 Gi-количество
i-го материала пожарной нагрузки, кг;
Gi-количество
i-го материала пожарной нагрузки, кг;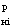 - низшая
теплота сгорания i-го материала пожарной нагрузки, МДЖ/кг.
- низшая
теплота сгорания i-го материала пожарной нагрузки, МДЖ/кг.
В
лабораторном помещении находятся: 2 стола из деревостружечного материала массой
по 16 кг; 2 стенда из аналогичного материала массой по 10 кг; 1книжная полка
массой 20 кг; 3 скамейки из ДСП массой по 12 кг; 2 хлопчатобумажные шторы по 5
кг, 1 доска из стеклопластика массой 25 кг, бумага массой 40 кг.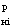 1=16,6
МДж/кг- для материала столов, стендов, скамеек, книжной полки; Q
1=16,6
МДж/кг- для материала столов, стендов, скамеек, книжной полки; Q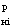 2=15,7
МДж/кг- для материала штор; Q
2=15,7
МДж/кг- для материала штор; Q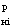 3=25,1 МДж/кг- для доски; Q
3=25,1 МДж/кг- для доски; Q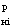 4=13,4
МДж/кг- для бумаги.
4=13,4
МДж/кг- для бумаги.
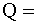 32
32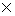 16,6+10
16,6+10 15,7+20
15,7+20 16,6+36
16,6+36 16,6+25
16,6+25 25,1+40´16,6+13,4´40=3445,3 МДж
25,1+40´16,6+13,4´40=3445,3 МДж
Принимаем
S=12 м2
G=3445,3
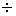 12=287,1 МДж/м2
12=287,1 МДж/м2
Сравнивая
полученные значения G=287,1 МДж/м2(181<287,1<1400) с
приведенными в таблице НПБ, помещение относится к категории В3.
Вентиляция
Концентрация
выделяющейся пыли может превышать нормы ПДК, поэтому лаборатории оснащены
обще-обменной приточно-вытяжной вентиляцией. Кратность воздухообмена для
вентиляции К = 1,5 ч-1 при температуре помещения 18 °С. Кроме того, в лаборатории имеется местная вентиляция - вытяжной шкаф
= 1-2 м/c.
Скорость
движения воздуха в рабочем пространстве: 0,8-1,5 м/с. При выборе вентиляционных
устройств учитывается предельно-допустимая концентрация вредных веществ рабочей
зоны. Кратность воздухообмена для местной вентиляции К = 350 ч-1 [45].
Освещение
Помещения с постоянным пребыванием людей должны иметь, как правило,
естественное освещение.
Естественное освещение подразделяется на боковое, верхнее и
комбинированное (верхнее и боковое).
Норма освещенности зависит от разряда зрительных работ, который
устанавливается по наименьшему размеру объектов различения.
При зрительной работе средней точности, размер объекта различения
составляет 0,5-1,0 мм. Разряд зрительной работы при этом 4 г.
В соответствии с вышеизложенным был определен коэффициент естественного
освещения, он составляет eн=4%.
Норма освещенности рабочего места при комбинированном освещении составит
300 лк согласно СНиП 23-05-95.
Освещение в лаборатории осуществляется люминесцентными лампами и боковым
светом.
Аптечка и ее содержание
В лабораторных помещениях предусмотрена аптечка универсальная. Аптечка
содержит:
Болеутоляющие средства: жаропонижающие, противовоспалительные,
успокаивающие, отхаркивающие; средства, применяемые при болях в
желудочно-кишечном тракте, валидол при болях в сердце, раствор аммиака для
вдыхания при обмороке, антисептические средства, используемые для промывания
ран, для смазывания ссадин, царапин, краев ран.
Перевязочные средства - перевязочный пакет, стерильные бинты, вата,
бактерицидный пластырь, резиновый кровоостанавливающий жгут, ванночка для
промывания глаз.
Помимо этого, обязательно наличие в лаборатории средств индивидуальной
защиты.
Для работы в лабораторных условиях предусмотрены следующие средства
индивидуальной защиты:
хлопчатобумажный халат для защиты от загрязнений;
резиновые перчатки для защиты кожи рук;
очки открытого типа, щиток с прозрачным экраном для защиты глаз;
респиратор “ лепесток ” типа У-2К для защиты органов дыхания;
- диэлектрические перчатки, резиновые коврики, для защиты от поражения
электрическим током [46].
Классификация помещений по возможности поражения
человека электрическим током
По возможности поражения электрическим током помещения лабораторий
относятся к классу помещений повышенной опасности, т.к. в лаборатории имеется
электрооборудование. Относительная влажность воздуха не превышает 75%,
температура воздуха T = +18-20 °С.
Электробезопасность
В данной дипломной работе электрооборудование использовалось на стадиях
помола, сушки, обжига. Для защиты от поражения электрическим током в условиях
лабораторий применяется защитное заземление всех видов электрооборудования. Так
как максимальное напряжение не превышает 500 В, сопротивление защитного провода
не превышает 4 Ом. Кроме того, постоянно контролируется исправность изоляции
токопроводящих частей установок.
Анализ технологических операций
При проведении исследований в рамках дипломной работы, на различных
стадиях технологии могут возникнуть опасные и вредные последствия. В настоящее
время большинство заводов по производству изделий из керамики являются
автоматизированными. В связи с чем, уровень опасности и вредности при
организации тех или иных технологических операций с точки зрения опасностей и
вредностей в рамках лаборатории.
Таблица 2- Анализ технологических операций с точки зрения опасностей и
вредностей при их проведении.
|
Наименование технологических операций
|
Оборудование д/проведения операций
|
Реактивы, необходимые д/проведения операции
|
Возможные опасности и вредности при проведении данной
технологической операции
|
Причины проявления данной опасности и вредности
|
Меры по безопасности проведения данной технологической
операции
|
|
Помол и перемешивание порошков
|
вибромельница
|
Спирт этиловый, порошки ZrO2, AlN, ZrN
|
Вдыхание пыли
|
Обеспечение СИЗ органов дыхания
|
|
|
|
Раздражение кожи рук и слизистых оболочек
|
|
Перчатки, защитные очки
|
|
Сушка порошков
|
Вакуумный сушильный шкаф
|
Порошки ZrO2-ZrN-AlN
|
Термический ожог
|
Не соблюдение требований ТБ
|
Перед изъятием порошков необходимо дождаться полного
охлаждения установки
|
|
Прессование образцов
|
Гидравлический пресс
|
Порошки ZrO2-ZrN-AlN
|
Вдыхание пыли
|
Высокая дисперсность прессуемых порошков; не соблюдение
требований ТБ
|
Обеспечение СИЗ органов дыхания
|
|
|
|
Раздражение кожи рук и слизистых оболочек
|
|
Перчатки, защитные очки
|
|
|
|
Повреждение верхних конечностей (попадание в установку)
|
|
Соблюдение требований ТБ
|
|
Обжиг образцов
|
Печь камерная
|
-
|
Термический ожог
|
Не соблюдение требований ТБ
|
При изъятии образцов необходимо пользоваться щипцами
|
|
Работа на компьютере
|
Компьютер
|
-
|
Нервно- психическая нагрузка
|
Длительное пребывание за компьютером
|
Соблюдение режима труда и отдыха
|
|
|
|
Заболевания глаз
|
|
Защитный экран
|
Меры первой помощи в случае травматизма (по таблице 2)
При отсутствии дыхания и пульса, расширенных зрачках и нарастающей
синюшности кожи делают искусственное дыхание и непрямой массаж сердца до
прибытия врача [47].
При работе с порошками, помещение лаборатории необходимо хорошо
проветривать, ввиду пылеобразования. Работать с порошками необходимо в
перчатках, предварительно смазав руки кремом.
Наиболее вероятным случаем травматизма является поражение электрическим
током. Первая помощь при поражении должна быть оказана незамедлительно.
Во-первых, следует прекратить воздействие на человека электрического тока:
выдернуть вилку из розетки, выключить рубильник. Далее следует вызвать скорую
помощь. Если тяжелых повреждений с потерей сознания нет, следует дать
успокаивающие средства.
При отсутствии дыхания и пульса, расширенных зрачках и нарастающей
синюшности кожи делают искусственное дыхание и непрямой массаж сердца до
прибытия врача [47].
При термических ожогах доврачебная помощь. Производят первичную обработку
обожженной поверхности: обмывают кожу мыльной водой с помощью марлевых
салфеток; можно обрабатывать кожу слабым раствором перманганата калия, спиртом.
Поврежденную поверхность закрывают сухой асептической повязкой. При сильных
ожогах (II-IV степень) обязательно обратиться к врачу [48].
Охрана окружающей среды
Для успешного проведения мероприятий по охране окружающей среды,
необходимо сочетание двух методов: безопасной технологии и тщательной очистки с
локализацией существующих вредных отходов.
Данные об отходах, образующихся во время работы, представлены в таблице
3.
Таблица 3- Характеристика производственных отходов
|
Отходы
|
Агрегатное состояние
|
Количество отходов,кг
|
Примечание (куда направляется отход)
|
|
Твердые отходы
|
ТВ.
|
0,5
|
В атмосферу
|
|
Вентиляционные выбросы
|
Г.
|
15
|
В атмосферу
|
|
Сточные воды
|
Ж.
|
5
|
В канализацию
|
Приложение В
Патентный поиск
Целью данного патентного поиска является композиционные керамические
материалы на основе оксида циркония и нитридов циркония и алюминия. Глубина
поиска - 30 лет.
Таблица А 1 - Параметры патентного поиска
|
Страна
|
Индекс МПК
|
Период, за который просмотрена патентная документация
|
Наименование источника патентной документации
|
|
Россия (СССР) США Германия (ФРГ, ГДР) Япония Великобритания
Франция Швеция Швейцария Канада EPV WO
|
C04B38/08 C04B28/26 С04В 33/00 B28B1/50 F27B9/00
|
1977 - 2007 гг.
|
РЖ ВИНИТИ «Химия»; Полные описания изобретений Интернет:
www.patent.ibm.com; www.uspto.gov; www.fips.ru
|
Таблица А 2 - Перечень обнаруженных патентных документов
|
№ заявки, страна
|
Индекс МПК
|
Даты приоритета и публикации
|
Название изобретения
|
|
95117334/02 Россия
|
C04B41/50 C23C18/12
|
1995.07.14-1997.07.10
|
Cпособ изготовления подложек с покрытием из нитридов
металлов
|
|
4788167США
|
C04B 3558
|
20.11. 86- 29.11.88
|
Ceramic composite
|
|
4016061 США
|
C23C 1500
|
16.01.74- 5.04.77
|
Resistive film composition
|
|
5679980 США
|
H01G 406; H01L 2912
|
19.12.96 - 21.10.97
|
Oxidizable layer.
|
Патентный поиск и анализ отобранных патентов показал, что материалы в
системе AlN-ZrO2-ZrN не разрабатывались. Отдельные компоненты или их
смесь широко используются в качестве функциональных покрытий на изделиях из
металлов, сплавов и композиционных материалов. В качестве примера можно
привести патенты № 95117334, № 4016061, № 5679980.
Наиболее близким по техническому решению является патент США № 4788167, в
котором описан процесс получения и состав многофазового поликристаллического
материала на основе AlN и Al2O3 с добавками одного из
нитридов - Ti, Zr, Hf. Основным назначением таких материалов является
изготовление абразивных инструментов.
Обнаружены сведения о большом количестве патентов, описывающих
керамические и композиционные материалы на основе ZrO2 с различными
добавками, в числе которых нитриды алюминия и циркония отсутствуют.
Таким образом, разработанный в дипломной работе керамический
композиционный материал на основе системы AlN-ZrO2-ZrN обладает
патентной чистотой и может стать предметом изобретения после подачи заявки в
Роспатент.
Приложение Г
Программа расчета симплекс-решеточного планированияc определением
адекватности модели и построением линийравных значений с записью результатов в
файл.Модель 3-й неполной степени (7 точек)Исходные данные в файле SIMP.DAT (см.
simp.hlp)Поиск точного значения Y максимального.Автор программы - Пантелеев И.
Б.t(119)3
open "i",#2,"simp.dat"i=1 to
4#2,tit$(i)i#2,n=7*(n-1)f>120 then tt=1.96 else tt=t(f)y(7,n):i=1 to 7j=1 to
n#2, y(i,j)ji
i=1 to 7(i)=0: mm(i)=0: nn(i)=1000000i
i=1 to 7(i)=0j=1 to n(i)=ys(i)+y(i,j)/nji
i=1 to 7j=1 to n=y(i,j)-ys(i)(i)=si2(i)+pp*pp/(n-1)j=s02+si2(i)/7ii=1 to
7j=1 to ny(i,j)>mm(i) then mm(i)=y(i,j)y(i,j)<nn(i) then nn(i)=y(i,j)ji
i=1 to 7(i)=ys(i)i
"Используем максимальные (1) или средние (0) значения"vvvv=0
then 5
i=1 to 7(i)=mm(i)i
CLS(1)=ys(1)(2)=ys(2)(3)=ys(3)(4)=4*ys(4)-2*ys(1)-2*ys(2)(5)=4*ys(5)-2*ys(1)-2*ys(3)(6)=4*ys(6)-2*ys(2)-2*ys(3)(7)=27*ys(7)-12*(ys(4)+ys(5)+ys(6))+3*(ys(1)+ys(2)+ys(3))
=0: mn=1000000i=1 to 7ys(i)>mx then mx=ys(i)ys(i)<mn then mn=ys(i)i
i=1 to 7(i)=e(i)i
" Результаты расчета параметров
полинома""------------------------------------------------""|
N | Yi cp. | Yi max | Yi min | Bi
|"------------------------------------------------"i=1 to 7"
"int(i);:print using"
#####.";ys(i);mm(i);nn(i);B(i)"------------------------------------------------"iПечать
в файл"Введите имя файла для
записи";sim$"o",#1,sim$#1," Результаты расчета параметров
полинома"#1,"------------------------------------------------"#1,"|
N | Yi cp. | Yi max | Yi min | Bi |#1,"------------------------------------------------"i=1
to 7#1, " "int(i);:print#1, using"
#####.";ys(i);mm(i);nn(i);B(i)#1,"------------------------------------------------"i#1,
"Рисуем треугольник? (1/0)"cccc<>1 then goto
8"Минимальное значение Y -:####.";mn"Максимальное значение Y
-:####.";mx"Введи начальное значение Y"b1"Введи конечное
значение Y"b2"Введи шаг расчета"st
9: cls=0=01,32: COLOR 15: PRINT
tit$(4)(480,330)-(80,330),15(80,330)-(280,30),15(280,30)-(480,330),15(481,331)-(79,331),15(79,331)-(280,31),15(280,31)-(481,331),15
Y=b1 TO b2 STEP st2,1=SS+2=0"Y=";Y240,23,1"X1= "X1=0
TO 100 STEP .53,4INT(X1)X2=0 TO 100-X1 STEP
.5=100-X1-X2=(B(1)*X1+B(2)*X2+B(3)*X3)/100=(B(4)*X1*X2+B(5)*X1*X3+B(6)*X2*X3)/10000=(B(7)*X1*X2*X3)/1000000=E1+E2+E3ABS(Y-Y2)>1
THEN 2(80+(1-X1/100-X2/200)*400,330-X2*3)DD=1 GOTO
2(81+(1-X1/100-X2/200)*400,330-X2*3)-(550,46+8*(SS-1)),8SS/2+3,70Y500,3=1
REMX2X1Y
5,1"END"zz
cls"Проверка адекватности модели:""Введите координаты
контрольной точки -""X1"X1: X1=X1/100"X2"X2:
X2=X2/100"Введите значение Y эксперим."YT=1-X1-X2=3*(X1*X1+X2*X2+X3*X3)=.5*X1*(6*X1*X1-2*X1+1-b)=.5*X2*(6*X2*X2-2*X2+1-b)=.5*X3*(6*X3*X3-2*X3+1-b)=4*X1*X2*(3*X1+3*X2-2)=4*X1*X3*(3*X1+3*X3-2)=4*X2*X3*(3*X2+3*X3-2)=27*X1*X2*X3=a1*a1+a2*a2+a3*a3+a4*a4+a5*a5+a6*a6+a7*a7=B(1)*X1+B(2)*X2+B(3)*X3=B(4)*X1*X2+B(5)*X1*X3+B(6)*X2*X3=B(7)*X1*X2*X3=E1+E2+E3=abs(YT-YR)=DY*sqr(n)/sqr(s02*sqr(1+k))using
"Расчетное значение Y ####.";YRusing "Коэффициент Стьюдента
расчетный ##.##";trusing "Коэффициент Стьюдента табличный
##.##";tt:printtr<tt then 6"Модель неадекватна."7
print "Модель адекватна."
print"Проверяем другую точку (1/0)"gggg<>1 then goto 9:
goto 8
print "Поиск максимального значения Y"X1=0 TO 1 STEP .005X2=0
TO 1 STEP .005X1+X2>1 THEN
11=1-X1-X2=B(1)*X1+B(2)*X2+B(3)*X3=B(4)*X1*X2+B(5)*X1*X3+B(6)*X2*X3=B(7)*X1*X2*X3=E1+E2+E3Y2>A
THEN 22 ELSE 11
A=Y2:C1=X1:C2=X2:C3=X3
REMX2X1USING"Содержание компонента 1
###.#";C1*100USING"Содержание компонента 2
###.#";C2*100USING"Содержание компонента 3
###.#";C3*100USING"Y максимальное ####.";A#1,
USING"Содержание компонента 1 ###.#";C1*100#1, USING"Содержание
компонента 2 ###.#";C2*100#1, USING"Содержание компонента 3
###.#";C3*100#1, USING"Y максимальное ####.";A
4
t(7)=2.36:t(14)=2.14:t(21)=2.08:t(28)=2.05:t(35)=1.69(42)=2.02:t(49)=2.01:t(56)=2:t(63)=2:t(70)=2:t(77)=1.99(84)=1.99:t(91)=1.99:t(98)=1.99:t(105)=1.98:t(112)=1.98(119)=1.981
stop
Пример расчета
(7 point)
Чумакова Н.Н. ZrO2-ZrN-AlN
прочность при изгибе
_C
.6 768.2 594.0 744.1 721.9
.2 636.9 432.7 521.1 607.9
.8 309.9 354.2 349.7 495.3
.3 336.1 340.3 333.3 396.7
.1 362.8 309.2 323.2 271.2
.3 437.5 289.8 444.3 459.7
.2 335.1 503.3 417.2 417.2