Индандион трехкомпонентый синтез
ВВЕДЕНИЕ.
Важное место в органической
химии, как в теоретической, так и в прикладном аспектах занимают индандион и
его производные. Среди производных индандиона найденное большое количество
биологически-активных препаратов. На их основе разработано большое количество
средств, используемых для борьбы с грызунами. Перспективным препаратом признан фентолацин ( 2-
(фенил-толилацетил) -индандион-1,3). Он обладает сильным разовым действием на
грызунов. Изоиндан ( 2 -
[фенил-(4-изопропилфенин)-ацетил]-индан-1,3-дион) оказывает противосвертывающее
действие на кровь, изменяет проницаемость стенок кровеносных сосудов, в
результате чего развивается кровоточивость, приводящая к гибели животных.
Кроме того производные индандиона
нашли широкое применение в фотонике и в аналитической химии (нингидрин
используется как качественный и количественный реактив при определении
первичных аминов и аминокислот).
Индандион и его производные хорошо
изучены во многих реакциях с электрофильными реагентами и реакциях
гетероциклизации.
Целью нашей работы является
трехкомпонентный синтез на основе индандиона, фурфурола и 5-амин-1Н-тетразола.
1.ИНДАНДИОН (Литературный обзор)
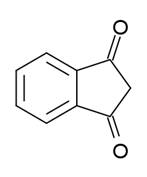 Индандион — органическое вещество. Существует
в форме дикетона. Значительный вклад в развитие химии индандиона и его
производных внёс профессор РТУ Г. Я. Ванаг — основатель рижской школы
химиков-органиков.
Индандион — органическое вещество. Существует
в форме дикетона. Значительный вклад в развитие химии индандиона и его
производных внёс профессор РТУ Г. Я. Ванаг — основатель рижской школы
химиков-органиков.
Получение.
Индандион получают кислым гидролизом
и одновременным декарбоксилированием натриевой соли
2-алкоксикарбонилиндан-1,3-диона (обычно этокси-) при повышенной температуре.

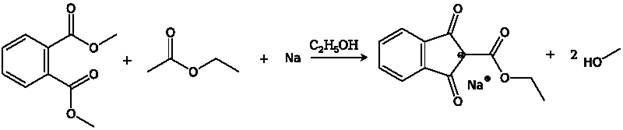
Саму же соль получают сложноэфирной
конденсацией алкилацетата и диалкилфталата.
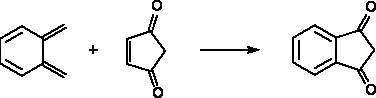
Реакция Дильса — Альдера из
орто-ксилилена и циклопент-4-ен-1,3-диона /1/.
При окислении индана пероксидом
водорода или трет-бутилгидропероксидом, в качестве основного продукта получают
индан-1-он, индандион получается лишь как примесь /2/.

1.2.Физические
и химические свойства.
Индандион существует в двух формах:
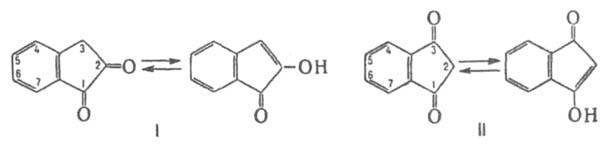
1,2-Индандион (I) - желтые кристаллы с Т. пл. 95 °С;
хорошо растворим в кипящей воде.
1,3- Индандион (II) - бесцветные или желтоватые кристаллы
с Т. пл. 129-130 °С /3/.
Енольная форма характеризуется
сопряжением и отрицательным частичным зарядом на 2-м атоме углерода и том атоме
кислорода, который не связан с водородом (то есть, любой из двух). Анион же
индандиона — это сопряжённая 6π-электронная система, отрицательный заряд
делокализирован. Согласно приблизительным расчётам по методу МО Хюккеля
наибольшая электронная плотность после обоих атомов кислорода находится опять-таки
на 2-м атоме углерода. Это обуславливает многие его химические свойства.
Общие свойства для дикетонов.
Енолизация — в воде pKе = 5,6, это соответствует двум процентам енола. В разных
растворителях Kе разная ввиду различных эффектов
сольватирования для OH- и CH-кислот. Дикетоны с пятичленным циклом менее
енолизированны, чем подобные соединения с шестичленным циклом — вероятно, ввиду
невозможности образования стабилизующей водородной связи в еноле.

Получается продуты C-, и
O-присоединения, но в основном реакция идёт, по-видимому, по 2-му атому
углерода. Это, однако, зависит также от растворителя и концентрации веществ.
Реакция происходит с енольной формой или анионом. Например, при бромировании
можно получить 2-броминдан-1,3-дион или 2,2-диброминдан-1,3-дион /4/.

Реакция нитрования проходит легко с
образованием 2-нитроиндандиона — сильной кислоты. C-электрофилы обычно
реагируют с анионом дикетона. Продукты реакции с альдегидами — обычно
бис-продукты.
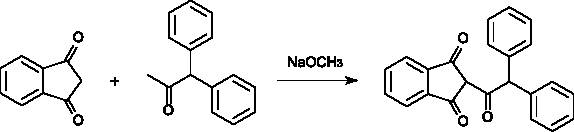
В качестве примера ацилирования можно
привести реакцию с 1,1-дифенилацетоном, которой можно получить родентицид
2-дифенилацетилиндан-1,3-дион (дифацинон или дифенадион) /5/.
В качестве других электрофильных
реакций присоединения можно упомянуть галогенирование, сульфирование,
азосочетание, нитрозирование.
Восстановление амальгамой цинка по
Клемменсену приводит к индану /6/.

Восстанавливет боргидридом натрия (в
присутствии палладиевого катализатора), получают 3-гидрокси-1-инданон; при
дальнейшем восстановлении —индан-1,3-диол /7/.

Гомолитические реакции —индандиона с
свободными радикалами, а также при окислении анионов образуются
стабилизированные делокализацией радикалы, тут же вступающие в дальнейшие
реакции, как, например, с алкадиенами, алкинами и друг с другом (димеризация).
Стабильны радикалы 2-арилзамещённых индандионов.
Частным случаем является окисление
индандиона в нингидрин с помощью NBS и диметилсульфоксида. Те же реагенты
помогают получить нингидрин из 1-инданона и 2-инданона /8/.

Специфические реакции.
Самоконденсация происходит весьма
легко с образованием биндона — специфического реагента на первичные амины.

1.3. Применение
Производные индандиона — биндон,
2-нитроиндандион, нингидрин — используют в аналитической химии. Есть
производные, которые, возможно, будут использоваться в фотонике (ведутся
исследования). Некоторые производные являются препаратами, понижающими
свёртываемость крови (антикоагулянты). В медицине, в частности, применяют
арилпроизводные (фенилин — 2-фенилиндан-1,3-дион и омефин — 2-гидроксиметил-2-фенилиндан-1,3-дион).
В качестве родентицида (крысиного яда) применяют ратиндан
(2-дифенилацетилиндан-1,3-дион); нужно, однако, помнить, что этот способ травли
крыс весьма жесток — крыса, ввиду своего образа жизни часто получающая
небольшие царапины, истекает кровью и погибает от её потери.
2.
Обсуждение
результатов.
Трехкомпонентный синтез 10-(3-фурил)-4,10-дигидро -9H-индено[1,2-d]тетразоло[1,5-a]пиримидин-9-она
С целью синтеза
10-(3-фурил)-4,10-дигидро -9H-индено[1,2-d]тетразоло[1,5-a]пиримидин-9-она мы использовали
методику мультикомпонентной реакции на примере взаимодействия индандиона с
фурфуролом и 5-амин-1Н-тетразом. Реакция проводилась с использованием - пиридина,
при нагревании. В результате получили чёрные кристаллы 10-(3-фурил)-4,10-дигидро
-9H-индено[1,2-d]тетразоло[1,5-a]пиримидин-9-она
с температурой плавления 129-130 ̊ С.


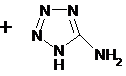
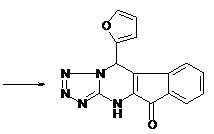
54%
ИК–спектры содержат
полосы колебаний в области 1750-1740 см-1 , обусловленные
характеристическими колебаниями с участием группы С=О.
ИК спектр содержит полосы
поглощения, соответствующие валентным колебаниям группы СН2алиф (2950- 2867 см-1); фуранового кольца (1036 – 1016
см-1). Вторичная аминогруппа гетероцикла проявляется одной узкой
полосой при (3344 – 3296 см-1).
3. Экспериментальная
часть
3.1 Физико-химические методы анализа
веществ
ИК-спектры записаны на
инфракрасном Фурье-спектрометре ФСМ-1201 на таблетках KBr (в областях 4000-1800
см-1 и 1500-1300 см-1) .
3.2. 10-(3-Фурил)-4,10-дигидро -9H-индено[1,2-d]тетразоло[1,5-a]пиримидин-9-он.


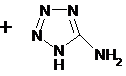

0.14 г (0.0009 моль) Индандиона
помещают в круглодонную колбу с обратным холодильником, добавляют 0.1 мл (0.1
г; 0.001 моль) фурфурола и 0.1 г (0.001 моль) 5-амин-1Н-тетразола, пиридин.
Реакционную смесь нагревают 3 часа до выпадения осадка.
Выпавшие черные кристаллы
отфильтровывают на воронке Бюхнера, сушат на воздухе.
Выход 0.1 г (54%)
ИК-спектр ν, см-1: 1750-1740,
1565-1500, 3165-3125 (С=О); 2950- 2867 (СНалиф.); 1036 – 1016 (Fu); 3344 – 3296 (Ar).
Выводы
1.
В литературном
обзоре обобщены сведения по синтезу, реакциям, свойствам индандиона за период
1970-2009 года.
2.
Синтезирован методом
циклоконденсации 10-(3-фурил)-4,10-дигидро -9H-индено[1,2-d]тетразоло[1,5-a]пиримидин-9-она с выходом 54%.
3. Состав и строение 10-(3-фурил)-4,10-дигидро
-9H-индено[1,2-d]тетразоло[1,5-a]пиримидин-9-она
установлено с помощью ИК-спектроскопии.
Инструкция по охране
труда и технике безопасности
Правила работы с
электрическими приборами.
Работа с электрическими
приборами требует точного соблюдения правил техники безопасности. Это связано с
тем, что при определенных условиях (высокая влажность, плохая изоляция),
поражение может вызвать напряжение 12 В. Кроме того, в условиях химической
лаборатории опасное воздействие на человека любого ощутимого тока вызывает
непроизвольное отдергивание рук, что может явиться причиной поломки стеклянной
аппаратуры или пролива огнеопасной жидкости.
В целях безопасности
работы категорически запрещается:
1.
Проверять на ощупь наличие напряжения или нагрева токоведущих частей прибора.
2. Применять
для соединения электрических приборов провода с повреж-денной изоляцией.
3.
Снимать кожух прибора, включенного в сеть.
Работа с
огнеопасными и легковоспламеняющимися жидкостями
Легковоспламеняющиеся
жидкости (ЛВЖ) – это такие жидкости, пары которых имеют температуру вспышки 61оС
в закрытом сосуде или 65оС в открытом сосуде (диэтиловый эфир,
ацетон, этанол).
Работающий с ЛВЖ обязан
соблюдать следующие правила:
1.
ЛВЖ и горючие жидкости должны храниться в лабораториях в толстостенных склянках
с пробками. Общий запас огнеопасных жидкостей, одновременно хранящихся в каждом
рабочем помещении не должен превышать 1л на сотрудника.
2. Запрещается
отгонять ЛВЖ на горелке или плитке с открытым элементом.
3.
Запрещается хранить ЛВЖ в вытяжных шкафах, в которых используются горелки и
другие нагревательные приборы, а также окислители.
4. Перегонять и
нагревать низкокипящие вещества следует в круглодонных колбах, изготовленных из
тугоплавкого стекла на банях, заполненных водой, глицерином или силиконовым
маслом.
5. По окончании работы
запрещается выливать горючие жидкости в канализацию. Их следует собирать в
специальную герметически закрывающуюся тару.
Работа с кислотами и щелочами
Крепкие кислоты, щелочи
и крепкие их растворы при попадании на тело могут вызвать сильные ожоги.
Поэтому при работе с ними следует соблюдать следующие меры предосторожности:
1.
Работать в очках
и резиновых перчатках.
2.
Обеспечить
удобное хранение кислот и щелочей.
3.
Приливать кислоту
в воду, а не наоборот.
4.
При переливании
из склянки в склянку пользоваться воронкой.
При ожогах кислотой
обожженное место промыть большими порциями воды и обработать 2% раствором
бикарбоната натрия.
При ожогах кислотой
обработать пораженное место раствором борной кислоты. При попадании кислоты
(или щелочи) в глаза промыть водой и обратиться к врачу.
Первая
помощь при острых отравлениях химическими веществами
Концентрированные
кислоты
Симптомы отравления: при
вдыхании паров – насморк, чихание, кашель, жжение в горле; при попадании брызг
в глаза – резкая боль, слезотечение; при попадании на кожу – ожоги.
Первая помощь: обильное
промывание водой, затем 2% раствором соды, затем опять водой, закапывание в
глаза новокаина, альбуцида.
Список используемых источников
1. D. B. Hansen and M. M.
Joullie: "The development of novel ninhydrin analogues" in Chemical
Society Reviews 2005, N 34, S 408–417.
2. J. Muzart:
"Homogeneous CrVI-Catalyzed Benzylic, Allylic and Propargylic Oxidations
by tert-Butyl Hydroperoxide" in Mini-Reviews in Organic Chemistry 2009, N 6,
S 9-20.
3. M. A. Matos, M. S.
Miranda, M. J. Monte, L. M. Santos, V. M. Morais, J. S. Chickos, P. Umnahanant,
J. F. Liebman: "Calorimetric and computational study of indanones" in
Journal of Physical Chemistry 2007, N 111, S 187-189.
4. D. Nematollahi, N.
Akaberi: "Electrochemical Study of Bromide in the Presence of
1,3-Indandione. Application to the Electrochemical Synthesis of Bromo
Derivatives of 1,3-Indandione" in Molecules, 2001, N 6, S. 639-646.
5. Thomas A. Unger:
"Pesticide Synthesis Handbook", Verlag William Andrew, 1996. S. 900.
6. S. A. Galton, M. Kalafer,
F. M. Beringer: "Rearrangements in the Clemmensen reduction of 1-indanones
and, 1,3-indandiones" in J. Org. Chem., 1970, N 35, S 1–6.
7. J. F. Neumer:
"2,3-Disubstituted 1-Indanones", in J. Org. Chem., 1976, N 41, S 3-5.
8. J. L. Hallman:
"Synthesis of Naphtho(f)ninhydrin and Synthesis of Polymer-supported Crown
Ethers". Dissertation, 1991