Синтез, очистка и исследование 2-нафтилацетата
КУРСОВАЯ
РАБОТА
Дисциплина:
ОРГАНИЧЕСКАЯ ХИМИЯ
Тема:
СИНТЕЗ, ОЧИСТКА И АНАЛИЗ 2-НАФТИЛАЦЕТАТА
СОДЕРЖАНИЕ
Реферат
Условные обозначения, названия и
единицы измерения физических величин
Введение
Свойства 2-нафтилацетата и
исходных веществ
.1 Физические свойства
2-нафтилацетата
.2 Электронное строение
1.3 Способы получения
.4 Свойства исходных веществ
2 Расчет количеств исходных
веществ
.2 Расчет количеств исходных
веществ по методике
2.3 Расчет количеств исходных
веществ по уравнению
3 Главные этапы синтеза
.1 Приготовление исходных и
вспомогательных реактивов и собирание приборов
.1.1 Приготовление исходных и
вспомогательных реактивов
.1.2Сборка приборов
.2 Отделение вещества от
сопутствующих продуктов
3.3 Идентификация
4 Ход синтеза
5 Характеристика
синтезированного вещества
5.1 Физико-химические константы и
растворимость
.2 Идентификация
.3 Выход продукта
Выводы и рекомендации
Список использованных источников
Приложения
УСЛОВНЫЕ ОБОЗНАЧЕНИЯ, НАЗВАНИЯ И ЕДИНИЦЫ
ИЗМЕРЕНИЯ ФИЗИЧЕСКИХ ВЕЛИЧИН
Абсолютная погрешностьδ,
%
Относительная погрешность∆
Выход вещества от теоретическогоηт,
%
Выход вещества от указанного в методикеηм,%
Индукционный эффектI
Мезомерный эффектM
Количество вещества ν,
моль
Избыток количества веществаνизб,моль
Теоретическое количество вещества по уравнениюνт,
моль
Избыток количества вещества в % ν(%),
%
Масса веществаm,
г
Масса раствораmр-ра,
г
Теоретическая масса веществаmт,
г
Масса вещества по методикеmм,
г
Масса полученного веществаmр,
г
Молярная масса вещества М, г/моль
Массовая доляω, %
Объем раствораV
или Vр-ра,мл
Показатель преломленияn20D
Плотность веществаρ, г/см3
Плотность раствораρр-ра, г/мл
Температура кипенияt,
⁰С
Температура плавленияt,
⁰C
Теоретическое значение температуры плавленияt1,
⁰C
Экспериментальное значение температуры плавленияt2,
⁰C
ВВЕДЕНИЕ
нафтилацетат
реактив синтезированный
Целью курсовой работы является синтез
2-нафтилацетата по выбранной методике. Рассчитать исходные количества вещества
по методике и по уравнению реакции, выход продукта. Анализ экспериментальных
данных: выход продукта реакции, физико-химические константы (определение
температуры плавления, проверка растворимости), идентификация. Рассмотреть
различные способы получения, строение, химические свойства данного вещества.
Для полученного 2-нафтилацета необходимо
провести очистку от сопутствующих веществ и проделать качественные реакции,
исследовать растворимость в различных растворителях, определить температуру
плавления. Проанализировать экспериментальные данные и сделать выводы по выходу
продукта, степени чистоты полученного вещества. Сделать вывод о
целесообразности использования данной методики для синтеза 2-нафтилацетата.
-Нафтилацетат - органическое соединение,
относится к классу сложных эфиров и имеет формулу:
Структурная формула: Молекулярная формула:
С12Н10О2

Название по систематической
номенклатуре:уксуснонафталиновый эфир.
По рациональной: 2-нафтилацетат.
1 СВОЙСТВА 2-НАФТИЛАЦЕТАТА И
ИСХОДНЫХ ВЕЩЕСТВ
.1 Физические свойства 2-нафтилацетата
-Нафтилацетат - бесцветное
кристаллическое вещество, кристаллизуется из этанола в виде игл, растворим в
этаноле, эфире, хлороформе, нерастворим в воде. Молекулярная масса 186,21
г/моль, температура плавления 68,5⁰С.[3] Сведений о токсичности
2-нафтилацетата не имеется, но данное вещество может быть получено из
нафталина, воздействие которогочрезвычайно опасно для здоровья человека, а
иногда даже смертельно[5].
.2 Электронное строение
Молекула 2-нафтилацетата состоит из двух
конденсированных бензольных колец (нафталина) и кислотного остатка уксусной
кислоты - иона. Рассмотрим сначала строение нафталина. Молекула нафталина
состоит из двух конденсированных колец в о-положенияхбензольных колец. В
нафталине все десять атомов С находятся sp2
- гибридизации. Не гибридизованные р-орбитали образуют сопряженную систему,
состоящую из десяти π-электронов.
Согласно современным представлениям молекула нафталина имеет плоское строение с
менее равномерным, чем в бензоле, распределением π-электронной
плотности, что проявляется в различной длине связей С - С:


Ацетат-ион  , входящий в
состав 2-нафтилацетата, находится в положении 2 (β), он относится
к ориентантам второго рода, и за счет отрицательных мезомерного (- М)и
индукционного эффекта (- I) снижает электронную плотность в
положениях 1, 3, 6, 8, так как α-положение второго кольца обладает
большей активностью по сравнению с β-положениями, то замещение
происходит в положениях 5 и 8.
, входящий в
состав 2-нафтилацетата, находится в положении 2 (β), он относится
к ориентантам второго рода, и за счет отрицательных мезомерного (- М)и
индукционного эффекта (- I) снижает электронную плотность в
положениях 1, 3, 6, 8, так как α-положение второго кольца обладает
большей активностью по сравнению с β-положениями, то замещение
происходит в положениях 5 и 8.

Характерные реакции:
реакции электрофильного замещение SE,
реакции нуклеофильного замещения по
связи  ,
,
реакции окисления.
· Реакции нуклеофильного замещения
Для 2-нафтилацетата характерны реакции гидролиза
(а), переэтерификации (б), образования амидов (в). Реакция катализируется
кислотами и основаниями, протекает при обычной температуре.
(а)

2-нафтилацетат нафталиновая кислота
В результате реакции гидролиза образуется
нафталиновая кислота и этиловый спирт [1].
(б)

2-нафтилацетат этанол2-нафтилпропанат метанол
При взаимодействии со спиртами возможна замена
радикала у гидроксильного кислорода, таким образом может образоваться другой
эфир, в данном случае образовался 2-нафтилпропанат.
· Реакции электрофильного замещения
(в)

2-нафтилацетатаммиак
2-нафтилацетатамидметанол
.3 Способы получения
-Нафтилацетат можно получить из органических
веществ различных классов несколькими способами: реакцией этерификации,
ацилирования спиртовгалогенарилами, ангидридами карбоновых кислот и реакцией
ацилирования в щелочной среде из солей карбоновых кислот.
· Реакция этерификации

нафталиновая кислота этиловый спирт
2-нафтилацетат [1]
Реакция проходит в присутствии минеральных
кислот.
· Реакция
ацилированиягалогенангидрида. Эта реакция идет в присутствии катализатора BF3.

хлор-2-нафтилат2-нафтилацетат[2]
· Реакция ацилирования в щелочной
среде:

2-нафтилацетатацетат натрия [3]
Побочные реакции:
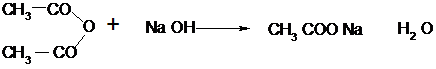

-нафтолгидроксид натриянафтолят
натрия
Реакция этерификации обратима, чтобы
увеличить выход вещества необходимо постоянное выведение эфира или воды из
сферы реакции. Ацилированиегалогенангидридами идет в присутствии дорогостоящего
катализатора фторида бора.
Для получения 2-нафтилацетата в
данном синтезе выбрана реакция ацилирования в щелочной среде[3], так как эта
реакция не требует жестких условий проведения, протекает быстро и выход
продукта реакции достаточно велик.
.4 Свойства исходных веществ
-Нафтол представляет собой
полупрозрачные белые пластинки с фенольным запахом.
Уксусный ангидрид - бесцветная с
резким запахом жидкость.
Гидроксид натрия - твердое
кристаллическое вещество белого цвета.
Остальные свойства исходных веществ
и их физические константы представлены в таблице 1.
Таблица 1 - Свойства 2-нафтилацетата и исходных
веществ
|
Название
вещества, формула
|
М,
г/моль
|
tкип. ºC
|
tпл. ºC
|
nD20
|
ω,%
|
ρ,
г/см3
|
Растворимость
|
Примечание
|
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
|
2-нафтилацетат
C12H10O2
|
186,21
|
--
|
68,5
|
--
|
--
|
--
|
Растворим
в этаноле, эфире, хлороформе,нерастворим в воде. [4]
|
|
Уксусный
ангидрид С4Н6О3
|
102,09
|
139,5
|
-73,1
|
1.3904
|
--
|
1,082
|
В
бензоле, эфире и др. органичсеких растворителях. С водой образует уксусную
кислоту.[5]
|
Раздражает
глаза и дыхательные пути, вызывает ожоги кожи
|
|
Гидроксид
натрия NaOH
|
39,997
|
1403
|
323
|
-
|
10
|
2,02
|
в
воде-52,2 (20 °С), метаноле-23,6 (28 oС), этаноле-14,7 (28 °С) [6]
|
Щелочь
при попадании на кожу и слизистые оболочки вызывает сильные ожоги
|
|
2-нафтол
С10Н7ОН
|
144
|
285
- 286
|
121,6
|
--
|
--
|
--
|
В
этаноле, диэтиловом эфире, хлороформе, бензоле, плохо растворим в воде.[4]
|
Горюче,НЕ
ДОПУСКАТЬ открытого огня.порошком, разбрызгиванием воды, пеной, двуокисью
углерода, взрывоопасно, при вдыхании появляются Мелкодисперсные частицы в
воздухе образуют взрывоопасныe смеси. Не допускать накопления пыли; закрытая
система, защищенное от взрыва при накоплении пыли электрооборудование и
освещение. НЕ ДОПУСКАТЬ РАССЕИВАНИЯ ПЫЛИ! Вдыхание Кашель.боли в горле, под
воздействием 2-нафтола на коже появляется покраснение. Защита органов
дыхПокраснение. Боль. Защитные перчатки. Защитная одежда. Ополоснуть и затем
промыть кожу водой с мылом. Боль в глазах.При проглатывании вызывает рвоту,
боли в желудке, судороги.Боль в животе. Судороги. Понос. Рвота. Не принимать
пищу, не пить и не курить во время работы. Прополоскать рот. Дать выпить
большое количество воды.
|
РАСЧЕТ КОЛИЧЕСТВ ИСХОДНЫХ ВЕЩЕСТВ
Все данные, необходимые для дальнейших расчетов
берутся из таблицы 2.
.1 Расчет количеств исходных веществ по методике
Исходные вещества для получения 2-нафтилацетата
берутся в следующих количествах:
2-нафтол, 10 г
Уксусный ангидрид, 10,5 мл,
ρ=1,082 г/мл
Гидроксид натрия, 50 мл, ω=10%,
ρ=1,11 г/см3
· Рассчитываем массу уксусного
ангидрида по формуле:
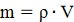
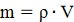 ,(1)
,(1)
где m-масса
вещества,г
ρ - плотность вещества,г/см3
V - объем
вещества, мл
m=1,082∙10,5=11,36
г
Количество вещества ν, мольвычисляют
по формуле:

 , (2)
, (2)
где ν - количество
вещества, моль
ν(С4Н6О3)=11,36/102,09=0,11
моль
· Рассчитываем массу гидроксида
натрия, содержащегося в 50 мл раствора , ω=10%, ρ=1,11
г/см3
Находим массу раствора гидроксида натрия по
формуле:

 , (3)
, (3)
где mр-ра - масса
раствора, г
ρр-ра- плотность раствора,г/мл
Vр-ра - объем
раствора, мл
mр-ра=1.11∙50=55.50г
Массу самого вещества находим из
формулы:

 , (4)
, (4)
где ω - массовая
доля, %
mв-ва - масса
растворенного вещества, г
m(NaOH)=55,5∙0,1=5,55
г
Рассчитываем количество вещества
гидроксида натрия из формулы (2):
ν(NaOH)=5,55/40=0,14
моль
· Рассчитываем количество вещества
2-нафтола
По формуле (2):
ν(С10Н7ОН)=10/144=0,07
моль
2.2 Расчет количеств исходных веществ по
уравнению
Из уравнения реакций [3] видно,что ν(С10Н7ОН):ν(С4Н6О3):ν(NaOH)=1:1:1,
следовательно, 2-нафтолвзят в недостатке. Считаем по недостатку.

ν(С10Н7ОН)=ν(С4Н6О3)=ν(NaOH)=0,07
моль
· Рассчитываем избыток гидроксида
натрия в молях и в % соответственно по формулам:

 , (5)
, (5)
где νизб -
избыток количества вещества, моль
νт - теоретическое количество
вещества по уравнению.


 , (6)
, (6)
νизб(С4Н6О3)=0,11 - 0,07=0,04
моль

νизб(NaOH)=0,14-0,07=0,07
моль

· Рассчитываем массы исходных веществ
по уравнению
Из формулы (2) находим массу в 100% вещества:
m(С10Н7ОН)=0,07∙144=10,08
г
m(С4Н6О3)=0.07∙102.09=7,15
г
m(NaOH)=0,07∙40=2,8
г
Из формул (2) и (4) рассчитываем массы и объемы
веществ данной концентрации:
m(С4Н6О3)=7.15 г
V(С4Н6О3)=7,15∙1,082=7,74
мл
mр-ра(NaOH)=2.8/0.1=28
г
Vр-ра=28/1,11=25,23
мл
Все расчеты сведены в таблице 2.
Таблица 2 - Количества исходных веществ
|
Название
вещества, формула
|
Требуемые
количества
|
избыток
|
|
По
уравнению
|
По
методике
|
νизб, моль
|
В
%
|
|
νт
|
в
г и мл
|
νм
|
В
г и мл
|
|
|
|
|
100%
вещества
|
Данной
концентрации
|
|
100%
вещества
|
Данной
концентрации
|
|
|
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
|
2-нафтол
С10Н7ОН
|
0,07
|
10,08
г
|
10,08
г
|
0,07
|
10,08г
|
10,08г
|
--
|
--
|
|
Уксусный
ангидрид С4Н6О3
|
0,07
|
7,15
г
|
7,15
г 7,74 мл
|
0,11
|
11,36
г 10,50 мл
|
11,36г
10,50 мл
|
0,04
|
36,36
|
|
Гидроксид
натрия NaOH, ω=10%
|
0,07
|
2,8
г
|
28
г 25,23 мл
|
0,14
|
5,55
г
|
55,5
г 50 мл
|
0,07
|
50,00
|
Реакция ацилированияβ-нафтола
уксусным ангидридом протекает в разбавленном растворе щелочи, уксусный ангидирд
берется в избытке, для того, чтобы сместить равновесие реакции в сторону
образования эфира, тем самым увеличивая выход продукта. Гидроксида натрия и
уксусного ангидрида по уравнению реакции требуется 0,07 моль, а по методике 0,118
и 0,04 моль соответственно.
3 ГЛАВНЫЕ ЭТАПЫ СИНТЕЗА
.1 Приготовление исходных и вспомогательных
реактивов и собирание приборов
· Прежде чем использовать 2-нафтол в
синтезе, его перекристаллизовывают из воды, разбавленного этилового спирта или
четыреххлористого углерода. В качестве растворителя удобно использовать воду, в
этом случае перекристаллизацию проводят так: круглодонную колбу с навеской
2-нафтола помещают на песчаную баню, добавляют небольшое количество воды (в
несколько меньшем количестве, чем требуется для полного растворения) и
нагревают колбу. После полного растворения 2-нафтола горячий раствор выливают в
плоскодонную колбу или химический стакан через воронку со смоченным бумажным фильтром
приспособление для перекристаллизация приведено на рисункеА1 в приложении А. В
процессе охлаждения отфильтрованного раствора образуются кристаллы 2-нафтола,
которые потом отделяют от воды вакуум-насосом на воронке Бюхнера (рисунок А2
приложения А).
· В круглодонную колбу на 500 мл
наливают 50 мл 10% раствор гидроксида натрия, помещают туда 10 г 2-нафтола,
взвешенного на технических весах. Аккуратно перемешивая содержимое колбы,
растворяют большую часть 2-нафтола.
· Добавляют 10,5 мл уксусного ангидрида
и колотый лед. Снова встряхивают колбу для большего растворения 2-нафтола.
· Приготовление раствора гидроксида
натрия, ω=10%,
50 мл.
Взвешиваем рассчитанную массу гидроксида натрия
(стр. 12).
Рассчитываем объем воды, требующийся для 50 мл
раствора:
m(H2O)=mр-ра
- m(NaOH)=55.5
- 5.55=50 г
ρ(H2O)=1
г/мл
V(H2O)=50∙1.00=50
мл
Навеску, взвешенную на технических электронных
весах, помещают в химический стакан, добавляют 50 мл воды и перемешивают
стеклянной палочкой до полного растворения.
.1.2 Сборка приборов
Круглодонную колбу со смесью соединяем с
обратным воздушным холодильником. Перемешивают смесь в течении 15 - 20 минут,
круговыми движениями колбы, придерживая холодильник (рисунок 1).

Рисунок 1 - Прибор для синтеза 2-нафтилацетата.
1 - обратный холодильник, 2 - круглодонная колба.
.2 Отделение вещества от сопутствующих продуктов
· Полученные кристаллы 2-нафтилацетата
отфильтровывают на воронке Бюхнера.
· Кристаллы 2-нафтилацетата промывают
на воронке водой, сушат на воздухе.
· Очищают высушенный продукт
перекристаллизацией из разбавленного этилового спирта или из бензина с
температурой кипения 60 - 80°С, так как 2-нафтилацетат растворим в этих
веществах. Процесс перекристаллизации можно проводить в химическом стакане. Для
этого в разбавленный этиловый спирт помещают 2-нафтилацетат и перемешивают
стекляннойпалочой до растворения вещества. Очищаемое вещество переходит в
раствор, а нерастворимые примеси будут оседать на дне стакана. Отделяют верхний
слой, аккуратно сливая его в химический стакан.
· Полученный очищенный 2-нафтилацетат
отсасывают на воронке Бюхнера и сушат.
· При необходимости повторяют очистку.
· Выход 2-нафтилацетата по методике
составляет 13 г.
.3 Идентификация
Для идентификации полученного вещества проводят
качественную реакцию, проверяют растворимость в растворителях, определяют
температуру плавления.
ХОД СИНТЕЗА
В качестве исходного вещества по методике
используют перекристаллизованный 2-нафтол, но для синтеза брали обычный
реактив, то есть перекристаллизацию не проводили. Сначала смешивали 2-нафтол и
10%-ный раствор гидроксид натрия. Смесь этих веществ в колбе приобрела бежевый
оттенок , произошло частичное растворение пластинок 2-нафтола. Затем добавили
колотый лед. В последнюю очередь добавляли уксусный ангидрид. Колбу соединили с
воздушным обратным холодильником. Перемешиваем смесь, встряхивая колбу. В
процессе реакциинаблюдается выпадение белых кристаллических пластинок
2-нафтилацетата. Через 15 минут содержимое колбы отфильтровали на воронке Бюхнера
(рисунок 2) и промыли водой. Полученное вещество высушили на воздухе.
Высушенный 2-нафтилацетат представлял собой темно-бежевое кристаллическое
вещество, имеющее слабый фенольный запах.
Произвели очистку вещества из разбавленного
этанола, при этом изменился цвет вещества - от темно-бежевого до
светло-бежевого. Продолжительность синтеза составила около 1,5 часа, не
учитывая время высушивания вещества.
Выход 2-нафтилацетата составил 6.3 г .
5 ХАРАКТЕРИСТИКА СИНТЕЗИРОВАННОГО ВЕЩЕСТВА
Синтезированный 2-нафтилацетат представляет
собой кристаллическое вещество светло-бежевого цвета, имеющие вкрапления
бесцветных кристаллов, со слабым фенольным запахом. Для характеристики данного
вещества следует установить его температуру плавления, провести идентификацию и
проверить растворимость в различных растворителях.
5.1 Физико-химические константы и растворимость
Для определения температуры плавления
использовался прибор, изображенный на рисунке 3А приложения А. В стеклянный
капилляр плотно набиваем 2 - 3 мм полученного 2-нафтилацетата, капилляр
присоединяем резиновым кольцом к термометру и помещаем в прибор для определения
температуры плавления. В процессе нагревания столбик уплотняется, появляются
пузырьки воздуха, в момент появления которых отмечаем температуру на
термометре. Была установлена температура плавления равная 68,5 °С.
Теоретическое значение составляет 71°С. Рассчитываем абсолютную погрешность:
t1 - теоретическое
значение температуры плавления,
t2 - значение,
определенное экспериментально.
Δ=|t1
- t2|=|71 - 68.5|=2.5
Рассчитываем относительную погрешность:
δ=Δ/t1∙100%=2.5/71∙100=3.52%
Достаточно высокую погрешность можно объяснить
присутствием примесей, которые трудно отделить обычной перекристаллизацией.
Проверили растворимость 2-нафтилацетата в четырех
разных растворителях: воде, ацетоне, диэтиловом эфире и этаноле. В четыре
пробирки поместили небольшое количество вещества и добавили растворители.
Полное растворение было отмечено в эфире, ацетоне, этаноле. Растворения в
горячей и холодной воде не произошло.
.2 Идентификация
Для определения 2-нафтилацетата нужно провести
качественную реакцию. Уравнения реакции:

В пробирку вносим небольшое количество
полученного вещества, добавляем 3 мл воды, немного раствора щелочи и кипятим
жидкость 1 - 2 минуты. Затем раствор охлаждаем, добавляем соляной кислоты и
несколько капель раствора хлорида железа (III).
Появляется зеленоватая окраска (реакция на 2-нафтол).
.3 Выход продукта
Вычислим теоретический выход. Как уже было
сказано ранее, 2-нафтол взят в недостатке, в количестве 0,07 моль,
следовательно ν(2-нафтилацетат) =
0,07 моль.
Рассчитываем теоретический выход 2-нафтилацетата
, используя формулу 3:
mт(С6Н5NH2)
= 0,07∙186,21 =13,03 г.
Выход вещества от теоретического (по уравнению)ηт,%:

 ,(3)
,(3)
где mp - масса
полученного вещества,
mТ -
теоретическая масса вещества.
ηт=6,3/13,03∙100=48,35 %
Выход вещества от указанного в
методикеηм:

 ,(4)
,(4)
гдеmp - масса
полученного вещества,
mМ -масса
вещества, указанная в методике.
ηм=6,3/13∙100=48,46%
Все данные, полученные в ходе работы
сводим в таблицу 4.
Таблица 3 - Выход и
физико-химические константы
|
Название
вещества, формула
|
Константа
вещества
|
Выход
вещества
|
|
|
mp,г
|
%
|
|
|
Установленная
в работе
|
По
литературным данным
|
|
От
теоретического, ηт
|
От
указанного в методике, ηм
|
|
2-нафтилацетат
C12H10O2
|
tпл, °С
|
68,5
|
6,3
|
48,35
|
48,46
|
6 ВЫВОДЫ И РЕКОМЕНДАЦИИ
· В ходе синтеза был получен
2-нафтилацетат, представляющий собой кристаллическое вещество темно бежевого
цвета. Была проведена очистка вещества. Качественная реакция дала положительный
эффект. Также для 2-нафтилацетата определена экспериментальным путем
температура плавления, которая отличается от теоретического показателя на
3,52%. При исследовании вещества на растворимость в воде, ацетоне, эфире и
этаноле, полученные результаты совпадают со справочными, 2-нафтилацетат
растворился в диэтиловом эфире, ацетоне и этаноле.
· Выход продукта равен 6,3 г, что
составляет 48,35 и 48,36% от выхода по уравнению реакции и от выхода по
методике соответственно. Причины небольшого выхода продукта: потери при
проведении синтеза, в процессе очистки часть вещества удалялась вместе с
примесями, по методике исходный 2-нафтол следует подвергать очистке методом
перекристаллизации, но в данном синтезе использовался неперекристаллизованный
реактив, что могло помешать большему образованию 2-нафтилацетата. Чтобы
увеличить выход продукта следует проводить очистку исходного 2-нафтола.
· Так как вещество получилось более
темного цвета, чем описано в методике, а температура плавления отличается
оттеоретической на 3,5%, можно предположить, что в нем еще осталось некоторое
количество примесей.
· Данная методика получения
2-нрафтилацетата вполне приемлема для проведения синтеза в лабораторных условиях,
так как не требует особенных условий реакции и протекает достаточно быстро.
Выбранный синтез 2-нафтилацетата практически безвреден для экологии, но может
оказывать вредное воздействие на человека в силу токсичности 2-нафтола,
уксусного ангидрида и гидроксида натрия.
· Полученное вещество применяется в
парфюмерии, в качестве отдушек в мыловарении.
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
1. Артеменко А.И. Органическая
химия: Учеб.для строит. спец. вузов - 5-е изд., испр. - М.: Высш. Шк., 2002. -
559 с.: ил.
. Ким А.М. Органическая
химия: учеб.пособие. - 2-е изд., испр. и доп. - Новосибирск: Сиб. унив. Изд-во,
2001. - 814 с.
. Практикум по органическому
синтезу. Учеб.пособие для студентов пед. ин-тов.М., «Просвещение», 1974, 240
стр.
. Храмкина М.Н. Практикум по
органическому синтезу. Изд. 3-е, испр., Л., «Химия», 1974, 320 стр.
5. Интернет
энциклопедия «Википедия»:<#"528864.files/image032.gif">
Рисунок А1 - Приспособление для горячего
фильтрования (перекристаллизации): 1 - электроплитка, 2 - растворитель, 3 -
химический стакан, 4 - воронка с фильтром, 5 часовое стекло

Рисунок А2 - Установка для фильтрования под
вакуумом: 1 - воронка Бюхнера с бумажным фильтром, 2 - резиновая пробка, 3 -
колба Бунзена, 4 -резиновая трубка к вакуум-насосу

Рисунок 3 - Прибор для определения температуры
плавления: а - термометр с капилляром помещенный в пробирку, б - крепление на
термометре капилляра с веществом.