Хлорирование воды
Хлорирование
воды
Для
обеззараживания воды хлорированием на водоочистных
комплексах используют хлорную известь, хлор и его производные, под действием
которых бактерии, находящиеся в воде, погибают в результате окисления веществ,
входящих в состав протоплазмы клеток. Хлор действует и на органические
вещества, окисляя их.
Для
качественного хлорирования необходимо хорошее перемешивание, а затем не менее,
чем 30-минутный (при совместных хлорировании и аммонизации 60-минутный) контакт
хлора с водой, прежде, чем вода поступит к потребителю. Контакт может
происходить в резервуаре фильтрованной воды или в трубопроводе подачи воды
потребителю, если последний имеет достаточную длину без водоразбора.
Дозу
хлора
устанавливают технологическим анализом из расчета, чтобы в 1 мл воды,
поступающей к потребителю, осталось 0,3... 0,5 мг хлора, не вступившего в
реакцию (остаточного хлора), который является показателем достаточности
Принятой дозы хлора. При этом условии доза хлора при хлорировании
фильтрированной воды составляет 2 ... 3 мг/л в зависимости от ее
хлоропоглощаемости, а при хлорировании подземной воды — 0,7... 1 мг/л. При
выключении на промывку или ремонт одного из резервуаров фильтрованной воды,
когда не обеспечивается время контакта воды с хлором, доза хлора должна быть
увеличена вдвое.
Хлорирование
воды
осуществляется жидким (газообразным) хлором. На малых водоочистных комплексах
(до 3000 м3/сут) допускается применение хлорной извести. При плюсовых
температурах и атмосферном давлении хлор представляет собой газ
зеленовато-желтого цвета с удушливым запахом и плотностью, значительно большей,
чем плотность воздуха (в 1,5... 2,5 раза в зависимости от температуры). При
повышении давления (при плюсовых температурах) хлор переходит в жидкое
состояние. В таком виде его перевозят и хранят в специальных стальных емкостях
(при давлении 0,6...1,0 МПа).

Рис.
14.1. Баллон (а) и контейнер (б) для хлора.
1
— стальной корпус; 2 — кольцо горловины; 3
— колпак; 4 — запорный вентиль; 5 —
сифонная трубка
В
настоящее время заводы по производству хлора поставляют хлор в основном в
баллонах двух типов: Е-24 (рис. 14.1, а) вместимостью до 25 ... 30 кг жидкого
хлора и Е-54 с содержанием хлора до 100 кг и в бочках. На крупных водоочистных
комплексах производительностью более 100 тыс. м3/сут хлор доставляют обычно в
специальных железнодорожных цистернах вместимостью до 48 т жидкого хлора, а
хранят его в бочках (рис. 14.1,6), которые в зависимости от размеров вмещают от
700 до 3000 кг жидкого хлора. Хлорное хозяйство должно обеспечивать прием,
хранение, испарение жидкого хлора, дозирование газообразного хлора с получением
хлорной воды.
Хлорное
хозяйство располагают в отдельно размещаемых хлораторных, где
сблокированы расходный склад хлора, испарительная и хлордозаторная. Расходный
склад хлора можно размещать в отдельных зданиях или вплотную к хлораторной,
отделяя его глухой стеной без проемов. Склад хлора в составе хлораторных можно
не предусматривать, в этом случае в хлордозаторной разрешается хранение одного
баллона жидкого хлора массой не более 70 кг. Хлордозаторные без испарителей,
размещаемые в блоке с другими зданиями комплекса или вспомогательными
помещениями хлорного хозяйства, отделяют от других помещений глухой стеной без
проемов и оборудуют два выхода наружу, при этом один из них должен иметь тамбур.
Трубопроводы передачи хлорной воды выполняют из поливинилхлорида, резины,
полиэтилена высокой плотности и др.
Хлорирование
воды
является надежным средством, предотвращающим распространение эпидемий, так как
большинство патогенных бактерий (бациллы брюшного тифа, туберкулеза и дизентерии,
вибрионы холеры, вирусы полиомиелита и энцефалита) весьма нестойки по отношению
к хлору. Спорообразующих бактерий хлор не уничтожает, что является одним из
недостатков этого метода обеззараживания.
Гидролиз
хлора происходит (рис. 14.2) в соответствии с Уравнением
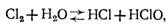
С
образованием хлорноватистой кислоты, которая диссоциирует на соляную кислоту и
атомарный кислород (в нейтральной или щелочной среде), обладающий сильными
окислительными свойствами. Ю. Ю. Лурье считает, что хлорноватистая кислота
диссоциирует в зависимости от рН с образованием гипохлоритного иона (ОСl-),
при этом окислительное воздействие на микроорганизмы оказывает как сама хлорноватистая
кислота, так и главным образом гипохлоритный ион:

При
применении вместо хлора хлорной извести имеет место реакция
2СаОС12
+ 2Н2О → СаС12 + Сa
(ОН)2 +
2НС10.
Дальнейшая
диссоциация хлорноватистой кислоты происходит аналогично описанному выше.

Эффект
подавления бактериальной жизни при хлорировании зависит от дозы
введенного хлора и продолжительности контакта его с водой. Поэтому
хлоропоглощаемость одной и той же воды, равная суммарному расходу хлора на
окисление микроорганизмов, органических и неорганических примесей, — величина
переменная, зависящая от дозы введенного хлора, продолжительности контакта,
величины рН, температуры воды и др. (рис. 14.3). Очевидно, что доза вводимого
хлора должна
Рис.
14.3. Зависимость хлоропоглощаемости от времени контакта хлора с водой: дозы
хлора, мг/л: 1 — 0,5;
2 — 0,75;
3
— 2,0;
4 —
4,0; 5 — 20,0
Быть
больше величины хлоропоглощаемости на величину остаточного хлора, присутствие
которого является гарантией того, что окисление бактерий и органических веществ
в воде практически завершено. Связь между дозой введенного в воду хлора и
содержанием остаточного хлора может иметь прямолинейный характер или ярко
выраженный излом (рис. 14.4). Непрямолинейный характер этой зависимости имеет
место при наличии в хлорируемой воде аммиака. Первая точка перелома на кривой 2
соответствует образованию монохлорамина NH2Cl
с
меньшим, чем у хлора окислительно-восстановительным потенциалом. Вторая —
переломная точка кривой соответствует моменту окисления образовавшегося
монохлорамина избыточным хлором.

Рис.
14.4. Зависимость остаточного хлора от дозы введенного
в воду при отсутствии (1) и при наличии (2) в ней аммонийных солей
На
практике в соответствии с качеством исходной воды применяют одно- или
двухкратное хлорирование воды. При обработке высокоцветных вод, а также вод,
богатых органическими веществами и бактериями, применяют двукратное
хлорирование. При этом хлор в воду дозируется сначала перед камерами
хлопьеобразования или осветлителями (предварительное хлорирование), а затем в
фильтрованную воду, перед резервуаром чистой воды. Предварительное хлорирование
необходимо для окисления органических защитных коллоидов, препятствующих
процессу коагуляции, а также окисления гуминовых веществ, обусловливающих
цветность воды, с целью экономии коагулянта, расходуемого на ее обесцвечивание.
Доза хлора на предварительное хлорирование значительно выше той, которая
вводится в фильтрованную воду, и может доходить до 5 мг/л.
В
некоторых случаях может возникнуть необходимость хлорирования воды повышенными
дозами хлора, т. е. применения так называемого перехлорирования, гарантирующего
высокий эффект ее обеззараживания. После перехлорирования воды остаточная
концентрация хлора в ней достаточно велика (1...7 мг/л), поэтому приходится прибегать
к последующему ее дехлорированию. Для этого чаще всего применяют обработку воды
сульфитом натрия, сернистым газом и фильтрование дехлорируемой воды через
активированный уголь. Дехлорирование воды сульфитом натрия, считая 3,5 мг (в
расчете на Na2S03-7H20)
на
1 мг связываемого хлора, протекает по уравнению
Na2S03
+ Н20
+ С12
= Na2S04 + 2НС1.
Дехлорирование
воды сернистым газом (в соотношении, примерно 1:1)
происходит в соответствии с уравнением
S02
+
2H2O
+ С12
→ H2S04
+
2НС1.
При
длительном пребывании питьевой воды перед поступлением к потребителям в
резервуарах и водоводах (более 1,5 ч) для продления бактерицидного действия
хлора, а также для предотвращения хлорфенольных запахов в воду кроме него
вводят также и аммиак. Введение аммиака, кроме того, сокращает расход хлора и в
ряде случаев улучшает вкус воды. При взаимодействии хлорноватистой кислоты
(образовавшейся при хлорировании воды) с аммиаком получаются монохлорамины:
HOCI
+
NH3 → NH2CI + Н2О,
которые,
гидролизуясь, образуют сильный окислитель — гипохлоритный ион:
NH2C1
+
Н20 → NH4+ + ОСl-.
Гидролиз
хлораминов протекает довольно медленно, поэтому в первое время
окислительное действие хлораминов ниже, чем хлора, но длительность
бактериального действия хлораминов значительно больше, в связи с чем и
применяют аммонизацию воды перед длительным ее пребыванием в резервуарах,
водоводах и сети. Соотношение доз хлора и аммиака зависит от качества исходной
воды. Обычно оптимальной, обеспечивающей образование монохлораминов, является
доза аммиака в пять-шесть раз меньше дозы хлора.
Аммиачное
хозяйство организуют аналогично хлорному и располагают в
отдельных помещениях. Аммиак хранят в расходном складе в баллонах или
контейнерах. Ввод аммиака производят в фильтрат при наличии фенолов — за 2 ...
3 мин до ввода хлора.
Различают
свободный хлор (молекулярный хлор, хлорноватистая кислота и
гипохлорит-ионы) и связанный (хлор, в виде хлораминов). Свободный хлор в 20—25
раз более бактерициден, чем связанный. С увеличением рН воды уменьшается
содержание связанного хлора.
На
бактерицидный эффект хлорирования значительно влияет
первоначальная доза хлора и продолжительность сохранения в обрабатываемой воде
его некоторой остаточной концентрации. Минимальная продолжительность контакта
30 мин при остаточном содержании свободного хлора 0,3—0,5 мг/л. Из патогенных
микроорганизмов наиболее чувствительны к хлору: холерный вибрион, бациллы
брюшного тифа и дизентерии. Паратиф В и микрокок более резистентны, на споровые
формы хлор почти не действует.
Количество
хлора, расходуемого на окисление примесей воды, называется хлоропоглощаемостью,
которая определяется как разница между количеством введенного хлора и его
концентрацией в воде через 30 мин контакта.
К
числу производных хлора, используемых при обеззараживании, относят: гипохлориты
натрия (NaClO*5H20),
кальция
[Са(С10)2], хлорит натрия (NaClO2),
оксид
хлора СlO2.
Гипохлорит
натрия
получают электролизом раствора поваренной соли в электролизере без диафрагмы.
При этом вначале выделяются: на аноде — хлор, а на катоде — едкий натрий,
которые взаимодействуя образуют гипохлорит натрия.
Хлорит
натрия
— сильный окислитель, в твердом состоянии — негорюч и не самовоспламеняем. Его
растворимость в0оде ПРИ 5 "С — 340, а при 60 °С — 550 г/л. При рН=2 он
разлагается с образованием оксида хлора(IV) и соляной кис- доты, при рН около 4
разложение замедляется, а при рН=7 он не разлагается. Его широко используют для
получения оксида хлора (IV). Оксид хлора (IV)
—
зеленовато-желтый газ с резким запахом, легко взрывается от электрической
искры, при солнечном освещении и при нагревании свыше 60ºС. Взрывоопасен в
обычных условиях при контакте со многими органическими веществами (нефть,
бензин и пр.). Его окислительный потенциал в кислой среде 1,5 В. Растворимость
оксида хлора (IV) в воде при 25°С — 81,06, а при 40 °С — 51,4 г/л. Его водные
растворы имеют более интенсивную окраску по сравнению с хлорной водой. На
водоочистных комплексах оксид хлора (IV) можно получать взаимодействием хлорита
натрия и хлора или с разбавленной соляной кислотой, либо озоном. Он обладает
более высоким бактерицидным и дезодорирующим действием, чем хлор. Присутствие в
воде аммонийных солей не влияет на его окислительные свойства. При обработке
вод, содержащих фенолы, не возникают хлорфенольные запахи, так как фенол
практически полностью окисляется оксидом хлора(IV) до малеиновой кислоты и
хинона, не имеющих в малых концентрациях запаха и привкуса.
Скорость
процесса обеззараживания воды хлором и его производными
определяется кинетикой диффузии оксиданта внутрь клетки и интенсивностью
отмирания клеток вследствие нарушения метаболизма (обмена веществ). С ростом
концентрации хлора в воде, повышением ее температуры и переводом его в
сравнительно легко диффундирующую, недиссоциированную форму скорость процесса
обеззараживания возрастает.
Бактерицидное
действие хлора уменьшается с повышением рН воды. Поэтому
обеззараживание воды хлором следует производить по возможности при более
высоких температурах и низких значениях рН (до ввода щелочных реагентов).
Содержащиеся в воде органические примеси, способные к окислению,
восстановители, коллоидные и диспергированные вещества, обволакивающие
бактерии, тормозят процесс обеззараживания воды.
Для
дозирования в воду хлора, аммиака и сернистого газа (при
дехлорировании) применяют вакуумные газодозаторы системы ЛОНИИ-100 (рис. 14.5)
и системы Л. А. Кульского (рис. 14.6). Из баллонов, установленных на
специальные весы (для контроля за расходом хлора), жидкий хлор передается в
Промежуточный баллон, где происходит его испарение и отделение загрязняющих
хлор примесей. Далее уже газообразный хлор проходит через фильтр со стекловатой
(для окончательной очистки хлор-газа) и через понижающий давление редуктор.
Степень понижения давления фиксируется двумя манометрами, установленными до и
после редукционного клапана. С помощью диафрагмы создается перепад давлений,
который служит импульсом для работы измерителя расхода хлора. Затем хлор,
поступая в смеситель, смешивается с водопроводной водой, образуя хлорную воду,
которая засасывается эжектором и отводится по назначению.
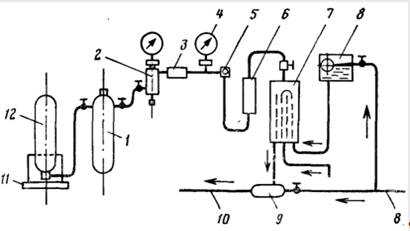
Рис.
14.5. Вакуумный хлоратор ЛОНИИ-100.
1
—
промежуточный баллон; 2 — фильтр со стекловатой;3— редукционный клапан для
снижения давления хлор-газа; 4— манометр; 5
— измерительная диафрагма; 6 — ротаметр; 7 —
смеситель; 8 — подача водопроводной воды;
9
— эжектор, создающий разряжение в хлораторе; 10 — отвод хлорной воды на
дозирование; 11 — весы; 12 — баллон с хлором
вода хлорирование обеззараживание газодозатор
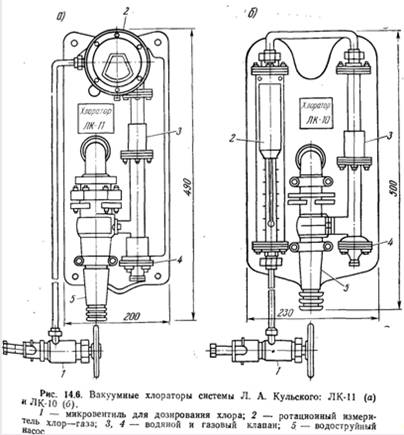
Вакуумные
хлораторы системы Л. А. Кульского показаны на рис. 14.6 —
хлоратор ЛК-11 средней производительности (рис. 14.6,а) для расхода хлора в
пределах 0,5 ... 4,5 кг/ч и хлоратор ЛК-10 малой производительности (рис.
14.6,6), рассчитанный на расход хлора в пределах 40 ... 800 г/ч.
Количество
резервных хлораторов на одну точку ввода рекомендуется принимать: при 1 ... 2
рабочих хлораторах — один резервный, при более двух — 2. Допускается
предусматривать общие резервные хлораторы для предварительного и вторичного
хлорирования воды.
С
одного стандартного баллона при обычной комнатной температуре можно получить не
более 0,5... 0,7 кг/ч хлор-газа. Поэтому на крупных водоочистных комплексах с
большим расходом хлора для увеличения съема хлора прибегают к специальному
обогреву баллонов (теплой водой или подогретым воздухом при температуре 10...
30°С). Испаритель оборудуют устройствами для контроля температуры воды и
давления хлора и воды. На водоочистных комплексах большой производительности
применяют бочки, величина съема хлора с которых на 1 м2 составляет около 3
кг/ч, при комнатной температуре.
Учитывая,
что хлор является отравляющим газом, при проектировании хлораторных установок
следует предусматривать необходимые меры, обеспечивающие безопасность
обслуживающего персонала.
К
числу этих мер относятся: наличие двух выходов из хлораторной, расположение
хлораторной на первом этаже; наличие приточно-вытяжной вентиляции с устройством
вытяжки в наиболее низкой части хлораторной, в месте, противоположном от входа
в хлораторную; устройство электроосвещения с газозащитной герметической
аппаратурой; наличие тамбура с размещением в нем спецодежды и противогазов, а
также устройств для включения и выключения вентиляции и освещения.
При
хлорировании воды отстоенным раствором хлорной извести крепостью 1 ... 1,5% его
приготавливают таким же способом, как и раствор коагулянта. Аналогичные
устройства служат и для дозирования раствора. Ввиду сильного коррозионного
действия раствора хлорной извести баки для его приготовления следует применять
деревянные, пластмассовые или железобетонные, а арматуру и трубы, — из
полиэтилена или винипласта. Объем растворных баков, м3, определяют по формуле
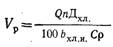
где
Q —
расчетный расход воды, м3/ч; n=
12 ... 24 ч — количество часов, на которое заготавливается раствор хлорной
извести; Дхл. :— принятая доза активного хлора, мг/л; bхл.и=1.....2
— концентрация раствора хлорной извести, %; С=25... ... 30 — содержание
активного хлора в продажной хлорной извести, %; р=1 — плотность раствора
хлорной извести, т/м3.
Литература
Алексеев
Л. С., Гладков В. А. Улучшение качества мягких вод. М.,
Стройиздат,
1994 г.
Аюкаев
Р. И., Мельцер В. 3. Производство и применение фильтрующих
материалов
для очистки воды. Л., 1985.
Вейцер
Ю. М., Мииц Д. М. Высокомолекулярные флокулянты в процессах
очистки воды. М., 1984.
Егоров
А. И. Гидравлика напорных трубчатых систем в водопроводных очистных
сооружениях. М., 1984.
Журба
М. Г. Очистки воды на зернистых фильтрах. Львов, 1980.