Технология производства полиакрилонитрила
Технология производства полиакрилонитрила
Введение
Полимер нитрила акриловой кислоты
(полиакрилонитрил) был впервые получен Моро в 1893 г. из этиленциангидрина
и амида акриловой кислоты. Затем в 1931 г. Карозерс разработал метод
получения латексов из полиакрилонитрила. Позднее, в 1940 году был предложен
метод сополимеризации акрилонитрила с бутадиеном (нитрильный каучук).
Поскольку полиакрилонитрил не растворялся в
известных органических растворителях, его невозможно было перерабатывать в
волокна. Впервые волокно из полиакрилонитрила получили с использованием в
качестве растворителя диметилформамида.
Позднее было установлено, что полиакрилонитрил
растворяется в концентрированном водном растворе роданида натрия или кальция.
Это имело большое значение для усовершенствования технологии получения полиакрилонитрила.
Полиакрилонитрил
и сополимеры на его основе нашли широкое применение в производстве волокон
широкого назначения, бутадиен-нитрильного каучука, ударопрочного полистирола и
других продуктов [1, С. 132].
1.
Структура
полиакрилонитрила
Полиакрилонитрил – труднокристаллизующийся
линейный, карбоцепный полимер белого цвета. Структурная формула:

Методом ЯМР удалось установить, что
микроструктура полиакрилонитрила зависит от условий полимеризации
акрилонитрила. В присутствии радикальных инициаторов (например, перекиси
бензоила, окислительно-восстановительных систем) при 40–80°С, а также анионных
катализаторов (бутиллития) или под действием 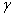 -излучения
при -78°С образуется полиакрилонитрил одновременно синдио- и изотактической
структуры (1:1). При получении полиакрилонитрила в канальных комплексах
(например, в комплексе акрилонитрила с мочевиной) при -78°С и радиационном
инициировании доля изотактической структуры возрастает до 75–90%.
-излучения
при -78°С образуется полиакрилонитрил одновременно синдио- и изотактической
структуры (1:1). При получении полиакрилонитрила в канальных комплексах
(например, в комплексе акрилонитрила с мочевиной) при -78°С и радиационном
инициировании доля изотактической структуры возрастает до 75–90%.
В зависимости
от условий полимеризации акрилонитрила могут быть получены полимеры различного
молекулярного веса (20000–350000).
Зависимость между молекулярной массой и
характеристической вязкостью [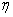 ], определяемой в
диметилформамиде (С=2–20 г./л) при 20°С, выражается уравнением [
], определяемой в
диметилформамиде (С=2–20 г./л) при 20°С, выражается уравнением [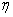 ]=K*10-3*M
]=K*10-3*M , в котором К и
, в котором К и  соответственно попарно равны: 1,75 и
0,66; 2,5 и 0,66; 0,233 и 0,75; 0,166 и 0,81; 0,392 и 0,75; 0,34 и 0,73; 0,317
и 0,746; 0,278 и 0,76. величины этих коэффициентов зависят от способа приготовления
раствора акрилонитрила [3, С. 354].
соответственно попарно равны: 1,75 и
0,66; 2,5 и 0,66; 0,233 и 0,75; 0,166 и 0,81; 0,392 и 0,75; 0,34 и 0,73; 0,317
и 0,746; 0,278 и 0,76. величины этих коэффициентов зависят от способа приготовления
раствора акрилонитрила [3, С. 354].
Молекулярно-массовое распределение
полиакрилонитрила, соответствующее преобладающему способу обрыва цепи
(рекомбинацией), характеризуется кривой с одним максимумом в случае гомогенной
полимеризации (при отсутствии модифицирующего действия среды, например,
диметилформамида или роданидов) и кривой с тремя максимумами в случае
гетерофазной полимеризации. Специальные виды волокон (прочные, термостойкие)
формуют из полиакрилонитрила, характеризующегося узким молекулярно-массовым
распределением, т. к. максимально возможная при вытяжке ориентация
уменьшается с увеличением полидисперсности. Полиакрилонитрил с наиболее
узким молекулярно-массовым распределением образуется при анионной полимеризации
акрилонитрила. При радикальной полимеризации акрилонитрила в гетерогенных
условиях образуется полиакрилонитрил с наиболее широким молекулярно-массовым
распределением.
Значение
стерического фактора (гибкости) макромолекулы полиакрилонитрила  =2,5–3,2, а длина сегмента Куна 3,17 нм
[5, С. 150].
=2,5–3,2, а длина сегмента Куна 3,17 нм
[5, С. 150].
2. Свойства полиакрилонитрила
2.1 Химические
Полиакрилонитрил
при нагревании изменяет свой цвет, причем этот процесс всегда сопровождается
потерей растворимости. Предполагается, что изменение окраски связано с
образованием азометиновых мостиков между соседними макромолекулами, чему
благоприятствует сильное притяжение, существующее между атомом азота и подвижным
атомом водорода, находящимся в  – положении:
– положении:

Стабилизация
полиакрилонитрила и его сополимеров может быть произведена добавлением N-алкилоксиацетамидов
(N, N-диметил-, N-этил-, N-метил-, N, N-диэтилоксиацетамидов). При стабилизации
вводят 1–20% одного из указанных соединений. Для создания тепло- и
светоустойчивых композиции можно приготовить при использовании стабилизаторов
общей формулы R2NCH2СH2CN, например 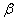 -диметиламинопропионитрила или
-диметиламинопропионитрила или 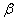 -n-бутиламинопропионитрила
[3, C.
354].
-n-бутиламинопропионитрила
[3, C.
354].
Термическое воздействие (выше 150°С) вызывает
необратимые изменения в химическом строении макромолекулы полиакрилонитрила,
являющиеся результатом последовательного взаимодействия групп – CN между собой с
образованием циклических структур. Это свойство полиакрилонитрила используется
при изготовлении углеродных волокон (волокон специального назначения).
Производство углеродных волокон на основе ПАН
волокон включает две стадии – термостабилизацию и карбонизацию. На стадии
термостабилизации ПАН волокна нагревают приблизительно до 180–300°С в кислородсодержащей
среде, при этом в структуре полимера протекает дополнительная ориентация.
Образующиеся одновременно поперечные межмолекулярные связи между цепями
позволяют избежать пиролиза при более высокой температуре. Довольно сложный
химизм процесса стабилизации в основном включает в себя циклизацию нитрильных
групп (C=N) и образование поперечных (межмолекулярных) связей цепных молекул,
сопровождающееся дегидрированием и окислительными реакциями. В ходе этого
процесса линейный полимер приобретает лестничную структуру [4, С. 30].

Образование хромофорных сопряженных связей – C=N–, вызывающее интенсивное
окрашивание полиакрилонитрила в оранжево-коричневый и далее в черный цвет,
промотируется нуклеофильными реагентами; наиболее эффективны карбоновые
кислоты, фенолы, имиды и менее активны амиды, алифатические амины, спирты,
альдегиды и кетоны (кроме ацетона). В инертной атмосфере такое превращение
протекает гладко и вплоть до 220°С не приводит к разрушению основной полимерной
цепи.
Нагревание на воздухе приводит к окислительному
дегидрированию с образованием конденсированных нафтиридиновых структур и осложняется
параллельно протекающими процессами термоокислительной деструкции полиакрилонитрила.

Продукты термического превращения
полиакрилонитрила нерастворимы в обычных для полиакрилонитрила растворителях и
обладают исключительно высокой термостойкостью: внесенные в пламя горелки
порошок или волокно черного цвета из термообработанного полиакрилонитрила
накаляются докрасна, но не горят [6, С. 44].
Полиакрилонитрил омыляется H2SO4 конц. (75–95%-ная)
на холоду; образуется хлопьевидный продукт белого цвета с молекулярной массой 62%
от исходной, содержащий амидные (молярная концентрация до 90%) и имидные звенья:

Этот продукт растворим в воде и слабых растворах
кислот и щелочей, но не растворим в диметилформамиде. Пленки, полученные из 20%-ного
водного раствора этого продукта, прозрачны и эластичны, но при высушивании становятся
хрупкими; при 200°С они сильно темнеют и при 250–260°С разрушаются, не плавясь.
Нагревание полиакрилонитрила в процессе
растворения в H2SO4 приводит к полному исчезновению амидных и имидных групп и
образованию карбоксильных групп.
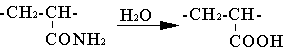
При обработке
полиакриламида раствором соды степень омыления достигает 30–40%. По
деструктивному действию омыляющие агенты можно расположить в следующий
возрастающий ряд: NaOH (1%-ный), НС1, НСООН, Na2CO3, H2SO4,
H3PO4. При взаимодействии полиакрилонитрила с
гидроксиламином при 50–100°С протекает реакция образования амидоксимных групп с
последующим выделением аммиака и образованием групп гидроксамовой кислоты:

Для реакции
применяется раствор сернокислого гидроксиламина и едкого натра в количестве,
достаточном для выделения – 99,2% гидроксиламина. Полимер после реакции
содержит как группы гидроксамовой кислоты, так и непрореагировавшие нитрильные
группы. Наличие в полимере групп гидроксамовой кислоты способствует лучшему
окрашиванию полиакрилонитрильного волокна.
2.2 Физические
Полиакрилонитрил
в отличие от других акриловых смол не растворяется в обычных растворителях. Эта
особенность объясняется значительными межмолекулярными силами, возникающими
вследствие полярной природы – С = N-групп. Представления о влиянии водородных
связей в полимерах на их растворимость в полярных растворителях и установление
растворимости полиакрилонитрила в гидротропных растворителях (например, в
концентрированном водном растворе роданистого кальция), послужили толчком к
поискам высокополярных растворителей.
Так как группа – CN является сильно
полярной, то полиакрилонитрил растворяется только в очень полярных
растворителях, например, в диметилформамиде, диметилацетамиде, этиленкарбонате,
диметилсульфоксиде, концентрированных водных растворах бромистого лития,
роданистого натрия или кальция, смеси ZnCl2+CaCl2, концентрированных HNO3 и H2SO4 (в последнем случае
группы – CN гидролизуются).
Показатель растворимости полиакрилонитрила  =30,8*10-3 (Дж/м3)0,5, а воды
=30,8*10-3 (Дж/м3)0,5, а воды  =46,4*10-3 (Дж/м3)0,5 напомним,
что растворение полимера в растворителе происходит при значениях
=46,4*10-3 (Дж/м3)0,5 напомним,
что растворение полимера в растворителе происходит при значениях 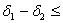 4 (Дж/м3)0,5, т.е.
4 (Дж/м3)0,5, т.е.
 должен быть почти равен
должен быть почти равен 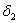 , что для воды и полиакрилонитрила не
наблюдается [4, C. 99].
, что для воды и полиакрилонитрила не
наблюдается [4, C. 99].
При нагревании полиакрилонитрил растворяется в N-формилпиперидине (170–180°С),
цианацетамиде (165–170°С), N-метил-иианацетамиде (180–190°С), этиленциангидрине (165–170°С),
однако при охлаждении этих растворов образуются гели (происходит застудневание).
Предполагается, что механизм застудневания растворов полиакрилонитрила
заключается в образовании трехмерной сетки за счет возникновения вторичных
межмолекулярных связей. Скорость застудневания повышается при увеличении
концентрации растворов, молекулярного веса полимера и количества введенной воды
[6, С. 43].
Растворители
способные разрушить межмолекулярные связи в полимере это диметилформамид и
тетраметиленсульфон, динитрил малоновой и янтарной кислот, смеси, содержащие
более 60% этиленкарбоната и воды, диметилцианамид, концентрированные водные
растворы некоторых солей, например бромистого лития, роданистого натрия и
кальция, хлористого цинка.
Для снижения
растворимости полиакрилонитрил обрабатывают водным раствором формальдегида.
Таблица 1 Свойства полиакрилонитрила
|
Свойство
|
Значение
|
|
Плотность, г/см3
|
1,14–1,15
|
|
Показатель преломления,
n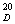
|
1,49–1,52
|
|
Температура
размягчения (с одновременной деструкцией), °С
|
220–230
|
|
Удельная теплоемкость, кДж/(кг*К) [кал/(г*°С)]
|
1,51
|
|
Прочность
при растяжении (для волокна), Мн/м2 (кгс/мм2)
|
600 (60)
|
|
Относительное
удлинение, %
|
10–35
|
|
Влагопоглощение
отпрессованного образца, %
|
1–2
|
|
Дипольный
момент, к*м (D)
|
1,13–10-4
|
|
Диэлектрическая проницаемость при
|
|
|
50 гц
|
6,5
|
|
1 Мгц
|
4,2
|
|
Удельное объемное электрическое сопротивление, Том*м (Ом*см)
|
1 (1014)
|
|
Тангенс угла диэлектрических потерь при
|
|
|
50 гц
|
|
1 Мгц
|
0,03
|
Для полиакрилонитрила характерны две температуры
стеклования. Первая из них лежит в области от 86 до 96,5 °C. Зависимость ее от
молекулярной массы хорошо описывается уравнением Флори:
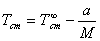
где а=(2,8±0,1)*105; Т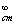 =(96,5±1,0)°С, т.е.
значение при М
=(96,5±1,0)°С, т.е.
значение при М . Вторая температураpa стеклования составляет
около 140°С и определяется сдвигом равновесия дипольного взаимодействия нитрильных
групп [6, С. 43].
. Вторая температураpa стеклования составляет
около 140°С и определяется сдвигом равновесия дипольного взаимодействия нитрильных
групп [6, С. 43].
2.3 Термические
Полиакрилонитрил
при нагревании в атмосфере азота не претерпевает никаких изменений до 200°С, но
при более высокой температуре происходит его размягчение и появление
газообразных продуктов, главным образом аммиака NH3, и водорода Н2.
При 270°С наблюдается также выделение цианистого водорода HCN. Из жидких продуктов
распада полимера можно выделить вещества, содержащие группы – NH2 и –
С = N. Также присутствуют винилацетонитрил и вещества, являющиеся димерами,
тримерами и тетрамерами акрилонитрила. Полимер окрашивается и становится
нерастворимым.
Энергия активации термической деструкции 130 кДж/молъ
(31 ккал / молъ).
При нагревании растворов полиакрилонитрила в
диметилформамиде в токе воздуха, кислорода или в инертной атмосфере в течение
30–40 часов полиакрилонитрил также окрашивается в желтый и далее в
темно-коричневый цвет; образующиеся при этом сопряженные системы растворимы в
диметилформамиде [6, С. 44].
При
температурах выше 700°С полиакрилонитрил подвергается химическому превращению в
полимер циклической структуры, содержащий сопряженные двойные связи. В
зависимости от условий пиролиза (вакуум или воздух, водород, азот и аммиак под
давлением) образуются продукты с различными свойствами. В ряде случаев может
быть получен продукт графитовой структуры, обладающий свойствами
полупроводников (удельная электропроводность 10-10 – 10-13
Мом/см).
При
длительной термической обработке полиакрилонитрильного волокна или ткани в
азоте и на воздухе получен термостойкий материал, выдерживающий кратковременное
воздействие пламени горелки и сохраняющий достаточную прочность.
3. Производство полиакрилонитрила
Акрилонитрил в присутствии инициаторов легко
вступает в редакцию полимеризации, сопровождающуюся выделением 73,3 кДж/моль
тепла.
В качестве инициаторов применяют пероксиды, азо-
и диазосоединения, а также элементоорганические соединения [1, С. 132].
Кислород ингибирует полимеризацию акрилонитрила,
поэтому процесс проводят в среде азота. Скорость реакции значительно возрастает
в присутствии следов ионов меди или железа.
При полимеризации акрилонитрила используют также
окислительно-восстановительные системы. Чаще всего применяют персульфат аммония
с тиосульфатом или гидросульфитом натрия, что позволяет проводить реакцию при
более низких температурах и получать полимер с более высокой молекулярной
массой.
В промышленности полиакрилонитрил получают
радикальной полимеризацией акрилонитрила в гетерогенных или гомогенных
условиях. Производство полиакрилонитрила может быть осуществлено как
периодическим, так и непрерывным методами.
Непрерывный технологический процесс получения
полиакрилонитрила состоит из стадий приготовления растворов, полимеризации
акрилонитрила, демономеризации дисперсии и конденсации акрилонитрила, фильтрации,
промывки и сушки полимера.
полиакрилонитрил
химический карбоцепный
Таблица 2 Нормы загрузки
компонентов
|
Аппарат 4
|
|
Персульфат
калия, кг
|
3,0
|
|
Вода
обессоленная, м3
|
0,44
|
|
Аппарат 5
|
|
Метагидросульфит
натрия, кг
|
0,1
|
|
Вода
обессоленная, м3
|
0,050
|
|
Аппарат 6
|
|
НАК, м3/ч
|
0,0224
|
|
Раствор
персульфата калия, м3/ч
|
0,073
|
|
Раствор
метагидросульфита натрия, м3/ч
|
0,0246
|
Полимеризация проводиться при различных
температурах: зона 1 30–32°С, зона 2
30–32°С, зона 2 35–37°С, зона 3
35–37°С, зона 3 25–30°С.
25–30°С.
Полимеризацию акрилонитрила проводят в реакторе
непрерывного действия в водной среде в присутствии
окислительно-восстановительной инициирующей системы из персульфата калия и
метагидросульфита натрия. Степень превращения мономера в полимер равна 80–85%.
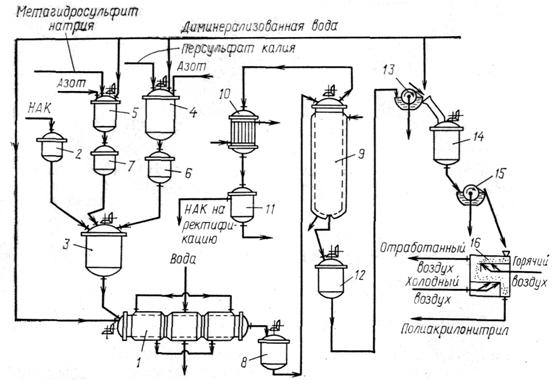
Рисунок 1 Схема
процесса производства полиакрилонитрила: 1 – полимеризатор; 2, 6, 7 – напорные
емкости; 3 – смеситель; 4, 5 – аппараты для растворения инициатора; 8 – промежуточная
емкость; 9 – колонна демономеризации – 10 – холодильник кожух отрубный; 11 – отстойник;
12 – сборник дисперсии полимера; 13, 15 – барабанные фильтры; 14 – репульпатор;
16 – сушилка с кипящим слоем
НАК подается
из напорной емкости 2 в смесительный аппарат 3. Водные растворы персульфата
калия и метагидросульфита натрия готовят в аппаратах для растворения 4, 5, из
которых они самотеком поступают в емкости 6, 7, а затем дозируются в аппарат 3.
Полученная дисперсия поступает в промежуточную
емкость 8, а затем в колонну 9 для отделения непрореагировавшего акрилонитрила
(демономеризации) путем отгонки. Демономеризация проводится при 50–60 °С и
остаточном давлении 6,6–20,0 кПа.
Пары акрилонитрила и воды конденсируются в
холодильнике 10. Конденсат поступает в отстойник 11, в котором он разделяется
на два слоя: верхний слой – акрилонитрил, нижний слой – 7%-ный раствор
акрилонитрила в воде.
Дисперсия полимера, из которой выделен
акрилонитрил, из аппарата 9 поступает в сборник 12, откуда периодически насосом
подается на вакуум-барабанный фильтр 13 для отделения полимера от маточного
раствора. Полимер с барабана срезается ножом и попадает на транспортный желоб.
Сюда же одновременно подается вода для смывания полимера в репульпатор 14. В
аппарате 14 полимер отмывается от остатков мономера и инициатора. Из репульпатора
пульпа подается на вакуум-барабанный фильтр 15. После фильтрации полимер с
влажностью 80% сушат в сушилке с кипящим слоем 16 до содержания влаги 0,7–1,5% [1,
С. 134].
Гетерофазная
полимеризация акрилонитрила характеризуется самоускорением (примерно до степени
превращения 20% при 60°С), которое обусловлено захватом макрорадикалов,
выпадающим в осадок полимером. Эффективные скорости роста захваченных макрорадикалов
зависят от температуры и степени экранирования активного центра свернутыми
цепями, препятствующими диффузии акрилонитрила и других реагентов в твердую
фазу.
Особенность
гетерофазной полимеризации – увеличение молекулярной массы полиакрилонитрила с
возрастанием степени превращения. Этот факт обусловлен захватом твердой фазой
макрорадикалов, которые при температуре ниже 60°С не гибнут. Гетерофазная
полимеризация акрилонитрила чувствительна к перемешиванию, центрифугированию,
так как в этих условиях возрастает числе столкновений глобул и, следовательно,
скорость обрыва цепи. Кислород в небольшом количестве способствует увеличению
скорости полимеризации вследствие дополнительного образования перекисей и гидроперекисей
акрилонитрила, служащих инициаторами. В присутствии большого количества
кислорода процесс ингибируется и в пределе может прерваться. Поэтому
полимеризацию с перемешиванием проводят в атмосфере инертного газа при охлаждении
реактора в изотермических условиях.
Скорость гетерофазной полимеризации акрилонитрила
v определяется суммой
скоростей Rs (в водном растворе акрилонитрила) и Rg (на глобулах полиакрилонитрила):

где kр и k р – константы скоростей
роста соответственно в водном растворе акрилонитрила и на глобулах
полиакрилонитрила; [М] – концентрация акрилонитрила в водном растворе; [М]адс
– эффективная концентрация акрилонитрила, адсорбированного на глобулах; [М'р]
– концентрация свободных радикалов в растворе; [р-] – концентрация
глобул в реакционной смеси.
р – константы скоростей
роста соответственно в водном растворе акрилонитрила и на глобулах
полиакрилонитрила; [М] – концентрация акрилонитрила в водном растворе; [М]адс
– эффективная концентрация акрилонитрила, адсорбированного на глобулах; [М'р]
– концентрация свободных радикалов в растворе; [р-] – концентрация
глобул в реакционной смеси.
Добавки Cu2O, Ni2O, MgO, A12O3, SiO2 к жидкому акрилонитрилу при -78°C или к твердому
акрилонитрилу при -196°С сенсибилизируют полимеризацию и повышают скорость
процесса. Акрилонитрил быстро полимеризуется в твердой фазе (степень превращения
~100%) в присутствии сильно измельченного катализатора (метод молекулярных
пучков); процесс особенно интенсивен при -160°С и -130°С (точки фазовых
переходов); при этом может иметь место взрывная полимеризация [6, С. 47].
Процесс
полимеризации акрилонитрила непрерывным методом осуществляется в реакторе с
мешалкой, в который непрерывно вводят акрилонитрил, водные растворы персульфата
аммония, восстановителя-активатора, например бисульфита или тиосульфата натрия,
и из которого непрерывно выводят суспензию полимера.
Радиационная полимеризация акрилонитрила под
действием 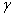 -лучей (60Со) и рентгеновских
лучей, а также быстрых электронов может протекать как по радикальному, так и по
анионному механизму в зависимости от температуры реакционной среды (жидкая или
твердая фаза).
-лучей (60Со) и рентгеновских
лучей, а также быстрых электронов может протекать как по радикальному, так и по
анионному механизму в зависимости от температуры реакционной среды (жидкая или
твердая фаза).
В жидкой фазе акрилонитрила полимеризуется с
самоускорением из-за радиолиза образующегося поли акрилонитрила и,
следовательно, повышенного выхода радикалов. Скорость (и) такого процесса (в массе) при
обрыве цепи рекомбинацией определяется выражением:
v=k*I 0,8,
где к – константа скорости роста; I – мощность дозы (17,2–430
мка/кг, или 4–100 р/мин). Энергии активации в интервале температур от -83
(т. пл.) до -116°С (твердая фаза), от -83 до 0 СС (жидкая фаза) и от
20 до 50 °С равны соответственно 0; 12,6 и 62,8 кДж/моль (0; 3 и 15 ккал /
моль). При воздействии 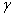 -лучей наблюдается
пост-эффект.
-лучей наблюдается
пост-эффект.
Производство полиакрилонитрила может
осуществляться в водных растворах минеральных солей – гомогенная полимеризация.
Гомогенную полимеризацию акрилонитрила можно
проводить в водных растворах солей NaCNS, Ca (CNS)2, ZnCl2+CaCl2 или MgCl2, Mg(ClО4)2.
Гомогенная полимеризация акрилонитрила в органических растворителях
(диметилформамид, диметилацетамид) в присутствии динитрила азодиизомасляной
кислоты возможна лишь при высоких концентрациях мономера в растворе до 25% [5,
С. 46].
Скорость гомогенной полимеризации акрилонитрила
определяется выражением:

где kи, kp, k0 – константы скорости соответственно инициирования, роста и
обрыва; [I]
– концентрация инициатора (или мощность дозы радиации); [М] -, концентрация
мономера.
Процесс проводят непрерывным способом в аппарате,
снабженном мешалкой, системой обогрева и охлаждения, при 79–80,5 °С и
атмосферном давлении. В реактор, содержащий 50,5%-ный водный раствор роданида
натрия, вводят смесь 92% акрилонитрила, 6% метилакрилата, 1% итаконовой кислоты,
0,1% инициатора – динитрила азобисизомасляной кислоты и другие добавки,
способствующие регулированию роста цепи. Реакционная смесь непрерывно подается
в аппарат снизу, а раствор полимера отводится сверху. Продолжительность
полимеризации 1–1,5 ч. Конверсия мономера составляет около 78% [1, С. 135].
При получении полиакрилонитрила в среде
органического растворителя (лаковый метод) полимеризации протекает в условиях,
при которых мономер и образующийся полимер находятся в растворе. В качестве
растворителей применяют диметилформамид (в большинстве случаев),
диметилацетамид,  -пирролидон и этиленкарбонат.
Инициатором обычно служит окислительно-восстановительная система, состоящая из
гидропероксида кумола и триэтаноламина. Наличие в полимере группы – CN, понижающей электронную
плотность двойной связи, способствует каталитической полимеризации акрилонитрила
по анионному механизму.
-пирролидон и этиленкарбонат.
Инициатором обычно служит окислительно-восстановительная система, состоящая из
гидропероксида кумола и триэтаноламина. Наличие в полимере группы – CN, понижающей электронную
плотность двойной связи, способствует каталитической полимеризации акрилонитрила
по анионному механизму.
Технологический режим и аппаратурное оформление
процесса мало отличаются от таковых при полимеризации акрилонитрила в водном
растворе солей.
Полиакрилонитрил получается в виде лака, который
используют в качестве прядильного раствора для получения волокна. При
необходимости из полиакрилонитрила можно выделить твердый порошкообразный полимер.
Полимеризация акрилонитрила в массе, или в блоке,
имеет ограниченное применение в промышленности и используется главным образом
для получения сополимеров акрилонитрила с другими мономерами. В результате
блочной полимеризации полиакрилонитрил получается в виде твердого порошка [1,
С. 135].
4. Применение полиакрилонитрила
Наиболее широко
полиакрилонитрил применяется для изготовления волокна различного назначения.
Для этой цели готовятся растворы полиакрилонитрила. Формование волокон
осуществляется по мокрому или сухому способу.

Рисунок 2.
Электронно-микроскопическое изображение бобовидного среза углеродного волокна,
полученного из ПАН волокна
При сухом
способе формования волокна раствор полиакрилонитрила продавливается через
фильеры в шахту навстречу току горячего воздуха. После выхода из прядильной
шахты волокно содержит 12–40% диметилформамида; его физико-механические
свойства невысоки. Для улучшения свойств волокно подвергают вытяжке, но
предварительно отмывают избыток растворителя горячей водой (90–100°С).
Полиакрилонитрильное
волокно по своим свойствам напоминает шерсть и может быть окрашено различными
красителями. Если ему сообщить основные свойства, то окрашиваемость улучшается.
Для этого изготовляют сополимеры акрилонитрила, содержащие небольшие количества
винилпиридина, N-бензилакриламида и других азотсодержащих непредельных
соединений. Обработка их аммиаком или аминами (лучше всего гексаметилендиамином)
дает возможность получить материалы с небольшим содержанием основных групп.
Полиакрилонитрильное волокно обладает следующими свойствами [3, С. 356]:
Таблица 3. Свойства полиакрилонитрильного волокна
|
Свойство
|
Величина
|
|
Плотность, г/см3
|
1,17
|
|
Предел прочности при
растяжении, г/денъе
|
3–4
|
|
Относительное удлинение,
%
|
8–35
|
|
Относительная прочность
во влажном состоянии, %
|
90–98
|
|
Гигроскопичность (при
20 °С и 60% относительной влажности), %
|
1,0
|
|
Водопоглощение, %
|
1–2
|
|
Температура плавления,
°С
|
250
|
|
Устойчивость:
|
|
|
-к кислотам
|
Очень хорошая
|
|
-щелочам
|
Умеренная
|
|
-органическим
растворителям
|
Очень хорошая
|
Специальные
ПАН волокна, которые обычно используются для производства углеродного волокна,
имеют круглую форму поперечного среза, диаметр до 15 мкм, площадь поперечного
сечения до 180 мкм2 и низкую линейную плотность – до 0,17 текс.
Коммерческое текстильное ПАН волокно имело бобовидную форму поперечного
сечения, площадь сечения 530 мкм2, линейную плотность 0,56 текс,
прочность при растяжении 226 МПа и относительное удлинение при разрыве 43,9%
[4, С. 33].
Полиакрилонитрильное
волокно используется для изготовления изделий широкого потребления, технических
тканей (фильтры, войлок, специальные сукна), брезентов, транспортных лент,
рыболовных сетей в качестве наполнителя слоистых пластиков.
Заключение
Полиакрилонитрил
представляет собой линейный карбоцепной полимер содержащий сильно полярную группу
– СN, что в большей мере
определяет его свойства. Этот полимер очень капризен в выборе растворителя, что
необходимо учитывать как при его синтезе, так и при переработке.
Полиакрилонитрил
– хорошее сырье для получения термоустойчивых материалов, воздействие
повышенных температур позволяет модифицировать его свойства. Он хорошо
сополимеризуется с большим числом мономеров, а полученные сополимеры являются
востребованными промышленными продуктами (лаки, клеи, АБС пластик)
Волокна,
получаемые из полиакрилонитрила, обладают широким спектром свойств. В
частности, на основе полиакрилонитрила производят термостойкие углеродные
волокна.
С момента
открытия полиакрилонитрила прошло больше ста лет, но он продолжает оставаться
востребованным и занимает не последнее место среди промышленных полимеров.
Проводятся исследования по созданию все новых и новых материалов на его основе.
Список литературы
1.
Коршак
В.В. Технология пластических масс/ В.В. Коршак; под ред. В.В. Коршака.
– 3-е изд., перераб. и доп. – М.: Химия, 1985. -560 с.
2.
Лебедев,
Н.Н. Химия и технология основного органического и нефтехимического
синтеза/ Н.Н. Лебедев. – 3-е изд., перераб. – М.: Химия, 1975. -736 с.
3.
Николаев
А.Ф. Синтетические полимеры и пластические массы на их основе/А.Ф. Николаев. –
2-е изд., доп.-Л.: Химия, 1966. -768 с.
4.
Процесс
изготовления углеродных волокон на основе коммерческих полиакрилонитрильных
волокон мокрого формования/ R. Eslami Farsani и [др.] // Химические волокна. – 2006. –
№5. – С. 30–33.
5.
Семчиков
Ю.Д. Высокомолекулярные
соединения: учебник для вузов/ Ю.Д. Семчиков. – М.: Академия, 2003. –
368 с.
6.
Энциклопедия
полимеров: энциклопедия. В 3 т. Т. 1. А-К. – М.: Советская энциклопедия,
1972. -1224 с.