Для получения оксида азота(II) в пробирку помещают
немного медных стружек и заливают разбавленную азотную кислоту. Пробирку
закрывают пробкой с газоотводной трубкой и укрепляют в штативе. Конец
газоотводной трубки опускают в кристаллизатор с водой и далее в цилиндр (рис.
3). При нагревании выделяется NO. NO легко окисляется кислородом воздуха, т. е.
действует как восстановитель:

В реакции с сернистым газом оксид NO – окислитель:
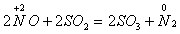
N+22O3
–
оксид азота(III), азотистый ангидрид (ему соответствуют азотистая кислота HNО2
и соли нитриты); это кислотный оксид, для него характерны все свойства
кислотных оксидов. Получают оксид N2O3 по реакции:
NO2 + NO  N2O3.
N2O3.
N+4O2–
оксид азота(IV), диоксид азота, бурый газ (токсичен).
Рассмотрим
электроны азота в молекуле NО. Это неспаренный электрон, свободная пара
электронов и еще два электрона на связи с кислородом – всего пять. А у атома
кислорода, «выходящего на связь», шесть электронов на четырех орбиталях. Если
расположить их по два, то одна орбиталь останется свободной. Именно ее и
занимает пара электронов атома азота (рис. 4, 5).

Рис. 4. Схема
электронного строения молекулы NO2 (первый вариант). (Точками обозначены электроны
атомов О, крестиками – электроны атома N)
Рис. 5. Схема
электронного строения молекулы NO2 (второй вариант). (Звездочкой обозначен
возбужденный атом O, стрелкой – донорно-акцепторная связь.
Раз пара
электронов, находящаяся на s-орбитали, «пошла на связь», она просто обязана
подвергнуться гибридизации. Возникает вопрос: какой тип гибридизации использует
атом? Ответ: три электронные орбитали азота находятся в состоянии sp2-гибридизации.
Молекула NO2 угловая, угол 134° (угол больше 120° потому, что 1
электрон отталкивает от себя электроны связи слабее, чем пара электронов) (рис.
6, 7).
Кристаллическая
решетка молекулярная, однако, поскольку сама молекула тяжелее NO и склонность к
димеризации у нее заметно выше, то плавиться и кипеть это вещество должно при
заметно более высоких температурах. Температура кипения составляет 21 °С,
поэтому при обычных условиях – 20 °С и 760 мм рт. ст. – оксид азота(IV)
жидкий.
Оксид азота (IV) в воде растворяется,
одновременно с ней реагируя, и получается при этом сразу две кислоты.
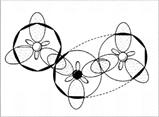
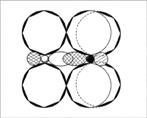
Рис. 6.
Молекула NO2 — вид «сверху»
Рис. 7.
Молекула NO2 – вид «сбоку», со стороны донорно-акцепторной связи.
(Второй атом кислорода не виден за орбиталями атома азота. Заштрихованные
кружки – это гибридизованные орбитали атомов, направленные к читателю.)
Оксид
азота(IV) имеет и характерный резкий запах, и рыжевато-бурый цвет, оттенки
которого отличаются друг от друга в зависимости от концентрации. Именно за этот
цвет выбросы оксидов азота в атмосферу называют «лисьими хвостами» [4].
Реакции оксида NO2
1) С водой:
2NO2 + Н2O = НNO3 +
НNO2.
2) С щелочами:
2NO2 + 2NaOH = NаNО3
+ NаNО2
+ Н2O.
3) Димеризация при охлаждении:

При температуре –11 °С равновесие полностью
смещено вправо, а при +140 °С – целиком влево.
N+52O5
– оксид азота(V), азотный ангидрид, кислотный оксид, сильный окислитель. Оксид
N2O5 легко разлагается:
2N2O5 = 4NO2
+ O2.
Из
гидроксидов азота мы рассмотрим наиболее многотоннажный – азотную кислоту.
Молекула
азотной кислоты полярна (из-за разной электроотрицательности кислорода и
водорода, потому что азот как бы скрыт внутри молекулы) и асимметрична. Все три
имеющихся в ней угла между связями азота с кислородом разные. Формальная
степень окисления азота высшая (+5). Но при этом только 4 связи у атома азота с
другими атомами – валентность азота равна 4.
Строение
молекулы легче понять, если рассмотреть процесс ее получения. Азотная кислота
получается при реакции оксида азота(IV) с водой (в присутствии кислорода): две
молекулы NO2 одновременно «атакуют» молекулу воды своими
неспаренными электронами, в результате связь водорода с кислородом разрывается
не как обычно (пара электронов у кислорода и «голый протон»), а одной молекуле
NO2 достается водород со своим электроном, другой – радикал ОН (рис.
8). Образуются две кислоты: обе кислоты сильные, обе быстро отдают свой протон
ближайшим молекулам воды и остаются в итоге в виде ионов NO2- и NO3-. Ион NO2- нестоек, две молекулы
НNО2 разлагаются на воду, NО2 и NО. Оксид NO реагирует с
кислородом, превращаясь в NО2, и так до тех пор, пока не получится
одна только азотная кислота.
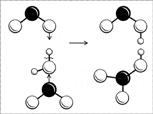
Рис. 8. Схема
образования молекул азотной и азотистой кислот. (Черный шар – атом N, большие белые шары –
атомы O,
маленькие белые шарики – атомы H.)
Формально
выходит, что с одним атомом кислорода атом азота связан двойной связью, а с
другим – обычной одинарной связью (этот атом кислорода связан еще и с атомом
водорода). С третьим атомом кислорода азот в HNO3 связан
донорно-акцепторной связью, причем в качестве донора выступает атом азота.
Гибридизация атома азота при этом должна быть sр2 из-за наличия
двойной связи, что определяет структуру – плоский треугольник. Реально
получается, что действительно фрагмент из атома азота и трех атомов кислорода –
плоский треугольник, только в молекуле азотной кислоты этот треугольник
неправильный – все три угла ОNО разные, следовательно, и разные стороны
треугольника. Когда же молекула диссоциирует, треугольник становится правильным,
равносторонним. Значит, и атомы кислорода в нем становятся равноценными.
Одинаковыми становятся и все связи.
Физические
свойства азотной кислоты
Соединение
ионизированное, пусть даже и частично, сложно перевести в газ. Таким образом,
температура кипения должна бы быть достаточно высокой, однако при такой
небольшой молекулярной массе температура плавления высокой быть не должна.
Следовательно, агрегатное состояние при 20°С жидкое. Что касается
растворимости, то, как и многие другие полярные жидкости, азотная кислота легко
смешивается с водой в любых соотношениях. Чистая азотная кислота бесцветна и не
имеет запаха. Однако из-за разложения на кислород и оксид азота(IV), который в
ней же и растворяется, можно сказать, что обычная концентрированная азотная
кислота имеет желто-бурый цвет и характерный для NO2 резкий запах.
Посмотрим, как влияет строение молекулы азотной кислоты на ее химические
свойства.
НNО3 – cильный окислитель
При взаимодействии НNО3 с металлами (М)
водород не выделяется:
М + НNО3 ® соль + вода +
газ.
Смесь HNO3 (конц.) с HCl (конц.) в
объемном соотношении 1:3 (1V
HNO3 + 3V HCl)
называют «царской водкой».
Au + HNO3 + 3HCl = AuCl3
+ NO + 2H2O.
+ 2H2O.
Азотная
кислота не реагирует с другими кислотами по типу реакций обмена или соединения.
Однако вполне способна реагировать как сильный окислитель. В смеси
концентрированных азотной и соляной кислот протекают обратимые реакции, суть
которых можно обобщить уравнением:


Образующийся
атомарный хлор очень активен и легко отбирает электроны у атомов металлов, а
хлорид-ион образует устойчивые комплексные ионы с получающимися ионами
металлов. Все это позволяет перевести в раствор даже золото. Концентрированная H2SO4 как сильное
водоотнимающее средство способствует реакции разложения азотной кислоты на
оксид азота(IV) и кислород. Азотная кислота – одна из сильных неорганических
кислот и, естественно, со щелочами реагирует. Реагирует она также и с
нерастворимыми гидроксидами, и с основными оксидами [4].
При изучении темы «Азот.
Соединения азота» пользуются учебником химии под редакцией Г.Е. Рудзитис, Ф.Г.
Фельдман, также учебником за 9 класс под редакцией Н.С. Ахметова. Дидактическим
материалом служит книга по химии для 8-9 классов под редакцией А. М. Радецкого,
В. П. Горшкова; используются задания для самостоятельной роботы по химии за 9
класс под редакцией Р.П. Суровцева, С.В. Софронова; используется сборник задач
по химии для средней школы и для поступающих в вузы под редакцией Г.П.
Хомченко, И.Г. Хомченко. На изучение этой темы отводится 7 ч [4, 5].
ГЛАВА 3.
МЕЖПРЕДМЕТНЫЕ СВЯЗИ ПРИ ИЗУЧЕНИИ III И V ГРУППЫ ПЕРИОДИЧЕСКОЙ СИСТЕМЫ
Д.И.МЕНДЕЛЕЕВА
3.1 III-А группа
Бор никогда
не встречается в природе в свободном состоянии, он всегда оказывается связанным
с кислородом. В этой форме он присутствует в борной кислоте Н3BO3,
которая содержится в воде горячих источников вулканических местностей. Кроме
того, в природе распространены многочисленные соли борной кислоты. Из этих
солей наиболее известна бура или тинкал Na2B4О7
. 10Н2О. Техническое значение имеют борацит 2Mg3B8O15
. MgCl2, пандермит Са2B6О11
. 3Н2О, колеманит Са2B6О11
. 5Н2О, кернит Na2B4О7 .
4Н2О.
Необходимо
указать и следующие минералы, которые являются производными борной кислоты:
борокальцит СаB4О7 . 4Н2О,
борнонатрокальцит NaСаB5О9 . 6Н2О,
гидроборацит MgCaB6О11 . 6Н2О,
боромагнезит 2Mg5B4О11 . 5Н2О,
сингалит MgAlBО4 и др. [9-11].
Бор и его
соединения имеют большое значение в народном хозяйстве. Изотоп 510B,
поглощающий нейтроны, применяют в ядерной технике для замедления ядерных цепных
реакций. Бура и борная кислота издавна применяется в медицине как антисептики.
Физиологическая
и биологическая активность бора очень высока. Бор способен влиять на важнейшие
процессы биохимии животных и растений. Вместе с Mn, Cu, Zn и Мо бор входит в
число пяти жизненно важных микроэлементов. Бор концентрируется в костях и
зубах, в мышцах, в костном мозгу, печени и щитовидной железе. Вероятно, что он
ускоряет рост и развитие организмов. Это видно из влияния бора на растения. При
борном голодании значительно уменьшается урожай и особенно количество семян.
Для жизнедеятельности животных важно его нахождение в молоке (коровьем) и в
желтке куриных яиц. Некоторые растения (кормовые травы и сахарная свекла)
собирают по несколько граммов бора с гектара угодий. Бор содержится в
значительных количествах в жировых тканях некоторых животных, пасущихся на
пастбищах, обогащенных бором. Состав соединений бора в организме неизвестен.
Установлено, что бор тормозит кишечную амилазу и кишечные протеиназы, усиливает
действие инсулина и тормозит окисление адреналина, ослабляет витамины В2
и В12. При избытке бора появляются борные энтериты. Избыточное
содержание бора ведет к заболеванию растений. Пшеница и овес страдают при
наличии 0,7 - 0,8 мгВ/кг почвы. Борьба с засолением почв бором ведется с
помощью промывки борных почв [9-11].
3.1.2
Алюминий
По своей
распространенности алюминий среди элементов занимает третье место, среди
металлов - первое. Он встречается главным образом в виде двойных силикатов, в
полевых шпатах и слюдах и в продуктах их выветривания - глинах. В свободном
состоянии алюминий никогда не встречается. Окись алюминия Al2O3
встречается в виде корунда и наждака. Из гидроокисей боксит AlO(OH) имеет
наибольшее техническое значение в качестве основного исходного продукта для
получения, Большое значение имеет также криолит Na3AlF6.
Из двойных
силикатов следует отметить: калиевый полевой шпат или ортоклаз K[AlSi3O8]
- главная составная часть изверженных пород: гранита, сленита, базальта,
кальциевый полевой шпат или анорит Сa[Al2Si2O8],
плагиоглаз, далее слюды: биотит, мусковый лепидалит, которые также содержатся в
изверженных породах. Силикат алюминия, содержащий фтор - топаз, относится к
числу драгоценных камней Al2(OH, F)2[SiO4]
[9-11].
При выветривании
полевых шпатов образуется каолин (фарфоровая глина), содержащий воду силикат
алюминия состава Al2O3 . 2SiO2 .
2H2O.
Сульфат
алюминия Al2(SO4)3 используется в качестве
протравы при крашении, для дубления кожи, в бумажном производстве. Сульфат
алюминия применяют для очистки природных вод от коллоидных частиц, загрязняющих
воду, которые захватываются гидроксидом алюминия, образующимся при этом
гидролизе соли.
Алюминий
имеет большое биологическое значение. Низкие концентрации ионов алюминия Al3+
стимулируют некоторые процессы жизнедеятельности растений. Например,
прорастание семян. Но более высокие концентрации снижают интенсивность
фотосинтеза, нарушают фосфорный обмен, задерживают рост корневой системы.
Некоторые производные алюминия применяют в медицине. Например, KAl(SO4)2
служит вяжущим средством. Основной ацетат алюминия AlOH(COOCH3)2
используется для дезинфекции [9-11].
3.1.3 Галлий
Галлий
встречается в природе как спутник цинка во многих обманках, но только в
исключительно малых количествах (0,002 % и меньше). В виде следов он встречается
почти как постоянный спутник алюминия. В всех сортах технического алюминия его
можно открыть спектрально. Самый богатый галлием минерал - германит. В нем
содержится 0,6 - 0,7 % галлия [9].
3.1.3.2 Токсикологическая характеристика
Долгое время
считалось, что галлий токсичен. Лишь в последнее время это мнение было
опровергнуто. Легкоплавкость галлия представляет интерес для стоматологов. Еще
в 1930 г. была испытана композиция для пломбирования зубов, в которой ртуть Hg
была заменена на галлий. И в настоящее время используются пломбы для
пломбирования зубов с использованием галлия [10].
3.2 V-A группа периодической системы
Газообразный N2 возникает в результате
реакции окисления NHH3, образующегося при извержении вулканов и разложении биологических
отходов:
4NH3 + 3O2 ® 2N2 + 6H2O.
Круговорот
азота – один из самых сложных, но одновременно самых идеальных круговоротов.
Несмотря на то, что азот составляет около 80% атмосферного воздуха, в
большинстве случаев он не может быть непосредственно использован растениями,
т.к. они не усваивают газообразный азот. Вмешательство живых существ в
круговорот азота подчинено строгой иерархии: только определённые категории
организмов могут оказывать влияние на отдельные фазы этого цикла. Газообразный
азот непрерывно поступает в атмосферу в результате работы некоторых бактерий,
тогда как другие бактерии – фиксаторы (вместе с сине-зелёными водорослями)
постоянно поглощают его, преобразуя в нитраты. Неорганическим путём нитраты
образуются и в атмосфере в результате электрических разрядов во время гроз.
Самые
активные потребители азота – бактерии на корневой системе растений семейства
бобовых. Каждому виду этих растений присущи свои особые бактерии, которые
превращают азот в нитраты. В процессе биологического цикла нитрат-ионы (NO3-) и ионы аммония (NH4+), поглощаемы растениями
из почвенной влаги, преобразуются в белки, нуклеиновые кислоты и т.д. Далее
образуются отходы в виде погибших организмов, являющихся объектами
жизнедеятельности других бактерий и грибов, преобразующих их в аммиак. Так
возникает новый цикл круговорота. Существуют организмы, способные превращать
аммиак в нитриты, нитраты и в газообразный азот. Основные звенья круговорота
азота в биосфере представлены схемой на рис. 10.

Рис. 10.
Круговорот азота
Биологическая
активность организмов дополняется промышленными способами получения
азотосодержащих органических и неорганических веществ, многие из которых
применяются в качестве удобрений для повышения продуктивности и роста растений.
Антропогенное
влияние на круговорот азота определяется следующими процессами:
1. Сжигание топлива приводит
к образованию оксида азота, а затем реакциям:
2NO
+ O2 ® 2NO2 ,
4NO2
+ 2H2O + O2 ® 4HNO3,
способствуя
выпадению кислотных дождей;
2. В результате воздействия
некоторых бактерий на удобрения и отходы животноводства образуется закись азота
– один из компонентов, создающих парниковый эффект;
3. Добыча полезных
ископаемых, содержащих нитрат-ионы и ионы аммония, для производства минеральных
удобрений;
4. При сборе урожая из почвы
выносятся нитрат-ионы и ионы аммония;
5. Стоки с полей, ферм и из
канализаций увеличивают количество нитрат-ионов и ионов аммония в водных
экосистемах, что ускоряет рост водорослей и других растений; при разложении
последних расходуется кислород, что приводит к гибели рыб. [12]
3.2.3 Соединения азота
Оксид
азота(I) относительно инертен, а потому «экологически нейтрален». Однако на
человека он оказывает наркотическое действие, начиная от просто веселья (за что
он и был прозван «веселящим газом») и, заканчивая глубоким сном, что нашло свое
применение в медицине. Интересно, что он безвреден, и для медицинского наркоза
применяют смесь оксида азота(I) с кислородом в таком же соотношении, что и
соотношение азота и кислорода в воздухе. Наркотическое действие снимается сразу
после прекращения вдыхания этого газа.
Два других
устойчивых оксида азота легко переходят один в другой, затем в кислоты, а затем
в анионы NO2- и NO3-. Таким образом, эти вещества представляют собой естественные
минеральные удобрения, если находятся в естественных количествах. В
«неестественных» количествах эти газы редко попадают в атмосферу в одиночестве.
Как правило, образуется целый «букет» ядовитых соединений, которые действуют
комплексно.
Например,
всего один завод азотных удобрений выбрасывает в воздух кроме оксидов азота,
азотной кислоты, аммиака и пыли от удобрений еще и оксиды серы, соединения
фтора, некоторые органические соединения. Ученые выясняют устойчивость
различных трав, кустов и деревьев к подобным «букетам». Уже известно, что, к
сожалению, ель и сосна неустойчивы и быстро погибают, однако белая акация,
канадский тополь, ивы и некоторые другие растения могут существовать в таких
условиях, более того, они способствуют удалению из воздуха этих веществ.
Сильное
отравление оксидами азота можно получить в основном при авариях на
соответствующих производствах. Ответная реакция организма будет разной из-за
различия в свойствах этих газов. «Едкий» NО2 в первую очередь
действует на слизистые оболочки носоглотки, глаз, вызывает отек легких; NО, как
малорастворимое в воде и не едкое вещество, проходит через легкие и попадает в
кровь, вызывая нарушения в центральной и периферийной нервных системах. Оба
оксида реагируют с гемоглобином крови, результат – гемоглобин перестает
переносить кислород.
Экологические
свойства азотной кислоты складываются из двух «половинок». Как сильная кислота,
она разрушающе действует не только на живые ткани (кожу человека, лист
растения), но и на почву, что достаточно актуально – кислотные (из-за
присутствия оксидов азота и серы) дожди, увы, не редкость. При попадании
кислоты на кожу возникает химический ожог, который болезненнее и заживает
значительно дольше, чем термический. Это были основные экологические свойства
катиона водорода.
3.2.3.1 Взаимодействие нитрат-иона с фауной
и флорой
Нитрат-ион –
неотъемлемая часть круговорота азота в природе. В обычных условиях и в
разбавленных растворах устойчив, слабо проявляет окислительные свойства, не
осаждает катионы металлов, тем самым способствуя транспортировке этих ионов с
раствором в почве, растениях и т. п.
Нитрат-ион
становится ядовитым только в больших количествах, нарушающих баланс других
веществ. Например, при избытке нитратов в растениях уменьшается количество
аскорбиновой кислоты. (Стоит напомнить, что живой организм настолько тонко
организован, что любое вещество в больших количествах нарушает равновесие и,
следовательно, становится ядовитым.)
Растения и
бактерии используют нитраты для построения белков и других необходимых
органических соединений. Для этого надо перевести нитрат-ион в ион аммония. Эта
реакция катализируется ферментами, содержащими ионы металлов (меди, железа,
марганца и др.). Из-за гораздо большей ядовитости аммиака и иона аммония в
растениях хорошо отработана и обратная реакция перевода иона аммония в нитрат.
Животные не
умеют строить все необходимые им органические соединения из неорганических –
отсутствуют соответствующие ферменты. Однако микроорганизмы, живущие в желудке
и кишечнике, этими ферментами обладают и могут переводить нитрат-ион в
нитрит-ион. Именно нитрит-ион и действует как отравитель, переводя железо в
гемоглобине из Fe2+ в Fe3+.
Соединение,
содержащее Fe3+ и называемое метгемоглобином, слишком прочно
связывает кислород воздуха, следовательно, не может отдавать его тканям. В
результате организм страдает от недостатка кислорода, при этом происходят
нарушения в работе мозга, сердца и других органов.
Обычно
нитрит-ион образуется не в желудке, а в кишечнике и не успевает перейти в кровь
и произвести все эти разрушения. Поэтому отравления нитратами достаточно редки.
Существует, правда, и другая опасность: в нашем организме есть много веществ, в
которых атомы водорода аммиака замещены на органические радикалы. Такие
соединения называют аминами. При реакции аминов с нитрит-ионами образуются
нитрозамины – канцерогенные вещества:

Они действуют
на печень, способствуют образованию опухолей в легких и почках. Интересно, что
активным замедлителем реакции образования нитрозаминов является давно нам
знакомая аскорбиновая кислота [4, 11-14].
4.1 Урок на тему «III-А
группа периодической системы химических элементов Д. И. Менделеева»
Занятие 1. Характеристика
химических элементов III-а группы периодической системы
Алюминий
Основные
цели. Формирование основополагающих понятий, умений и навыков. Характеристика
химических элементов III-a группы периодической системы. Строение атома,
физические и химические свойства, применение и получение алюминия.
Оборудование.
Периодическая система химических элементов, рис. 2, 1 б.
Вещества.
Алюминий.

ХОД ЗАНЯТИЯ
|
Основное содержание
|
Формы обучения
|
Методы обучения
|
Средства обучения
|
|
1. Актуализация знаний,
умений и навыков учащихся.
1) Перечислите химические
элементы IIIa группы периодической системы в порядке усиления их
металлических свойств.
|
|
|
Рис. 2
|
|
2) Электронная формула
внешнего энергетического уровня 3s23p1 принадлежит
атому:
а) бора; б) алюминия;
в) галлия; г) таллия.
|
|
|
|
3) Перечислите
физические и химические свойства и области применения алюминия, используя
рис. 21.3
|
|
|
|
2. Получение алюминия
|
|
|
Рис. 1, б
|
|
3. Подведение итогов
|
|
|
|
Краткое
сообщение на тему «Металлы III группы с точки зрения химика-эколога»
Опросить
учащихся.
Информация о
домашнем задании. § 50 ([3]). Напишите уравнения реакций, при помощи которых
можно осуществить превращения веществ:

Самоанализ урока
Занятие 2.
Оксиды и гидроксиды алюминия
Основные
цели. Формирование основополагающих понятий, умений и навыков. Углубить знания
учащихся об амфотерности оксидов и гидроксидов. Аквакомплексы,
гидроксокомплексы, химизм производства алюминия электролизом оксида алюминия.
Оборудование.
Схема производства алюминия (процесс электролиза), штатив с пробирками, рис. 1,
а.

Вещества.
Растворы AlCl3, NaOH, H2SO4.
ХОД ЗАНЯТИЯ
|
Основное содержание
|
Формы обучения
|
Методы обучения
|
Средства обучения
|
|
1. Амфотерность оксида
алюминия
|
|
|
|
|
2. Запись уравнений
реакций взаимодействия оксида алюминия с гидроксидом натрия и азотной
кислотой
|
|
|
|
3. Амфотерность
гидроксида алюминия. Запись ионных уравнений реакций. Разбор образования
аква- и гидроксокомплексов. Сверить запись уравнений реакций с домашним
заданием. Коллоидные частицы
|
|
Лабораторный опыт 21
|
|
4. Разбор химизма
образования гидроксида алюминия в производстве алюминия
|
|
|
рис. 3
|
|
5. Подведение итогов
|
|
|
|
Сообщение на
тему «Экологические аспекты переработки алюминийсодержащих руд»
Опросить
учащихся.
Информация о
домашнем задании. § 50; таблица 21.1 ([13, 28]).
Самоанализ
урока
Занятие 3. Гидролиз солей
алюминия
Основные
цели. Формирование основополагающих понятий, умений и навыков. Расширить знания
о гидролизе солей. Применение гидролиза солей.
Оборудование.
Штатив с пробирками, схема «Гидролиз солей».
Вещества.
Растворы сульфата или хлорида алюминия, лакмусовая бумага (лакмус) синяя,
фиолетовая.

ХОД ЗАНЯТИЯ
|
Основное содержание
|
Формы обучения
|
Методы обучения
|
Средства обучения
|
|
1. Актуализация знаний,
умений и навыков учащихся об амфотерности оксида и гидроксида алюминия
|
|
|
|
|
2. Гидролиз солей
алюминия:
а) анализ результата
опыта;
в) вывод
|
|
Лабораторный опыт 22(1)
|
Схема «Гидролиз солей»
|
|
3. Выполнение задания.
Напишите уравнения реакций, при помощи которых можно осуществить превращения
веществ:

|
|
|
|
|
4. Подведение итогов
|
|
|
|
Опросить
учащихся
Информация о
домашнем задании. § 50 ([13-15]).
Самоанализ
урока.
Знать: важнейшие свойства и
применение азота, аммиака, оксидов азота, азотной кислоты, нитратов; важнейшие
минеральные удобрения, условия их рационального хранения и использования;
устройство прибора для получения аммиака в лабораторных условиях; качественные
реакции на нитрат-ионы и ион аммония; химические реакции, лежащие в основе производства
аммиака и азотной кислоты, условия их осуществления; общие научные принципы
химического производства.
Уметь: давать характеристику
подгруппе элементов; составлять уравнения изученных реакций, рассматривать их с
точки зрения окислительно-восстановительных и ионных представлений; определять
на практике нитрат-ионы, а также ион аммония; решать комбинированные задачи.
Основные понятия:
донорно-акцепторный механизм образования связи, ион аммония, несолеобразующий
(безразличный) оксид, селитры, удобрения (туки), азотистый ангидрид, азотный
ангидрид, нитриды.
Контрольные вопросы
1.
Каково
строение атома азота?
2.
Каковы
возможные валентности и степени окисления азота?
3.
Где
в природе встречается азот?
4.
Как
получают азот в лаборатории и в промышленности?
5.
Каковы
физические свойства азота?
6.
Каковы
химические свойства азота? Напишите уравнения реакций.
7.
Где
применяется азот?
8.
Каково
строение молекулы аммиака? Какой тип химической связи в молекуле NH3?
9.
Как
образуется донорно-акцепторная связь в ионе аммония?
10.
Почему
аммиак способен окисляться?
11.
Каковы
физические свойства аммиака?
12.
Как
аммиак взаимодействует с водой и кислотами?
13.
Какие
два способа окисления аммиака вам известны? Приведите уравнения соответствующих
реакций.
14.
Где
применяется аммиак?
15.
Почему
соли аммония схожи с солями калия?
16.
Какова
растворимость в воде солей аммония?
17.
Как
получают аммиак в лаборатории и на производстве? Составьте уравнения реакций
получения NH3.
18.
Каковы
общие свойства солей аммония? Напишите уравнения реакций.
19.
Каковы
специфические свойства солей аммония? Подтвердите свой ответ уравнениями
реакций.
20.
Какова
качественная реакция на соли аммония? Составьте уравнение реакции.
21.
Какие
оксиды азота вам известны?
22.
Как
можно получить монооксид азота? Каковы его физические свойства?
23.
Как
можно получить диоксид азота? Каковы его физические свойства?
24.
Как
диоксид азота взаимодействует с водой и щелочами? Напишите уравнения реакций.
25.
Каковы
физические свойства азотной кислоты?
26.
Каково
строение молекулы азотной кислоты?
27.
Каковы
валентность и степень окисления азота в азотной кислоте?
28.
Как
можно получить азотную кислоту? Приведите уравнение реакции.
29.
Почему
азотная кислота является сильным окислителем?
30.
Как
азотная кислота взаимодействует с металлами?
31.
Какие
газообразные вещества могут выделяться при восстановлении азота в азотной
кислоте?
32.
Какие
металлы не взаимодействуют с концентрированной азотной кислотой? Почему?
33.
Как
взаимодействуют с разбавленной азотной кислотой медь и серебро? Напишите
уравнения реакций.
34.
В
какой таре можно хранить азотную кислоту?
35.
Как
разлагается азотная кислота?
36.
Как
взаимодействуют неметаллы с азотной кислотой? Приведите уравнения реакций.
37.
Какие
еще соединения азота вам известны?
38.
Как
называют соли азотной кислоты? Каковы их физические свойства?
39.
Какие
нитраты являются удобрениями?
40.
Какие
способы получения нитратов вам известны? Составьте уравнения реакций.
41.
Как
могут разлагаться нитраты при нагревании? Напишите уравнения реакций разложения
KNO3, Cu(NO3)2 и AgNO3.
42.
Почему
нитраты могут быть окислителями?
43.
Как
отличить нитраты от других солей?
44.
Какие
вещества называют удобрениями?
45.
Какие
виды удобрений вам известны?
46.
Перечислите
важнейшие удобрения каждой группы.
47.
Какие
элементы составляют семейство азота?
48.
Как
изменяются свойства элементов группы Vа и их соединений с увеличением атомного
номера? Почему?
Рассмотрим в
качестве примера разработки некоторых уроков по теме «Производство азотной кислоты».
4.1.2 Урок по теме
«Получение азотной кислоты»
Цель урока:
Рассмотреть процесс получения азотной кислоты в лабораторных условиях, изучить
и закрепить химизм процесса.
Приборы и
материалы: штатив, реторта, воронка, тубус, резиновая пробка, чашка с холодной
водой, печь или спиртовка
Реактивы:
концентрированная серная кислота, 15-20 г. нитрата натрия.
ХОД УРОКА
Собрать
прибор по рисунку 3. В реторту поместить 15-20 г NaNO3 и прилить через воронку,
вставленную в тубус столько концентрированной H2SO4, чтобы она покрыла соль.
Закрыть тубус стеклянной или резиновой пробкой и опустить конец реторты в сухую
колбу, помещенную в чашку с холодной водой. Осторожно нагревать реторту. Когда
в приемнике соберется несколько миллилитров кислоты, нагревание прекратить и,
дав реторте охладиться, разобрать прибор. Кислоту сохранить для следующих
опытов. Объяснить появление у нее окраски..
Остерегаться
попадания HNO3 на одежду или на руки: она быстро разрушает ткань, а на руках
появляются желтые пятна и ожоги.
Написать
уравнение реакции:
H2SO4 + NaNO3 ® HNO3 + NaHSO4
Вопросы:
Почему реакция проводят при несильном нагревании?
Сделайте вывод о проведенной работе[16-19].
4.1.3
Практическая работа на тему «Азотная кислота и
ее соли»
Цель урока:
Научиться применять полученные знания о свойствах азотной кислоты и ее солей на
практике.
ХОД УРОКА
I.
Организационный момент.
II.
Фронтальный опрос:
- Какие
реакции называют окислительно-восстановительными?
- Какие
химические свойства HNO3 вы знаете?
- Дождевая
вода после грозы содержит следы азотной кислоты. Чем это объясняется?
III. Индивидуальный
опрос
1-й учащийся
- задание №
2-й учащийся
- задание №
IV. Самостоятельная
работа
На оставшееся
время учитель раздает всем карточки с тремя заданиями, два из которых уже
разбирались на уроке, а третье задание - творческое, направлено на выявление
дополнительных знаний по данной теме.
Например,
такая карточка может выглядеть следующим образом:
Карточка
№ 1
1) Рассчитайте
массовую долю азота в следующих веществах:
а) N2O; б) N2O4; в)Cu(NO3)2; г)NH4NO3;
д)Fe(NO3)3.
2)
Напишите
уравнения реакций, с помощью которых можно осуществить цепь следующих
превращений:
NO2 ® HNO3 ® Ba(NO3)2 ® KNO3
3)
Почему
молекула NO2 легко димеризуется, а для SO2 подобный процесс не
характерен?
V. Домашнее задание:
Задача № 7;
2) Составить кроссворд на тему: «Азотная кислота и ее большое семейство». [3 (c. 55-60), 17-20]
ГЛАВА
5. ЗАДАЧИ И ТЕСТЫ
5.1
Задачи и тесты по теме «V-A группа ПС»
Задача 1. На
гашеную известь, взятую в небольшом количестве подействовали 3,15 кг чистой
азотной кислоты. Какую массу нитрата кальция Ca(NO3)2 получили, если практический
выход составляет 98%?
Дано:
m(HNO3) =
3,15кг.
wвых
(CaNO3) = 98%
m(CaNO3)-?
Решение:
Ca(OH)2
+2HNO3 ®Ca(NO3)2 + 2H2O
M
(HNO3)=63 г/моль; m (HNO3)=2×63 =126 кг.; M (Ca(NO3)2)=164
г/моль; m (Ca(NO3)2)=164
кг.
Находим
теоретический выход:
126:3,15=164×X1; m(Ca(NO3)2)теор
=4,1кг.
Находим 98% -
ный выход:
4,1 кг (Ca(NO3)2)
соотв. 100% - ному выходу
X2
-//- 98% - ному выходу
 кг
кг
Ответ: m
(Ca(NO3)2)практ. = 4,02 кг.
Задача 2.
Химический завод выбрасывает в атмосферу 120 т. нитрата аммония. Какова
ежесуточная потребность в аммиаке (в м3, при 0°С и 101,3 кПа)?
Дано:
m(NH4NO3)=120 т/сут.
M(NH4NO3)
= 80г.
V(NH3)-?
Решение:
NH3
+ HNO3 ®NH4NO3
M(NH4NO3) = 80г.
Составим
пропорцию:
X литров NH3
соответствуют 120×106 граммам NH4NO3
22,4 литров
NH3 соответствуют 80 граммам NH4NO3,
Тогда 

Ответ:
Ежесуточная потребность завода в аммиаке составляет 33600м3
Задача 3. Как
известно, памятник Кузьме Минину выполнен из бронзы (75% Cu, 25% Sn), поэтому
он постепенно разрушается под действием кислотных дождей. Написать реакцию
коррозии памятника. Какой объем газа выделится при полном разрушении памятника?
Какие меры принимаются для предотвращения коррозии? Масса памятника принимается
равной 2750 кг.
Дано:
w(Сu) = 75%
m = 2750кг.
_____________
V(NO2)
- ?
Решение:
4HNO3
+ Cu = Cu(NO3)2 + 2NO2 + 2NO2
2750 кг.®100%
X1кг®75% Сu
 кг.
кг.
Составляем
пропорцию:
2062,5
×103г. Cu ® X2 л. NO2
64
л. Cu ® 44,8 л. NO2
 л.
л.
Ответ: 1) при
полном разрушении памятника Кузьме Минину под действием кислотных осадков
выделится 1443,75 м3 NO2; 2) для предотвращения коррозии
памятник несколько раз в год протирают антикоррозионными органическими
веществами.
Задача 4.
Почва содержит 3,1 % органического вещества. Вычислить процентное содержание
(W) углерода и азота в почве, если органическое вещество содержит 60% углерода
и массовое отношение С:N=8:1.
Дано:
w(орг. в-ва) = 3,1%
w(C) = 60%
С:N=8:1.
_________________
Wс-?
WN-?
Решение:
Допустим, что
100% - это 100 г, тогда m (орг. в-ва) = 3,1г.
m(С) =  г.
г.
m(N) =  г.
г.
Процентное
содержание углерода и азота в 100 г почвы:
Wс=
WN=
(m(N) / m(почвы))× 100 %
WN
= (0,23г./100г.) × 100 % = 0,23%
Ответ:
Процентное содержание углерода и азота в 100 г = 1,86% и 0,23%.
Задача 5.
Свекла, выращенная в г. Курске имеет содержание нитратов 3000 мг/кг(что в 2
раза больше предельно допустимой концентрации). Сколько килограммов этой свеклы
надо счесть, чтобы смертельной дозы для человека (15гр.)?
 Решение:
Решение:
в 1кг. свеклы
®
3гр (NO3-)
d x кг.
свеклы ®
15гр (NO3-)
Ответ: 5кг
свеклы, выращенной в г. Курске, содержит смертельную дозу нитрат ионов [20, 26,
27].
Задача № 6. При нормальных
условиях 12 л газовой смеси, состоящей из аммиака и углекислого газа, имеют
массу 18 г. Сколько литров каждого из газов содержит смесь? Каковы объемные
доли каждого компонента в смеси?
Решение
Обозначим V(NH3)
= x л, V(CO2)
= (12 - x) л.
Тогда n(NH3)
= x/22,4 моль, n(СО2)
= (12 – x)/22,4 моль,
 ,
,  .
.
Составим уравнение:
 , х = 4,62 л NH3;
, х = 4,62 л NH3;
V(CO2)
= 12 – 4,62 = 7,38 л.
Найдем объемные доли газов в смеси:
j (NH3)
= 4,62/12 = 0,385 или 38,5%,
j (СО2) = 1 – 0,385 = 0,615 или 61,5%.
Задания для самоконтроля
1. Напишите уравнения практически осуществимых
реакций:
|
а) NH4Cl +
AgNO3 ® …;
в) AgCl + NH4NO3
® …;
д) HNO3 +
SiO2 ® …;
ж) Hg(NO3)2
 …; …;
и) Fe2O3
+ HNO3 ® …;
|
б) (NH4)2SO4
+ NaOH ® …;
г) HNO3 (разб.) + Cu ® …;
е) HNO3 +
MgCO3 ® …;
з) NH3 + O2
 …; …;
к) NH4Cl  …; …;
|
2. Напишите уравнения реакций следующих превращений:

3. Составьте схемы электронного баланса, расставьте
коэффициенты в уравнениях реакций:
а) HNO3
+ С  СО2 + NO
+ H2O;
СО2 + NO
+ H2O;
б) HNO3 + AsH3
 H3AsO4
+ NO2 + H2O;
H3AsO4
+ NO2 + H2O;
в) HNO3 + P +
H2O  H3PO4
+ NO;
H3PO4
+ NO;
г) HNO3 + CuS
 Сu(NO3)2
+ H2SO4 + NO + H2O;
Сu(NO3)2
+ H2SO4 + NO + H2O;
д) MnO2 + K2CO3
+ KNO3  K2MnO4
+ KNO2 + CO2;
K2MnO4
+ KNO2 + CO2;
е) K2CrO4
+ (NH4)2S + H2O  Сr(OH)3
+ KOH + NH4OH + S.
Сr(OH)3
+ KOH + NH4OH + S.
4. При взаимодействии 28 л (н. у.) аммиака с
раствором азотной кислоты массой 400 г, в котором содержится 0,24 массовые доли
HNO3, образуется нитрат аммония массой 90 г. Вычислите выход
продукта реакции в процентах от теоретически возможного. Ответ. 90%.
5. При нагревании технического нитрата меди(II)
массой 75,2 г выделяется кислород объемом 4 л (н. у.). Рассчитайте массовую
долю примесей в образце нитрата. Ответ.
10,7%.
6. Имеется смесь хлорида, карбоната и нитрата натрия
массой 50 г. Определите массовую долю каждого компонента смеси, если известно,
что при действии на нее избытка соляной кислоты выделяется газ объемом 2,24 л
(н. у.), а при прокаливании такой же массы смеси выделяется кислород объемом
2,24 л (н. у.). Ответ. w(NaCl)
= 44,8%, w(Na2CO3) = 21,2%, w(NaNO3)
= 34%.
7. При действии избытка разбавленной азотной кислоты
на образец известняка массой 80 г, содержащий 20% примесей, выделяется оксид
углерода(IV), который пропускают через раствор, содержащий 25,6 г гидроксида
натрия. Определите, какая соль (кислая или средняя) образуется. Какова ее
масса? Ответ. 53,76 г NaHCO3.
8. Определите, какая соль образовалась и какова ее
масса, если раствор гидроксида кальция объемом 200 мл, концентрация которого
0,2 моль/л, прореагировал с 9,8%-м раствором ортофосфорной кислоты массой 200
г.
Ответ. 9,36 г Са(Н2РО4)2.
9. Оксид фосфора(V), полученный окислением 31 г
фосфора, растворен в 495 г воды с образованием ортофосфорной кислоты. В этот
раствор пропущено 44,8 л аммиака. Определите состав полученной соли и ее
концентрацию в растворе (массовую долю в процентах). Ответ. 22% (NH4)2НРО4
[19-29].
.
5.2
Тесты
1. Определите
содержание по следующей характеристике: применяется в домашних холодильниках в
качестве охлаждающего средства, устойчив, сильно разрушает озоновый слой.
а) NH3
б) CF2Cl2 +
в) CFCl3
г) H2SO4
2. “Нашатырь”
получают на производстве в результате взаимодействия аммиака с хлороводородом,
реакция протекает ступенчато: NH3 + H2O = NH3×H2O, NH3×H2O + HCl = NH4Cl
+ H2O. Определите роль воды в суммарном процессе:
а)
растворитель
б)
промежуточный продукт
в) конечный
продукт
г)
катализатор +
3. Выберите
вещество, которое при возгорании нельзя тушить водой:
а) метан
б) аммиак
в) калий +
г) фосфор
4. Выберите
наиболее экологически чистое топливо из перечисленных ниже:
а) нефть
б) уголь
в) биомасса
в) природный
газ
д) солнечная
энергия +
5. В
атмосфере какого газа производят сварку активных или средней активности металлов,
хранят и перевозят произведения живописи:
а) неон
б) водород
в) азот +
г) аммиак
6. Как влияет
уменьшение содержания связанного азота в почве на растения?
а) при
недостатке азота задерживается рост и развитие растений, листья приобретают
бледно-зеленую окраску, а затем желтеют; +
б) при
недостатке азота задерживается рост и развитие растений и листья чернеют;
в) при
недостатке азота растения начинают цвести и листья приобретают особый оттенок,
так как азот является сдерживающим фактором.
7. В
современных установках получения азотной кислоты нет постоянных источников
сточных вод. Почему?
а) для
получения азотной кислоты нет необходимости использовать воду;
б) эти
установки потребляют большое количество оборотной охлаждающей воды, которую
периодически сливают в приямок и нейтрализуют; +
в) системы, в
которых используется для охлаждения вода, полностью заменены на системы с
воздушным охлаждением.
8. Назовите
важнейшие области применения аммиака в народном хозяйстве:
а) получение
сложных и азотных минеральных удобрений;
б)
производство синтетических красителей;
в) взрывчатые
вещества, нитролаки;
г)
пластические массы и лекарственные вещества;
д) все
варианты. +
9. Что
привело к существенному снижению количества сточных вод при производстве
аммиака?
а) применение
воздушного охлаждения; +
б) в
результате замены поршневых компрессоров трубокомпрессорами; +
в)
существенное снижение забора воды.
10. Какие
выбросы в окружающую среду характеризуют крупнотоннажное производство NH3?
а) газовые,
содержащие в своем составе NH3, оксиды азота и углерода и др.
примеси;
б) сточные
воды, состоящие из конденсата, продуктов промывки реакторов и систем
охлаждения,
в)
низкопотенциальную теплоту.
Ответ: все
11. Между атомами в молекуле азота существует:
а) двойная связь;
б) тройная связь; +
в) одинарная связь;
г) пять химических связей.
12. Азот достаточно инертен по
отношению к металлам, но сравнительно легко протекает следующая реакция:
а) Cu + N2 = ... ;
б) Zn + N2 = ... ;
в) Al + N2 = ... ;
г) Li + N2 = ... . +
13. Летучее водородное соединение
азота имеет формулу:
a) NH2;
б) N2H4;
в) NH3; +
г) NО2.
14. В какой реакции азот проявляет
восстановительные свойства? (б)

15. Вещество Mg3N2
называют:
а) нитрат магния;
б) нитрит магния;
в) сульфат магния;
г) нитрид магния. +
16. Сколько свободных электронных пар имеет азот в
молекуле аммиака?
а) 2;
б) 4;
в) 1; +
г) 3.
17. Аммиак в лаборатории получают по
реакции:
а) NH4Cl +
Ca(OH)2 = ... ; +
б) N2 + 3H2
= ... ;
в) Са3(PO4)2 + (NH4)2SO4
= ... ;
г) (NH4)3РO4 + HCl
= ... .
18. Выберите ряд веществ,
соответствующий нарастанию молекулярных масс:
а) озон, аммиак, кислород;
б) аммиак, кислород, озон; +
в) кислород, аммиак, озон;
г) кислород, озон, аммиак.
19. Аммиак может реагировать с
соляной кислотой по реакции NH3 + HCl = NH4Cl. Четвертый
атом водорода присоединяется по донорно-акцепторному механизму, при этом
донором является:
а) водород;
б) хлор;
в) азот; +
г) группа NH4+.
20. В аммиаке и катионе аммония
степень окисления азота одинаковая: –3. Какие валентности у атомов азота в этих
соединениях?
а) Обе – III;
б) обе – IV;
в) III и II;
г) III и IV. +
21. Нашатырный спирт – это:
а) NH3;
б) NH3•H2O; +
в) NH4Сl;
г) N2H4.
22. Для какой реакции повышение
давления сместит равновесие вправо?
а) N2 (г.) + О2 (г.) = 2NO
(г.);
б) Н2 (г.) + S (ж.) = Н2S
(г.);
в) N2 (г.) + 3Н2 (г.) = 2NН3
(г.); +
г) Н2 + Сl2 = 2НCl.
23. В лаборатории азотную кислоту
получают по реакции: (б)

24. При взаимодействии
концентрированной азотной кислоты с серебром помимо соли и воды выделяется газ:
а) NO2; +
б) NO;
в) N2;
г) N2О.
25. При термическом разложении
нитрата калия выделяется газ:
а) N2;
б) NO2;
в) О2; +
г) N2О.
26. Формула аммиачной селитры:
а) КNO3;
б) (NH4)3PO4;
в) NH4NO3; +
г) (NH4)2SO4
[30-34].
ЛИТЕРАТУРА
1.
Исидоров.
Химия атмосферы. М.: Мир, 1991.
2.
А.И.
Бусев, И.П. Ефимов. Определения, понятия, термины в химии. М.: Просвещение,
1981, 192 с.
3.
Рудзитис
Г.Е. Химия: Неорган. химия. Орган. Химия: Учеб. для 9 кл. общеобразовательных
учреждений. / Г. Е. Рудзитис., Ф. Г. Фельдман. – 10-е изд., испр. – М.:
Просвещение, 2001, с. 133 – 139.
4.
Экологическая
химия азота / www.1september.ru
5.
Ахметов
Н.С. Учебник для 9 класса общеобразовательных учреждений. М.: Просвещение, 1998
г.
6.
Программы
для общеобразовательных учреждений: Химия. 8-11 кл. Сост. Н.И.Габрусева. — М.:
Дрофа, 2000. — 192 с.
7.
Примерная
программа среднего (полного) общего образования по химии (профильный уровень). www.edu.ru
8.
Асадник
В.Н. Неорганическая химия. Блок-схемы, таблицы, формулы: Учеб. пособие. / В.Н.
Асадник. – Мн.: Книжный Дом, 2004. – с. 28 – 41.
9.
Реми.
Неорганическая химия. Т. 1.
10.
Олеин
С.С., Фадеев Г.Н. Неорганическая химия. Учебник для с/х вузов. М., 1979.
11.
Хомченко
Г.П. Неорганическая химия. М., 1978.
12.
М.Д.
Гольдфейн, Н.В. Кожевников, А.В. Трубников, С.Я. Шулов. Проблемы жизни в
окружающей среде. Учебное пособие. Химия. 1996г, №16.
13.
Денисов
В.В., Дрововозова Т.И. и др. // Химия. М.: Р- н/Д, Март, 2003
14.
Алпатьев
А.М. Развитие и преобразование окружающей среды. Л.: Наука, 1983
15.
Богдановский
Г.А. Химическая экология. М.: МГУ, 1994.
16.
Тарасова
Н.П., Кузнецов В.А. и др. Задачи и вопросы по химии окружающей среды. М.: Мир,
2002.
17.
Химия
в школе // Журнал. - М.: Просвещение, 2001, № 4, стр.16.
18.
Кутепов
А.М. и др. Общая химическая технология. Учеб. для техн. вузов. 2-е изд. М.:
Высш. шк., 1990, стр.148-162.
19.
Практикум
по неорганической химии. Учеб. пособие для студ. хим.-биол. фак-в пединст-в.
Изд. 2-е. М.: Просвещение, 1978. стр.180-183.
20.
Бабич
Л.И. Практикум по неорганической химии. Учеб.пособие.М.:Просвещение.1978,с.
312.
29.
Ахметов
М.А. Система обучающих заданий: творческий уровень. / Химия в школе, 2004, № 1,
с. 21 – 28.
30.
Сорокин
В.В., Злотников Э.Г. Проверь свои знания: Тесты по химии: Кн. для учащихся. –
М.: Просвещение: Учеб. лит., 1997.
31.
Н.Н.
Черняев, М.А. Ахметов. Тестовые задания и индивидуализация обучения / Химия в
школе, 2001, № 9.
32.
Суровцева
Р.П., Гузей Л.С., Останний Н.И., Татур А.О. Тесты по химии. 8-9 классы.
Учебно-методическое пособие. М.: Дрофа, 1997.
33.
Глориозов
П.А., Рысс В.Л. Проверочные работы по химии. 7, 8, 9, 10 классы. М.:
Просвещение, 1980, 1981, 1985.
34.
Гаврусейко
Н.П. Проверочные работы по неорганической химии. 8-9 классы. М.: Просвещение,
1990.